
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Trích mẫu thử, đánh số. Dùng thuốc thử: nước cho cả hai cặp chất (a), (b)
(a) Mẫu thử hoà tan trong nước là CaO, mẫu thử không tan là CaCO3
(b) Mẫu thử hoà tan trong nước là CaO, mẫu thử không tan là MgO
\(CaO_{ }+H_2O->Ca\left(OH\right)_2\)

a)(C6H10O5)n + nH20 (axit)------>nC6H12O6
b)C6H12O6 (men,30-35 độ) ------->2C2H5OH + 2CO2
1 tấn=1000000g
nC6H10O5=1000000/(12*6+1*12+16*6)=5555...
vì hiệu suất PỨ là 80% nên nC6H12O6=5555.6*80%=4444.48(MOL)
số mol C2H5OH gấp đôi số mol C6H12O6 nên nC2H5OH=4444.48*2=8888.96(MOL)
do hiệu suất phản ứng là 75% nên só mol thực tế là nC2H5OH=8888.96*75%= 6666.72(MOL)
mC2H5OH=6666.72*(12*2+1*6+16)~306.7(kg...

Có đề hoá và đáp án chi tiết ở các link mà cô đã cung cấp ở trên nhé
Nguyễn Quỳnh Trang Lê

(1) \(Cl_2+H_2\underrightarrow{t^o}2HCl\)
(2) \(2Fe+3Cl_2\underrightarrow{t^o}2FeCl_3\)
(3) \(Cl_2+2NaOH\rightarrow NaCl+NaClO+H_2O\)
(4) \(Cl_2+H_2O⇌HCl+HClO\)


(1) \(S+H_2\underrightarrow{t^o}H_2S\)
(2) \(Cu+S\underrightarrow{t^o}CuS\)
(3) \(S+O_2\underrightarrow{t^o}SO_2\)

Dùng H2O, quỳ tím và dd HCl để nhận biết được mỗi chất theo sơ đồ nhận biết sau đây:

1.
Theo đề bài ta có : \(\left\{{}\begin{matrix}nAl=\dfrac{0,54}{27}=0,02\left(mol\right)\\nH2SO4=\dfrac{120.4,9}{100.98}=0,06\left(mol\right)\end{matrix}\right.\)
PTHH :
\(2Al+3H2SO4->Al2\left(So4\right)3+3H2\uparrow\)
0,02mol...0,03mol.......0,01mol.............0,03mol
Theo PTHH ta có : nAl = \(\dfrac{0,02}{2}mol< nH2SO4=\dfrac{0,06}{2}mol=>nH2SO4\left(dư\right)\) ( tính theo nal)
=> VH2(đktc) = 0,03.22,4 = 6,72(l)
=> \(\left\{{}\begin{matrix}C\%ddH2SO4\left(dư\right)=\dfrac{\left(0,06-0,03\right).98}{0,54+120-0,03.2}.100\%\approx2,44\%\\C\%ddAl2\left(SO4\right)3=\dfrac{0,01.302}{0,54+120-0,03.2}.100\%\approx2,5\%\end{matrix}\right.\)
Theo đề bài ta có : nNa2O = \(\dfrac{15,5}{62}=0,25\left(mol\right)\)
a) PTHH :
\(Na2O+H2O->2NaOH\)
0,25mol....0,25mol.....0,5mol
b) Nồng độ mol dd A là :
CMddNaOH = 0,5/0,5 = 1(M)
c) PTHH :
\(2NaOH+H2SO4->Na2SO4+H2O\)
0,5mol.........0,25mol
=> mddH2SO4 = \(\dfrac{0,25.98}{20}.100=122,5\left(g\right)=>VddH2SO4=\dfrac{122,5}{1,14}\approx107,5\left(ml\right)\)
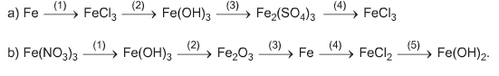
 Hãy viết phương trình hóa học theo các giai đoạn trên. Tính khối lượng rượu etylic thu được từ một tấn tinh bột.
Hãy viết phương trình hóa học theo các giai đoạn trên. Tính khối lượng rượu etylic thu được từ một tấn tinh bột.
 Sơ đồ 2
Sơ đồ 2 Đề thi học sinh giỏi Hóa
Đề thi học sinh giỏi Hóa Sơ đồ 1
Sơ đồ 1
a) (1) Fe + 2FeCl3 → 3FeCl2
(2) 3Ba(OH)2 + 2FeCl3 → 3BaCl2+ 2Fe(OH)3↓
(3) 2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 6H2O
(4) Fe2(SO4)3 + 3BaCl2 → 2FeCl3+ 3BaSO4↓
b) (1) 3NaOH+Fe(NO3)3→3NaNO3+Fe(OH)3↓
(2)2Fe(OH)3 t0 → Fe2O3+3H2O
(3)2Al + Fe2O3 → Al2O3+2Fe
(4)Fe + 2HCl→FeCl2+H2↑
(5) FeCl2 + 2NaOH → 2NaCl + Fe(OH)2