Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

cho chất p.p vào thì
chuyển sang màu hồng là;HCl, H2SO4
màu xanh: BaCl2,NaOH, Ba2SO4
ta kẻ bảng cho hai nhóm trên lần lượt tác dụng với nhau là ra

2 Lấy cùng một thể tích dd NaOH cho vào 2 cốc thủy tinh riêng biệt. Giả sử lúc đó mối cốc chứa a mol NaOH.
Sục CO2 dư vào một cốc, phản ứng tạo ra muối axit.
CO2 + 2NaOH → Na2CO3 + H2O (1)
CO2 + Na2CO3 + H2O → 2NaHCO3 (2)
Theo pt (1,2) nNaHCO3 = nNaOH = a (mol)
* Lấy cốc đựng muối axit vừa thu được đổ từ từ vào cốc đựng dung dịch NaOH ban đầu. Ta thu được dung dịch Na2CO3 tinh khiết
NaHCO3 + NaOH → Na2CO3 + H2O
1.Kết tủa A là BaSO4, dung dịch B có thể là H2SO4 dư hoặc Ba(OH)2
TH1: Dung dịch B là H2SO4 dư
Dung dịch C là Al2(SO4)3 ; Kết tủa D là Al(OH)3
TH2: Dung dịch B là Ba(OH)2
Dung dịch C là: Ba(AlO2)2 ; Kết tủa D là BaCO3
các pthh
BaO + H2SO4 → BaSO4 + H2O
BaO + H2O → Ba(OH)2
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Al2(SO4)3 + 3Na2CO3 + 3H2O → 2Al(OH)3 + 3CO2 + 3Na2SO4
Ba(OH)2 + 2H2O + 2Al → Ba(AlO2)2 + 3H2
Ba(AlO2)2 + Na2CO3 → BaCO3 + 2NaAlO2

Câu 1:
c) CM (HCl) dư = \(\frac{0,11}{0,25}\) = 0,44 (M)
ddAgồm \(\begin{cases}HCl:0,11mol\\AlCl_3:0,1mol\\CuCl_2:0,045mol\end{cases}\)
d) Các pư xảy ra theo thứ tự:
Mg + 2HCl \(\rightarrow\) MgCl2 + H2 (1)
Mg + CuCl2 \(\rightarrow\) MgCl2 + Cu (2)
3Mg + 2AlCl3 \(\rightarrow\) 3MgCl2 + 2Al (3)
Giả sử CR chỉ gồm Cu => ko xảy ra pt(3)
nCu = \(\frac{1,92}{64}\) = 0,03 (mol)
Theo pt(1) nMg= \(\frac{1}{2}\) nHCl = 0,055 (mol)
PT(2) nCu < nCuCl2 (0,03 < 0,045 )
=> CuCl2 dư
=> Giả sử đúng
mMg = (0,055 + 0,03) . 24 =2,04 (g)
Câu 3: a) Hiện tượng: Khi sục khí Cl2 vào nước vừa có tính chất vật lí , vừa tính chất hóa học:
- Vật lí: Có một phần khí tan trong nước
- Hóa học: Có chất mới tạo thành
PT: Cl2 + H2O \(\rightarrow\) HCl + HClO
b) Hiện tượng: tạo thành chất khí, cháy ở nhiệt độ cao hoặc có ánh sáng
PT: Cl2 + H2 \(\underrightarrow{t^0}\) 2HCl (khí)

Dùng phương án A. Nước vôi trong là tốt nhất vì nước vôi trong có phản ứng với tất cả các khí thải tạo thành chất kết tủa hoặc dung dịch. PTHH:
Ca(OH)2 +SO2 → CaSO3 ↓+ H2O
Ca(OH)2 +CO2 → CaCO3 ↓ + H2O
Ca(OH)2 +H2S → CaS + 2H2O
Ca(OH)2 + 2HCl → Cacl2 + 2H2O

+ Cho A tác dụng với dd NaOH dư:
Chất rắn A1: Fe3O4, Fe; dd B1: NaAlO2 và NaOH dư; khí C1: H2
+ Cho khí C1 tác dụng với A1
Fe3O4 + 2H2 ---> 3Fe + 4H2O.
Chất rắn A2: Fe, Al, Al2O3
+ Cho A2 tác dụng H2SO4 đặc nguội.
Al2O3+ 3H2SO4---->Al2(SO4)3+3H2O
Dd B2: Al2(SO4)3
+ Cho B2 tác dụng với dd BaCl2
Al2(SO4)3+ 3BaCl2--->2AlCl3+3BaSO4
B3: BaSO4
Xác định được các chất: A1, A2, B1, B2, B3, C1

A : CuO
B : C
C : CO2
D : Ca(OH)2
PTHH: 2CuO + C ---to→ 2Cu + CO2
CO2 + Ca(OH)2 → CaCO3 + H2O
A là CuO
B là C (trong dạng than)
C là CO2 và có CO
D là NaOH
PTHH: CuO+C=>Cu+CO2+CO
NaOH+CO2=>NaHCO3+H2O
NaOH+CO2=>Na2Co3+H2O

a) Để chứng minh dung dịch H2SO4 loãng có những tính chất hóa học của axit, ta thực hiện các thí nghiệm:
Cho axit H2SO4 loãng lần lượt phản ứng với Fe, CuO, KOH:
Fe + H2SO4 → FeSO4 + H2 (có khí thoát ra)
(kim loại Cu không tác dụng với dd H2SO4 loãng)
CuO + H2SO4 → H2O + CuSO4 (dung dịch có màu xanh lam)
2KOH + H2SO4 → K2SO4 + H2O
(Cho quỳ tím vào dung dịch KOH, dung dịch có màu xanh. Rót từ từ dung dịch H2SO4 thấy màu xanh dần biến mất đến khi dung dịch không màu)
b) Để chứng minh dung dịch H2SO4 đặc có những tính chất hóa học riêng ta thực hiện các thí nghiệm:
Cho axit H2SO4 đặc tác dụng với Cu đun nóng và với glucozơ:
Cu + H2SO4 đ, nóng → CuSO4 + SO2 + H2O
(Đồng bị hòa tan dần, dung dịch chuyển sang màu xanh và có khí mùi hắc thoát ra)
C12H22O11 \(\underrightarrow{H_2SO_4}\) 12C + 11H2O
(Đường bị hóa thành than và đẩy lên khỏi cốc)
a) dung dịch H2SO4 loãng có những tính chất hóa học của axit
2KOH + H2SO4 ---> K2SO4 + 2H2O
Fe + H2SO4 ---> FeSO4 + H2\(\uparrow\)
CuO + H2SO4 ---> CuSO4 + H2O
b) dung dịch H2SO4 đặc ngoài những tính chất hóa học của axit còn có những tính chất hóa học riêng
Cu + 2H2SO4 --t0--> CuSO4 +SO2\(\uparrow\) +2H2O
C6H12O6 --H2SO4--> 6C + 6H2O

Nhiệt phân hỗn hợp, ta có PTPƯ:
BaCO3 BaO + CO2
MgCO3 MgO + CO2
Al2O3 không
Chất rắn Khí D: CO2.
+ Hòa tan A vào H2O dư, ta có PTPƯ:
BaO + H2O Ba(OH)2
MgO + H2O không
Al2O3 + Ba(OH)2 Ba(AlO2)2 + H2O
Kết tủa
+ Khi cho dung dịch B tác dụng với CO2 dư:
Ba(AlO2)2 + 2CO2 + 4H2O 2Al(OH)3 + Ba(HCO3)2
+ Hòa tan C vào dung dịch NaOH dư, ta có PTPƯ:
MgO + NaOH không
Al2O3 + 2NaOH 2NaAlO2 + H2O
(Vì kết tủa C cho vào dung dịch NaOH dư có tan một phần chứng tỏ C có Al2O3 dư; phần không tan là MgO).

+ Điều chế khí cacbonic
CaCO3--->CO2+CaO
+ Điều chế dd NaOH
2NaCl+2H2O---->2NaOh+H2+Cl2
+ Các phản ứng đều chế muối
CO2+NaOh===>NaHCO3
NaHCO3+CO2+H2O--->Na2CO3+H2O
Cách tiến hành :
- Cho 2V dd NaOH vào hai cốc A và B sao cho VA = 2VB (dùng ống đong chia độ).
- Gọi số mol NaOH ở cốc A là 2a mol thì số mol NaOH ở cốc B sẽ là a mol
- Sục khí CO2 dư vào cốc A xảy ra phản ứng (1). Sau đó đổ cốc A vào cốc B xảy ra phản ứng (2). Như vậy ta thu được trong cốc B dung dịch 2 muối NaHCO3 và Na2CO3 có tỷ lệ 1:1
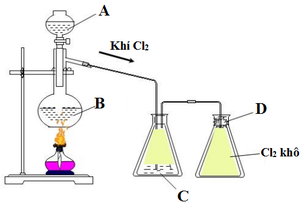

A: HCl
B: MnO2; KMnO4; KClO3
C: H2SO4 đặc
D: bông tẩm NaOH
Dung dịch C hấp thụ H2O làm khô khí Cl2.
Bông tẩm NaOH ngăn không cho khí Cl2 (độc hại) thoát ra ngoài môi trường.
MnO2 + 4HCl → MnCl2 + Cl2↑ + 2H2O
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
KClO3 + 6HCl → KCl + 3Cl2↑ + 3H2O