Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

+ Xét phản ứng: NH3 + HCl → NH4Cl
Chất cho proton là HCl, chất nhận proton là NH3:
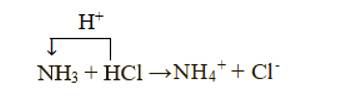
+ Xét phản ứng: NH3 + HNO3 → NH4NO3
Chất cho proton là HNO3, chất nhận proton là NH3:
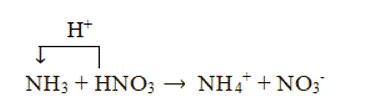
+ Xét phản ứng: 2NH3 + H2SO4 → (NH4)2SO4
Chất cho proton là H2SO4, chất nhận proton là NH3:
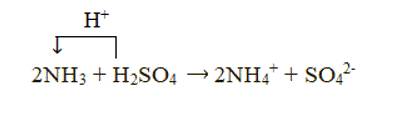

3AgNO3+Na3PO4\(\rightarrow\)Ag3PO4\(\downarrow\)+3NaNO3(sản phẩm có kết tủa)
BaCO3+HNO3\(\rightarrow\)Ba(NO3)2+CO2\(\uparrow\)+H2O(sản phẩm có chất khí-không có kết tủa)
Al2(SO4)3+3BaCl2\(\rightarrow\)3BaSO4\(\downarrow\)+2AlCl3(sản phẩm có kết tủa)
(NH4)2SO4+2KOH\(\rightarrow\)K2SO4+2NH3\(\uparrow\)+2H2O(sản phẩm có chất khí-không có kết tủa)

NH4NO2 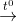 N2 + 2H2O; NH4NO3
N2 + 2H2O; NH4NO3  N2O + 2H2O
N2O + 2H2O
N có số oxi hóa +3 và +5 trong NO2- và NO3- : đóng vai trò chất oxi hóa.
N có số oxi hóa -3 trong NH4+: đóng vai trò chất khử.

1.
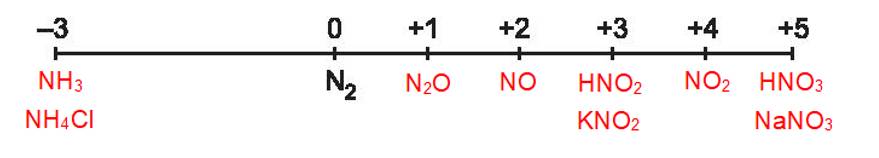
2. Khi tham gia phản ứng oxi hoá – khử, số oxi hoá của nitrogen có thể giảm hoặc tăng, do đó nitrogen thể hiện tính oxi hoá hoặc tính khử. Một số quá trình minh hoạ:
Quá trình oxi hoá: \(\mathop {{{\rm{N}}_{\rm{2}}}}\limits^{\rm{0}} \to {\rm{2}}\mathop {\rm{N}}\limits^{{\rm{ + 2}}} {\rm{ + 4e}}\)
Quá trình khử: \(\mathop {{{\rm{N}}_{\rm{2}}}}\limits^{\rm{0}} + {\rm{6e}} \to {\rm{2}}\mathop {\rm{N}}\limits^{ - 3} \)
Đáp án D
2 NH 3 + 2 Na → 2 NaNH 2 + H 2
Số oxi hóa của H giảm từ +1 xuống 0 nên NH 3 là chất oxi hóa