Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: 3Fe + \(2O_2\) --->\(Fe_3O_4\)
theo pt: 3_____2_____________1
theo đề: x______y_____________0.01
nFe3O4 là: 0.01mol
\Rightarrow nO2= 0.01*2/1=0.02 mol
VO2= 0.02*22.4=0.448l
b, PTHH : 2KMnO4 ----> K2MnO4 + MnO2 + O2
theo pt: 2__________1________1______1
theo đề: x___________________________0.02
=> n KMnO4= 0.02*2/1= 0.04 mol
=>mKMnO4= 0.04*158=6.32g
a. số mol của Fe3O4 là :
2.32 : 232 =0.01 mol
theo tỉ lệ mol ta có số mol của Fe là:
0.01 * 3 = 0.03 mol
khối lượng sắt là: 0.03*56=1.68g
số mol oxi là: 0.01*2=0.02mol
thể tích oxi là: 0.02*22.4= 0.448g
b. 2KMnO_4 ---> K2MnO4 + MnO2 + O2
---> nKMnO_4 = 2nO2 = 0,04 mol ---> mKMnO_4=0.04*158=6.32g

a) \(3Fe+2O_2-t^o->Fe_3O_4\)
b) \(n_{Fe}=\frac{5,6}{56}=0,1\left(mol\right)\)
Theo pthh : \(n_{Fe_3O_4}=\frac{1}{3}n_{Fe_3O_4}=\frac{0,1}{3}\left(mol\right)\)
=> \(m_{Fe_3O_4}=232\cdot\frac{0,1}{3}\approx7,73\left(g\right)\)
c) Theo pthh : \(n_{O2\left(pứ\right)}=\frac{2}{3}n_{Fe}=\frac{0,2}{3}\left(mol\right)\)
=> \(n_{O2\left(can.dung\right)}=\frac{0,2}{3}\div100\cdot120=0,08\left(mol\right)\)
=> \(V_{O2\left(can.dung\right)}=0,08\cdot22,4=1,792\left(l\right)\)

\(n_{Fe_3O_4}=\dfrac{2.32}{232}=0.01\left(mol\right)\)
\(3Fe+2O_2\underrightarrow{^{t^0}}Fe_3O_4\)
\(0.03......0.02.........0.01\)
\(m_{Fe}=0.03\cdot56=1.68\left(g\right)\)
\(m_{O_2}=0.02\cdot32=0.64\left(g\right)\)
\(2KMnO_4\underrightarrow{^{t^0}}K_2MnO_4+MnO_2+O_2\)
\(0.04............................................0.02\)
\(m_{KMnO_4}=0.04\cdot158=6.32\left(g\right)\)
a)
n Fe3O4 = 2,32/232 = 0,01(mol)
3Fe + 2O2 \(\xrightarrow{t^o}\) Fe3O4
0,03....0,02.......0,01...........(mol)
m Fe = 0,03.56 = 1,68(gam)
m O2 = 0,02.32= 0,64(gam)
c)
$2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
n KMnO4 = 2n O2 = 0,04(mol)
m KMnO4 = 0,04.158 = 6,32 gam

Bài 3 :
PTHH : \(6Fe+4O_2\left(t^o\right)->2Fe_3O_4\) (1)
\(n_{Fe_3O_4}=\dfrac{m}{M}=\dfrac{2,32}{56.3+16.4}=0,01\left(mol\right)\)
Từ (1) => \(3n_{Fe_3O_4}=n_{Fe}=0,03\left(mol\right)\)
=> \(m_{Fe}=n.M=1,68\left(g\right)\)
Từ (1) => \(2n_{Fe_3O_4}=n_{O_2}=0,02\left(mol\right)\)
=> \(V_{O_2\left(đktc\right)}=n.22,4=0,448\left(l\right)\)
Bài 4 :
PTHH : \(4P+5O_2\left(t^o\right)->2P_2O_5\) (1)
\(n_P=\dfrac{m}{M}=\dfrac{6,2}{31}=0,2\left(mol\right)\)
\(n_{O_2}=\dfrac{V}{22,4}=\dfrac{6,72}{32}=0,21\left(mol\right)\)
Có : \(n_P< n_{O_2}\left(0,2< 0,21\right)\)
-> P hết ; O2 dư
Từ (1) -> \(\dfrac{1}{2}n_P=n_{P_2O_5}=0,1\left(mol\right)\)
=> \(m_{P_2O_5}=n.M=14,2\left(g\right)\)
Bài 3:
\(n_{Fe_3O_4}=\dfrac{2,32}{232}=0,01\left(mol\right)\)
PTHH: 3Fe + 2O2 ---to→ Fe3O4
Mol: 0,03 0,02 0,01
\(m_{Fe}=0,03.56=1,68\left(g\right);V_{O_2}=0,02.22,4=0,448\left(l\right)\)

a) Phương trình hóa học của phản ứng:
3Fe + 2O\(_2\) → Fe\(_3\)O\(_4\).
nFe3O4 = \(\dfrac{2,32}{232}\) = 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.
a.
\(n_{Fe_3O_4}=\dfrac{2,32}{232}=0,01mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,03 0,02 0,01 ( mol )
\(m_{Fe}=0,03.56=1,68g\)
\(m_{O_2}=0,02.32=0,64g\)
b.
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,04 0,02 ( mol )
\(m_{KMnO_4}=0,04.158=6,32g\)

a, \(n_{Fe_3O_4}=\dfrac{6,96}{232}=0,03\left(mol\right)\)
PTHH: 3Fe + 2O2 ----to----> Fe3O4
Mol: 0,09 0,06 0,03
\(m_{Fe}=0,09.56=5,04\left(g\right)\)
\(m_{O_2}=0,06.32=1,92\left(g\right)\)
b,
PTHH: 2KClO3 ----to---> 2KCl + 3O2
Mol: 0,02 0,06
\(m_{KClO_3}=0,02.122,5=2,45\left(g\right)\)

a) Phương trình hóa học của phản ứng:
3Fe + 2O2 → Fe3O4.
nFe3O4 = 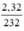 = 0,01 mol.
= 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.
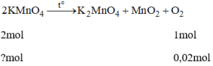
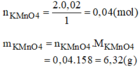
Đáp án C