Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nC=nCO2=0,672:22,4=0,03
=> mC=0,03.12=0,36 g
=> %C=60%
nH2O=2.nH=2.0,72/18=0,08
=< mH=0,08
=> %H=13,3%
=> %O=100-13.3-60=26,7%

mC = 0,67222,40,67222,4 x 12 = 0,360 (g); mH = 0,72180,7218 x 2 = 0,08 (g)
mO = 0,6 - (0,36 + 0,08) = 0,16 (g).
%mC = 0,360,60,360,6 x 100% = 60,0%;
%mH = 0,080,60,080,6 x 100% = 13,3%;
%mO = 100% - (%C + %H) = 26,7%.

Ta có: \(n_{COOH\left(X\right)}=n_{CO_2}=0,7mol\)
Khi đốt X có: \(n_{CO_2}=0,4mol;n_{CO_2}=0,8mol\)
Theo ĐLBT oxi có \(n_O=2n_{COOH\left(X\right)}+2n_{O_2}=2n_{CO_2}+n_{H_2O}\)
\(\Rightarrow n_{H_2O}=y=0,6mol\)

Ta thấy trong X có các ancol có đặc điểm: số C = số nhóm OH
=> Khi đốt cháy X : \(n_{CO_2}=n_{C\left(X\right)}=n_{OH}=0,25mol\)
=> Khi phản ứng vớ Na => \(n_{H_2}=\frac{1}{2}n_{OH}=0,125mol\)
=> V = 2,8 lít
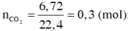
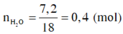
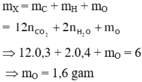
Đáp án C