Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Từ kí hiệu ta thấy nguyên tử Ar có số đơn vị điện tích hạt nhân là 18; vậy Ar có 18 prôtn, 18 electron và có 40-18= 22 nơtron
b) Lớp vỏ electron của nguyên tử có 18e được phân bố như sau : 1s2 2s2 2p6 3s2 3p6.

Gọi số p,e,n trong của M và X lần lượt là p1,e1,n1 , p2,e2,n2
=> 2(p1+e1+n1) + ( p2+e2+n2)=140
Mà số p=số e
=> 2(2p1 + n1) + ( 2p2 + n2) = 140 <=> (4p1+2p2) + (2n1+n2)=140 (I)
Lại có : (4p1+2p2)-(2n1+n2)=44 (II)
Từ (I) và (II ) => \(\left\{{}\begin{matrix}4p1+2p2=92\left(1\right)\\2n1+n2=48\end{matrix}\right.\)
Lại có : (p1 + n1) - (p2+n2)=23 (III)
(2p1 + n1 -1) - (2p2+n2+2) =31 (IV)
Từ (III) và (IV) => \(\left\{{}\begin{matrix}p1-p2=11\left(2\right)\\n1-n2=12\end{matrix}\right.\)
Từ (1) và (2) => \(\left\{{}\begin{matrix}p1=19\\p2=8\end{matrix}\right.\)
=> số e của M là 19 e
số e của X là 8 e
=> cấu hình e của M là : 1s22s22p63s23p64s1
cấu hình e của X là : 1s22s22p4

ta có : Tổng số hạt cơ bản trong 1 nguyên tử là 95
\(\Rightarrow p+e+n=95\Leftrightarrow2p+n=95\) \(\left(1\right)\)
ta có : tỉ số giữa hạt proton + nơtron so với hạt electron là \(\dfrac{13}{6}\)
\(\Rightarrow\dfrac{p+n}{e}=\dfrac{p+n}{p}=\dfrac{13}{6}\Leftrightarrow6\left(p+n\right)=13p\)
\(\Leftrightarrow6p+6n=13p\Leftrightarrow6p+6n-13p=0\Leftrightarrow-7p+6n=0\) \(\left(2\right)\)
- từ \(\left(1\right)\) và \(\left(2\right)\) ta có hệ phương trình : \(\left\{{}\begin{matrix}2p+n=95\\-7p+6n=0\end{matrix}\right.\)
giải ra ta có : \(\left\{{}\begin{matrix}p=30\\n=35\end{matrix}\right.\) \(\Rightarrow\) kẻm \(\left(Zn\right)\)
vậy \(p=e=30\) và \(n=35\)

Cái nguyên tử X mình làm ko ra bạn xem lại đề cái 53,125 nếu là 53,125% thì bạn giải ra đươc p = 16 và n = 17 đó là lưu huỳnh ( ra nghiệm đẹp mình nghĩ là đúng )
Ta có 2p + n = 8 và n = 52,63/100 . ( p + n ) từ hệ trên bạn giải ra p = 9 và n = 10 đó là Flo

z = 18 suy ra trong hạt nhân Ar có 18p và 22n (40 - 18), lớp vỏ electron của nguyên tử có 18e được phân bố như sau : ls2 2s2 2p6 3s2 3p6.

3. Khối lượng mol của hợp chất đó là :
2.28 = 56 (g/mol)
mC = \(\frac{56.85,7}{100}\approx48\left(g\right)\)
mH = 56 - 48 = 8 (g)
nC = \(\frac{48}{12}=4\left(mol\right)\)
nH = \(\frac{8}{1}=8\left(mol\right)\)
Vậy công thức hóa học là C4H8.

a) Tổng khối lượng của electro: 7 x 9,1.10 -28 = 63,7.10 -28 g
Tổng khối lượng của proton : 7 x 1.67.10 -24 = 11,69.10 -24 g
Tổng khối lượng của nơtron : 7 x 1.675.10 -24 = 11,72.10-24g
Khối lượng của nguyên tử nitơ là : 23,42.10 -24 g.
b) 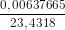 .100% = 0,027%.
.100% = 0,027%.

4Na + O2 ------------> 2Na2O ( cần nhiệt độ )
2. Na2O + H2SO4 ------> Na2SO4 + H2O
3. Na2O + H2O -----> 2NaOH
4. Na2O + H2CO3 ------> Na2CO3 + H2O
5. 2NaOH + H2SO4 ---> Na2SO4 + 2H2O
6. Na2SO4 + Ba(OH)2 ----> BaSO4 + 2NaOH
7. Na2CO3 + Ca(OH)2 ----> 2NaOH + CaCO3
8. 2NaOH + H2CO3 ----> Na2CO3 +2H2O
9. NaOH + HCl ---> NaCl +H2O
10. Na2CO3 + BaCl2 -----> 2NaCl + BaCO3
11. Na2SO4 + BaCl2------> 2NaCl + BaSO4
bổ sung phương trình 12. từ NaCl thành Na2SO4 :
2NaCl + Ag2SO4 ---> Na2SO4 + 2AgCl
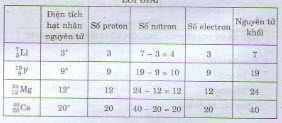
Đáp án đúng : C