Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
10,36 gX + 0,12 mol HCl → X có 0,12 mol NH2→ mN(X) = 1,68 g → mO(X) =1,68:7.16 = 3,84 g
nO =0,24 mol → nCOOH = 0,24 :2 =0,12 mol
X chứa 0,12 mol COOH + 0,15 mol NaOH → 0,12 mol H2O
Áp dụng định luật bảo toàn khối lượng
mX +mNaOH = mrắn + mH2O → mrắn = 10,36 + 0,15.40-0,12.18=14,2
Đáp án A
Chú ý:
Sai lầm và chú ý:
Trong rắn thu được có cả muối và NaOH

10 , 36 g X + 0 , 12 m o l H C l → X c ó 0 , 12 m o l N H 2
→ m N ( X ) = 1 , 68 g a m → m O ( X ) = 1 , 68 7 .16 = 3 , 84 g a m
n O = 0 , 24 m o l → n C O O H = 0 , 24 : 2 = 0 , 12 m o l
X chứa 0,12 mol COOH + 0,15 mol NaOH → 0 , 12 m o l H 2 O
Áp dụng định luật bảo toàn khối lượng
m X + m N a O H = m r a n + m H 2 O → m r a n = 10 , 36 + 0 , 15.40 − 0 , 12.18 = 14 , 2 g a m
Đáp án cần chọn là: A

Đáp án D.
Ta có: mO : mN = 16 : 7
⇒ nO : nN = 1 : 0,5.
⇒ Hỗn hợp X đã cho có hai nhóm ∑n–COOH = ∑n–NH2.
⇒ nNaOH phản ứng = nHCl = 0,12 mol
⇒ nH2O tạo thành = 0,12 mol
⇒ BTKL ta có m = 10,36 + 0,25 x 40 – 0,12 x 18 = 18,2 gam.

Ta có: mO : mN = 16 : 7 ⇒ nO : nN = 1 : 0,5.
⇒ Hỗn hợp X đã cho có hai nhóm ∑n–COOH = ∑n–NH2.
⇒ nNaOH phản ứng = nHCl = 0,12 mol ⇒ nH2O tạo thành = 0,12 mol
Chọn A

Cho m gam hỗn hợp X gồm ( Fe , FeO , Fe2O3 ) có tỷ lệ khối lượng tương ứng là 7:18:40 .Hỗn hợp X tan vừa hết trong 500 ml H2SO4 loãng 0,68 M thu được dung dịch B và thoát ra V lít khí H2 ( đktc). Cho dung dịch B tác dụng NaOH dư lọc kết tủa nung khô trong không khí thu được 22,4 gam chất rắn. Giá trị của V là ?
A. 0,448
B. 0,896
C. 2,24
D. 1,12

Đáp án B
Ta có: n N : n O = 1 : 2 nên n N H 2 : n C O O H = 1 : 1 .
Suy ra khi tác dụng với 0,15 mol NaOH thì dư ra 0,03mol NaOH.
Áp dụng sự tăng giảm khối lượng, ta có:
mrắn = mmuối + mNaOH dư = (mX + 22.nNaOH pư) + 0,03.40
= 10,36 + 22.0,12 + 0,03.40 = 14,2 gam.

Đáp án B
Gọi công thức của amino axit là: ( H 2 N ) x R ( C O O H ) y
Ta có:
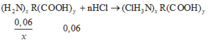
![]()
![]()
Mặt khác ta có:
![]()
→ n N a O H = n - C O O H = 0 , 06 m o l < n N a O H (đề)
→ NaOH dư
→ n H 2 O = n N a O H ( P U ) = 0 , 06 m o l
Áp dụng định luật bảo toàn khối lượng ta có:
m
=
m
X
+
m
N
a
O
H
-
m
H
2
O
=
7
,
1
(
g
)

gọi công thức ban đầu của hợp chất axit hữu cơ mà R(COOH)x
theo bài ra :2 A + xNa2CO3 ---> 2R(COONa)x + xCO2 + xH2O
khối lượng muối tăng lên là khối lượng của Na = ( 22,6 - 16) / 22 = 0,3
từ phương trinh trên = > nA = 0,3/x = 0,175 = > x = 1,7 => axit 1 chức và axit 2 chức.
gọi công thức của 2 axit là : Cn1H2n1+1COOH : a mol và Cn2H2n2(COOH)2 : b mol
viết phương trình phản ứng cháy của hỗn hợp trên , kết hợp với dữ liệu n kết tủa = nCO2 = 47,5 : 100 = 0,475 mol
ta có : \(\begin{cases}a+b=0,175\\a+2b=0,3\\\left(n1+1\right)a+\left(n2+2\right)b=0,475\end{cases}\)giải hệ ta được a = 0,05 , b = 0,125 và pt : 2n1 + 5n2=7 => n1= 1 và n2= 1 => ct : C2H4O2 Và C3H4O4
10,36 g X +vừa đủ 0,12 mol HCl
=>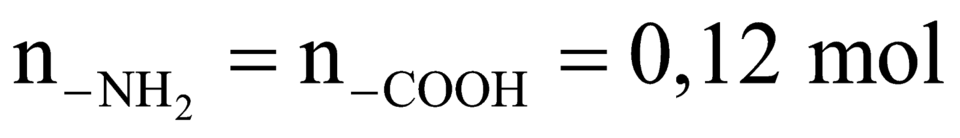
10,36 g X + 0,15 mol NaOH
Chọn đáp án A