Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án D
Ta có: n N a O H = 0 , 3 → n X = 0 , 3 n R C O O N a = 25 , 56 → m X = 25 , 56 - 22 . 0 , 3 = 18 , 96
Ta gọi: n C O 2 = x n H 2 O = y → 44 x + 18 y = 40 , 08 12 x + 2 y = 18 , 96 - 0 , 3 . 2 . 16 → x = 0 , 69 y = 0 , 54
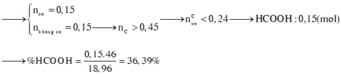

gọi công thức ban đầu của hợp chất axit hữu cơ mà R(COOH)x
theo bài ra :2 A + xNa2CO3 ---> 2R(COONa)x + xCO2 + xH2O
khối lượng muối tăng lên là khối lượng của Na = ( 22,6 - 16) / 22 = 0,3
từ phương trinh trên = > nA = 0,3/x = 0,175 = > x = 1,7 => axit 1 chức và axit 2 chức.
gọi công thức của 2 axit là : Cn1H2n1+1COOH : a mol và Cn2H2n2(COOH)2 : b mol
viết phương trình phản ứng cháy của hỗn hợp trên , kết hợp với dữ liệu n kết tủa = nCO2 = 47,5 : 100 = 0,475 mol
ta có : \(\begin{cases}a+b=0,175\\a+2b=0,3\\\left(n1+1\right)a+\left(n2+2\right)b=0,475\end{cases}\)giải hệ ta được a = 0,05 , b = 0,125 và pt : 2n1 + 5n2=7 => n1= 1 và n2= 1 => ct : C2H4O2 Và C3H4O4

Đáp án C
- Do X tác dụng với AgNO3 sinh ra Ag
=> Trong X có một este dạng HCOOR1
- Mà cho X td với NaOH thu được 2 muối của 2 axit cacboxylic đồng đẳng kế tiếp
=> este còn lại có dạng CH3COOR2
nHCOOR1=0,5nAg=0,1 mol
=> nCH3COOR2=0,25-0,1=0,15 mol
=>Tỉ lệ mol của HCOOR1 và CH3COOR2 là 2/3
Trong 14,08 gam X:
![]()
![]()


Trong 0,16 mol E chứa x mol X và y mol Y
nE = x + y = 0,16
nNaOH = 2x + 3y= 0,42
=> x = 0,06 và y = 0,1 (mol)
=> nX : nY = 3: 5
Trong m gam E chứa X (3e mol) và Y (5e mol).
X = C3H6(OH)2 + 2HCOOH + ?CH2 – 2H2O
Y = C3H5(OH)3 + 3HCOOH + ?CH2 – 3H2O - 3H2
Quy đổi m gam E thành:
C3H6(OH)2: 3e
C3H5(OH)3: 5e
HCOOH: 21e
CH2: u
H2: -15e
H2O: -21e
nO2 = 4.3e + 3,5.5e + 0,5.21e + 1,5u – 0,5.1,5e = 0,5
nCO2 = 3.3e + 3.5e + 21e + u = 0,45
=> e = 0,005 và u = 0,225
n muối no = 6e = 0,03 (mol)
n muối không no = 15e = 0,075 (mol)
Muối no và muối không no có tương ứng k và g nhóm CH2.
nCH2 = 0,03k + 0,075g = 0,225
=> 2k + 5g = 15
Do k > 1 và g ≥ 2 nên k = 2,5 và g = 2 là nghiệm duy nhất.
Vậy muối no gồm HCOONa: 0,03 (mol) ; CH2: 0,03k = 0,075 (mol)
=> m muối no = 3,09
Tỉ lệ: 8e mol E → 3,09 gam muối no
=> 0,16 mol E → a gam muối no
=> a = 12,36 (g)
Đáp án cần chọn là: C

Ta có nNaOH = 0,3= naxit = n este suy ra nO trong axit= 0,3.2 = 0.6 mol
Và ta có maxit = m muối – 22.0,3= 18.96g
Đốt cháy X thu được sản phẩm cho vào bình NaOH :
Thu được mkhối lượng bình tăng = mCO2 + mH2O = 40,08g
Suy ra số mol O2 phản ứng là : (40,08 - 18,96)/32 = 0,66 mol (bảo toàn khối lượng)
Bảo toàn O: ta suy ra được nCO2 = 0.69 mol và nH2O = 0.54 mol
Ta có naxit không no = nCO2 - nH2O = 0,15 mol
Số H trung bình trong hỗn hợp axit = (0,54.2)/0,3 = 3,6 (mà axit k no có số H ít nhất là 4 nên axit no là HCOOH) → m axit không no = 18,96- 0,15.46 = 12,06g
→ Đáp án B

Đáp án là B
Ta có nNaOH = 0,3= naxit = n este
suy ra nOtrong axit= 0,3.2 = 0.6 mol
Và ta có
maxit = m muối – 22.0,3= 18.96g
Đốt cháy X thu được sản phẩm cho vào bình NaOH :
Thu được
mkhối lượng bình tăng = ![]()
= 40.08g
Suy ra số mol O2 phản ứng là=( 40.08-18.96) /32=0.66 mol (bảo toàn khối lượng)
Bảo toàn O:
![]() = 0.69 và
= 0.69 và![]() =0.54
=0.54
Ta có
naxit không no = ![]() -
- ![]()
=0.15 mol
Số H trung bình trong hỗn hợp axit = 0.54*2/0.3 = 3.6 ( mà axit k nó có số H ít nhất là 4 nên axit no là HCOOH)
=> m axit không no = 18.96- 0.15*46
= 12.06g

Chọn A