Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Dựa vào hiệu độ âm điện, trong:
* Na2O: liên kết ion.
* MgO: liên kết ion.
* HBr: liên kết công hóa trị phân cực.
* CaBr2: liên kết ion.

So sánh | Liên kết ion | Liên kết cộng hóa trị không có cực | Liên kết cộng hóa trị có cực |
Giống nhau | Các nguyên tử kết hợp với nhau để tạo ra cho mỗi nguyên tử lớp electron ngoài cùng bền vững giống cấu trúc khí hiếm ( 2e hoặc 8e ). | ||
Khác nhau về cách hình thành liên kết | Cho và nhận electron | Dùng chung e, cặp e không bị lệch | Dùng chung e, cặp e bị lệch về phía nguyên tử có độ âm điện mạnh hơn. |
Khác nhau về nguyên tố tạo nên liên kết | Giữa kim loại và phi kim | Giữa các nguyên tử của cùng một nguyên tố phi kim | Giữa phi kim mạnh yếu khác nhau |
Nhận xét | Liên kết cộng hóa trị có cực là dạng trung gian giữa liên kết cộng hóa trị không cực và liên kết ion. |

Đáp án A
X là F, Y là K, Z là O. Liên kết cộng hóa trị phân cực tạo bởi F và O.

Ta có ![]()
Y có số lớp e lớp ngoài cùng là 7 nên là 1 halogen.
Vậy lk giữa X và Y là XY: lk ion
Đáp án D

Chọn B
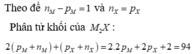
X chiếm 8/47 phần khối lượng => Nguyên tử khối X=16 và M=39
=> Số proton trong X là 8 (oxi), trong M là 19 (kali)
Hợp chất K 2 O có liên kết ion.

Chọn B
Cấu hình electron nguyên tử X là: [Ar]4s2 → X là kim loại nhóm IIA
X có xu hướng nhường 2e khi hình thành liên kết hóa học:
X → X2+ + 2e
Cấu hình electron nguyên tử Y là: [He]2s22p5 → Y là phi kim nhóm VIIA
Y có xu hướng nhận 1e khi hình thành liên kết hóa học:
Y + 1e → Y-
Vậy hợp chất tạo thành là XY2, liên kết tạo thành trong hợp chất là liên kết ion.