

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



a.
BTKL ta có mX = mY => nX . MX = nY . mY
MX / My = nY / mY =0.75
Đặt nX = 1 mol => nY = 0,75 mol => nH2 phản ứng = 1 – 0,75 = 0,25mol
* TH hidrocacbon là anken: n anken = n H2 = 0,25 mol => n H2 trong X = 0,75 => M = (6,75 – 0,75 . 2)/0,25 = 21 (loại) * TH là ankin: => n akin = 0,25/2 = 0,125 => n H2 trong X = 0,875 mol => M = (6,75 – 0,875 . 2)/0,125 = 40 =>C3H4
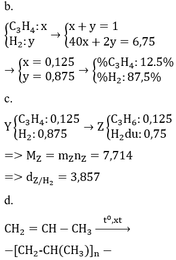


. 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O (1)
a/158 mol ............................................... a/63,2 mol
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O (2)
a/87 mol ..............................a/87mol
Ta có: a/63,2>a/87. Vậy khí clo ở phản ứng (1) thu được nhiều hơn phản ứng (2)
b. 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O (1’)
amol 2,5a mol
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O (2’)
amol a mol
Ta có 2,5a > a. Vậy dùng KMnO4 để điều chế thì thu được nhiều khí clo hơn so với dùng MnO2 khi lấy cùng khối lượng cũng như số mol.

2Cu + O2------>2CuO (có nhiệt độ )
CuO + H2SO4(đặc nóng ) ----> CuSO4 + H2
H2 + KOH -----> K + H2O( có nhiệt độ )

Hỗn hợp khí gồm CO2, SO2 và C2H4 gồm có 2 oxit axit tác dụng được với kiềm và 2 chất có thể tác dụng với brom trong dung dịch nên khi cho hỗn hợp vào dung dịch chứa một chất tan A, thì còn lại một khí B đi qua dung dịch sẽ có hai trường hợp:
- Trường hợp 1: Chất A là kiềm thì 2 oxit axit phản ứng và bị giữ lại trong dung dịch kiềm, còn lại khí B là C2H4 không phản ứng và đi qua dung dịch kiềm.
Các PTHH: CO2 + 2NaOH ---> Na2CO3 + H2O SO2 + 2NaOH ---> Na2SO3 + H2O
- Trường hợp 2: Chất A là dung dịch nước brom, hai chất phản ứng được và bị giữ lại trong dung dịch là SO2 và C2H4 còn khí B là CO2 không phản ứng và đi qua dung dịch.
Các PTHH:
SO2 + Br2 + 2H2O ---> 2HBr + H2SO4
C2H4 + Br2 ---> C2H4Br2

Cho hỗn hợp X vào dung dịch HCl lấy dư:
PTHH: Al2O3 + 6HCl → 2AlCl3 + 3H2O
MgO + 2HCl → MgCl2 + H2O
Fe + 2HCl → FeCl2 + H2
Dung dịch Y gồm: AlCl3, MgCl2, FeCl2, HCl dư
Khí Z là H2
Chất rắn A là Cu
Cho A tác dụng với H2SO4 đặc nóng.
PTHH: Cu + 2H2SO4(đặc, nóng) → CuSO4 + SO2 + 2H2O
Khí B là SO2
Cho B vào nước vôi trong lấy dư
PTHH: SO2 + Ca(OH)2 → CaSO3 + H2O
Kết tủa D là CaSO3
Cho dung dịch NaOH vào Y tới khi kết tủa lớn nhất thì dừng lại.
PTHH: NaOH + HCl → NaCl + H2O
3NaOH + AlCl3 → Al(OH)3 + 3NaCl
2NaOH + MgCl2 → Mg(OH)2 + 2NaCl
2NaOH + FeCl2 → Fe(OH)2 + 2NaCl
Chất rắn E là: Al(OH)3, Mg(OH)2, Fe(OH)2
Nung E trong không khí
Chất rắn G là Al2O3, MgO, Fe2O3

a) thù hình Ví dụ: O2 và O3. S2, S8 và Sn.
b) nhiệt độ nóng chảy cao. Nhà bác học Edison phải mất 10.000 thí nghiệm mới tìm ra được vật liệu W sử dụng trong dây tóc bóng đèn.
c) anot. Thu được Na ở catot (cực –) và Cl2 ở anot (cực +)
d) HF Các vật liệu thủy tinh có cấu tạo bởi SiO2, và: SiO2 + 4HF → SiF4 + 2H2O