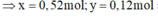Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
![]()
=> Y chứa H + dư
![]()
![]()
Bảo toàn khối lượng:
![]()
![]()
![]()
Bảo toàn nguyên tố Hidro: n N H 4 + = 0 , 04 m o l
Bảo toàn nguyên tố Nito: n F e ( N O 3 ) 2 = 0 , 08 m o l
![]()
![]()
![]()
![]()
Bảo toàn e:
![]()
![]()
![]()
Bảo toàn nguyên tố Clo:
![]()
![]()
= 298,31 (g)
Giải hệ => x = 0,52 mol; y = 0,12 mol ![]()

Đáp án B
Thêm AgNO3 vào Y → NO chứng tỏ trong Y có chứa cặp H+ và Fe2+ → anion trong Y chỉ có Cl- mà thôi.
Lượng H+ dư được tính nhanh = 4nNO = 0,18 mol → lượng phản ứng là 1,64 mol.
Sơ đồ:
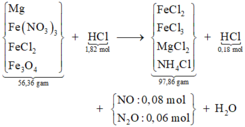
Bảo toàn khối lượng cả sơ đồ có
![]()
Theo đó, bảo toàn nguyên tố H có 0,04 mol NH4Cl và có 0,08 mol Fe(NO3)3 (theo bảo toàn N sau đó).
Tiếp tục theo bảo toàn electron mở rộng hoặc dùng bảo toàn O có ngay số mol Fe3O4 là 0,04 mol.
Gọi số mol Mg và FeCl2 trong X lần lượt là x, y mol → 24x + 127y = 27,72 gam.
Xét toàn bộ quá trình, bảo toàn electron ta có:


Đáp án B
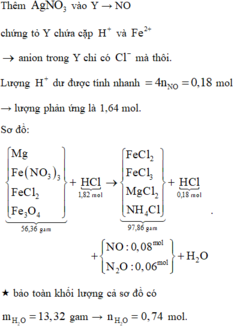
Theo đó, bảo toàn nguyên tố H có 0,04 mol NH4Cl và có 0,08 mol Fe(NO3)3 (theo bảo toàn N sau đó).
Tiếp tục theo bảo toàn electron mở rộng hoặc dùng bảo toàn O có ngay số mol Fe3O4 là 0,04 mol.
« Gọi số mol Mg và FeCl2 trong X lần lượt là x, y mol


A. 184,1 gam và 91,8 gam.
B. 84,9 gam và 91,8 gam.
C. 184,1 gam và 177,9 gam.
D. 84,9 gam và 86,1 gam.

gọi công thức ban đầu của hợp chất axit hữu cơ mà R(COOH)x
theo bài ra :2 A + xNa2CO3 ---> 2R(COONa)x + xCO2 + xH2O
khối lượng muối tăng lên là khối lượng của Na = ( 22,6 - 16) / 22 = 0,3
từ phương trinh trên = > nA = 0,3/x = 0,175 = > x = 1,7 => axit 1 chức và axit 2 chức.
gọi công thức của 2 axit là : Cn1H2n1+1COOH : a mol và Cn2H2n2(COOH)2 : b mol
viết phương trình phản ứng cháy của hỗn hợp trên , kết hợp với dữ liệu n kết tủa = nCO2 = 47,5 : 100 = 0,475 mol
ta có : \(\begin{cases}a+b=0,175\\a+2b=0,3\\\left(n1+1\right)a+\left(n2+2\right)b=0,475\end{cases}\)giải hệ ta được a = 0,05 , b = 0,125 và pt : 2n1 + 5n2=7 => n1= 1 và n2= 1 => ct : C2H4O2 Và C3H4O4

Đáp án B
Bảo toàn khối lượng:
Bảo toàn nguyên tố Hidro: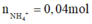
Bảo toàn nguyên tố Nito: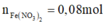
Đặt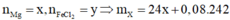
Bảo toàn e: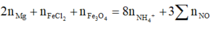
Bảo toàn nguyên tố Clo:
= 289,31 (g)
Giải hệ: