Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi số mol của axit axetic và axit fomic lần lượt là x và y (mol)
Phương trình hoá học ở dạng phân tử:
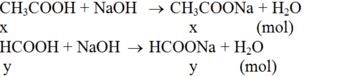
Phương trình hoá học ở dạng ion:
CH3COOH + OH- → CH3COO- + H2O
HCOOH + OH- → HCOO- + H2O

nNO = \(\dfrac{6,72}{22,4}\) = 0,300 (mol)
nHNO3nHNO3 = 1,00 x 1,5 = 1,5 (mol)
pthh: 3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O (1)
Theo (1) ta tính được nCu = 0,45 mol => mCu = 28,8 gam
nHNO3nHNO3 = 1,2 mol
nCu(NO3)2nCu(NO3)2 = 0,45 mol
mCuO = 30 gam – 28,8 gam = 1,2 gam => nCuO = 0,015 mol
CuO + 2HNO3 → Cu(NO3)2 + H2O (2)
Theo (2) ta tính được nHNO3nHNO3 là 0,030 mol, nCu(NO3)2nCu(NO3)2 là 0,015 mol
Phần tram khối lượng CuO: % mCuO = \(\dfrac{1,2}{30}\) . 100% = 4,0 %
Từ (1) và (2) ta tính được số mol HNO3 dư là 0,27 mol.
Nồng độ mol HNO3 sau phản ứng: 0,18 M
Nồng độ mol của Cu(NO3)2: 0,31 M

Phần trăm về khối lượng của CH3CHO là 44,0%, của CH3COOH LÀ 56,0%. Thể tích dung dịch NaOH là 0,46 lít.
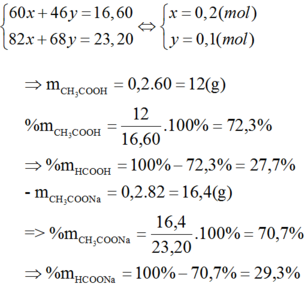
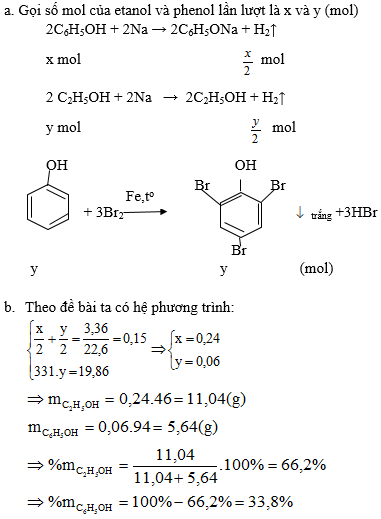
a) CH3COOH + NaOH -> CH3COONa + H2O
HCOOH + NaOH -> HCOONa + H2O
b) Khối lượng muối tăng so với khối lượng của axit : 6,60 gam.
Đặt x là số mol axit axetic ; y là số mol axit fomic
RCOOH à RCOONa : ta có ∆M = 22,0 (g/mol)
22,0(x+y) = 6,6 à x + y = 0,300 (1)
60,0x + 46,0y = 16,60 (2)
Giải hệ (1) và (2) ta được x = 0,200 ; y = 0,100
% HCOOH = 27,7% ; %CH3COOH = 72,3%.
%HCOONa = 29,3% ; %CH3COONa = 70,7%