Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

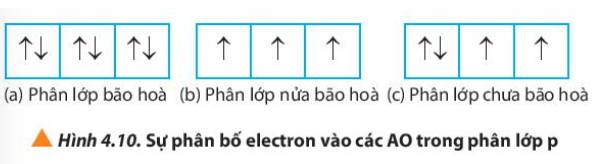
(a) Phân lớp bão hòa => Không có electron độc thân
(b) Phân lớp nửa bão hòa => Số electron độc thân = số orbital của phân lớp đó
(c) Phân lớp chưa bão hòa => số electron độc thân nhỏ hơn số orbital trong phân lớp đó
Trường hợp a) không có electron độc thân
Trường hợp b) có 3 electron độc thân
Trường hợp hợp c) có 2 electron độc thân
Nhận xét:
Phân lớp bão hòa chứa đủ số electron tối đa.
Phân lớp nửa bão hòa chứa một nửa số electron tối đa.
Phân lớp chưa bão hòa chưa đủ số electron tối đa.

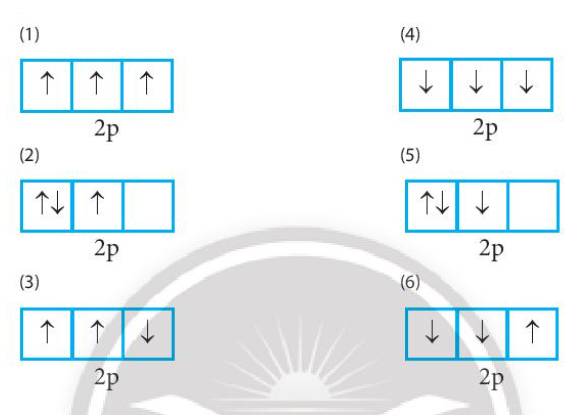
(1): đúng vì chứa tối đa electron và biểu diễn electron độc thân bằng mũi tên đi lên
(2): sai vì số electron độc thân chưa tối đa
(3): sai vì biểu diễn 1 electron độc thân bằng mũi tên đi xuống
(4): sai vì biểu diễn electron độc thân bằng mũi tên đi xuống
(5): sai vì số electron độc thân chưa tối đa, biểu diễn electron độc thân bằng mũi tên đi xuống
(6): sai vì biểu diễn 2 electron độc thân bằng mũi tên đi xuống

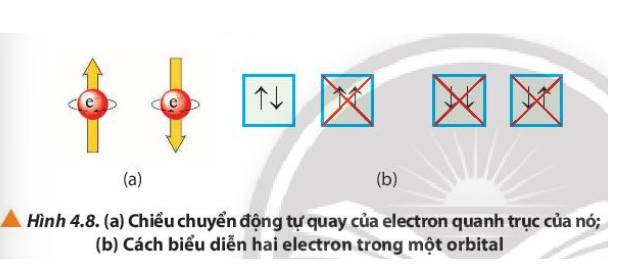
Để biểu diễn orbital nguyên tử, người ta sử dụng các ô vuông, gọi là ô lượng tử, mỗi ô lượng tử ứng với một AO, mỗi AO chứa tối đa 2 electron.
Nếu trong AO chỉ chứa một electron thì electron đó gọi là electron độc thân (kí hiệu bởi một mũi tên hướng lên ↑). Ngược lại, nếu AO chứa đủ hai electron thì các electron đó gọi là electron ghép đôi (kí hiệu bởi hai mũi tên ngược chiều nhau ↑↓).
Trong 1 orbital chỉ chứa tối đa 2 electron và có chiều tự quay ngược nhau

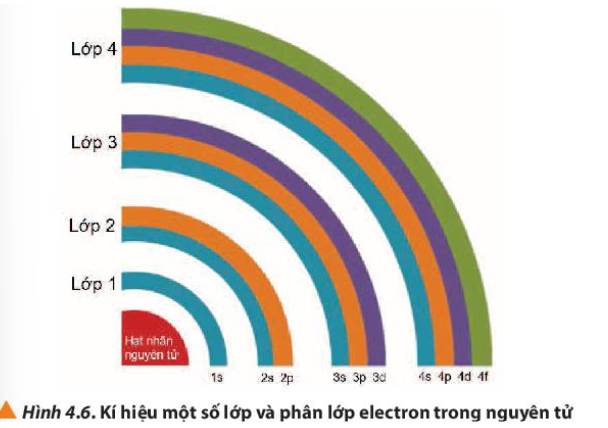
- Lớp 1 có 1 phân lớp
- Lớp 2 có 2 phân lớp
- Lớp 3 có 3 phân lớp
- Lớp 4 có 4 phân lớp
=> Từ lớp 1 đến lớp 4, số phân lớp trong mỗi lớp bằng số thứ tự của lớp đó

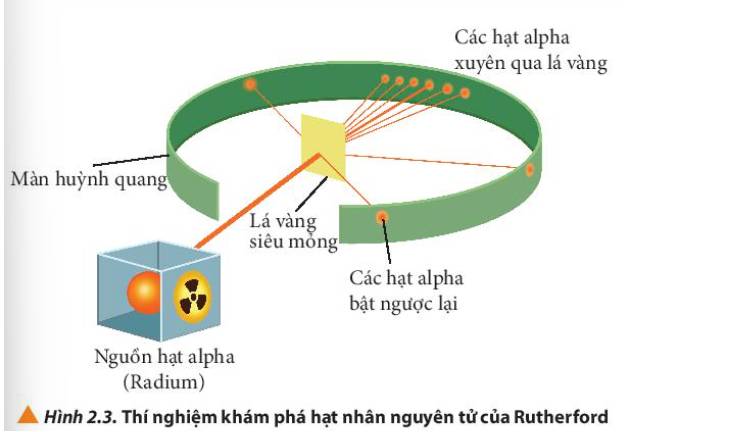
- Quan sát Hình 2.3 thấy được: hầu hết các hạt α đi thẳng, có vài hạt bị bắn theo đường gấp khúc
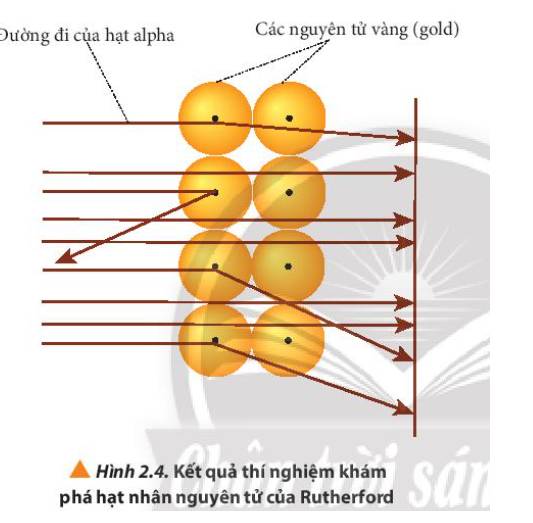
- Quan sát Hình 2.4 giải thích: các hạt α bị bắn theo đường gấp khúc là do va vào hạt nhân của nguyên tử vàng, các hạt không va vào hạt nhân thì đi thẳng
- Các hạt alpha hầu hết đều xuyên thẳng qua lá vàng, một số ít bị lệch hướng và một số rất ít bị bật ngược lại.
Giải thích: Do nguyên tử có cấu tạo rỗng, ở tâm chứa một hạt nhân mang điện tích dương có kích thước rất nhỏ so với kích thước nguyên tử nên hầu hết các hạt alpha có thể đi xuyên qua lá vàng.

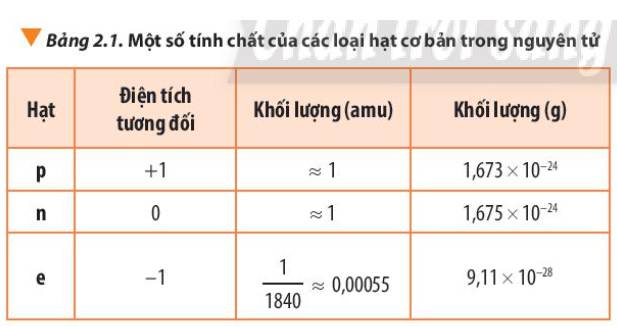
Ta có:
\(\dfrac{m_P}{m_e}=\dfrac{1}{\dfrac{1}{1840}}=1840\left(lần\right)\)
Kết quả này cho thấy khối lượng của các hạt electron không đáng kể so với khối lượng của proton và neutron, do đó khối lượng của nguyên tử gần bằng khối lượng của hạt nhân.
Tỉ lệ khối lượng 1 proton với 1 electron:
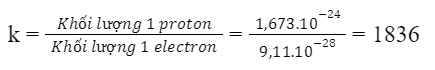
=> Khối lượng 1 electron nhỏ hơn rất nhiều so với khối lượng 1 proton
=> Có thể coi khối lượng nguyên tử = khối lượng hạt nhân do khối lượng của electron không đáng kể so với khối lượng của proton và neutron

Trong cùng một khoảng thời gian, cốc (1) được đun nóng bị mất màu, cốc (2) không được đun nóng màu chỉ nhạt hơn. Chứng tỏ nhiệt độ cao hơn đã làm phản ứng ở cốc (1) xảy ra nhanh hơn.

- Ion sodium: có 10 electron ở lớp vỏ và 11 proton trong hạt nhân
- Ion oxide: có 10 electron ở lớp vỏ và 8 proton trong hạt nhân
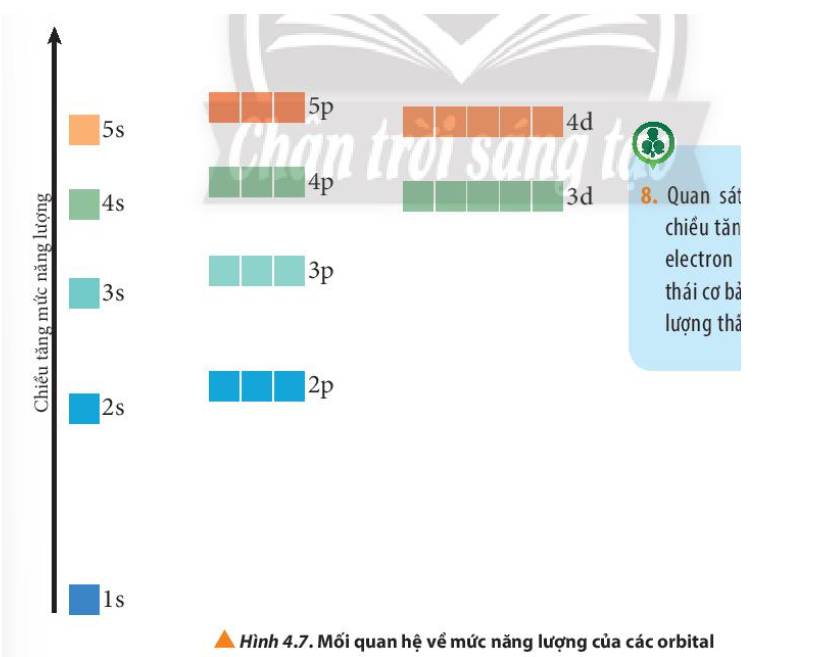


Ở trạng thái cơ bản, các electron trong nguyên tử chiếm lần lượt những orbital có mức năng lượng từ thấp đến cao: 1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p…