Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Số electron ở lớp ngoài cùng của nguyên tử Na =1
Số electron ở lớp ngoài cùng của ion Na+ =8
=>Số electron ở lớp ngoài cùng của ion Na+ nhiều hơn số electron ở lớp ngoài cùng của nguyên tử Na
Số electron ở lớp ngoài cùng của nguyên tử Cl =7
Số electron ở lớp ngoài cùng của ion Cl- =8
=>Số electron ở lớp ngoài cùng của ion Cl- nhiều hơn số electron ở lớp ngoài cùng của nguyên tử Cl
Số electron lớp ngoài cùng của `Na` bé hơn ion `Na^+`
Số electron lớp ngoài cùng của `Cl` bé hơn ion `Cl^-`

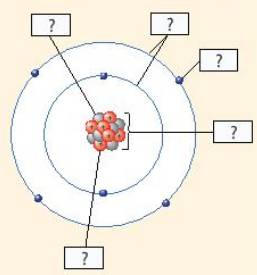
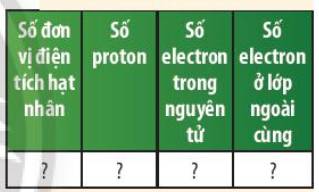
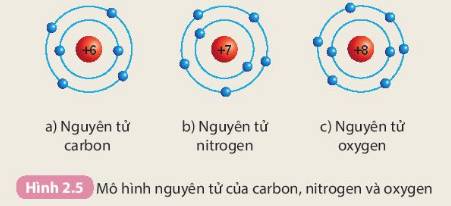
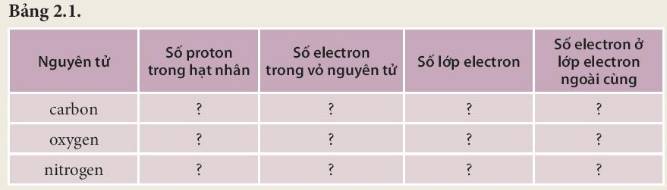
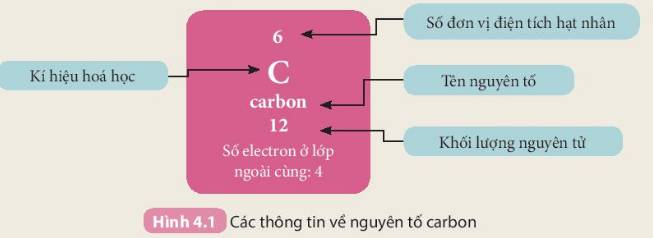
Các số điền hàng carbon lần lượt là: 6 - 6 - 2 - 4
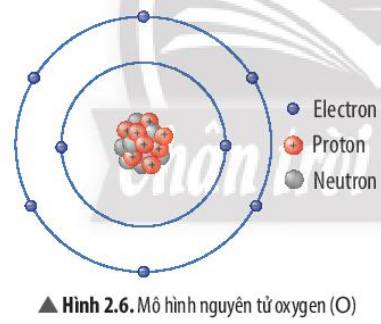
Các số điền hàng oxygen lần lượt là: 8 - 8 - 2 - 6
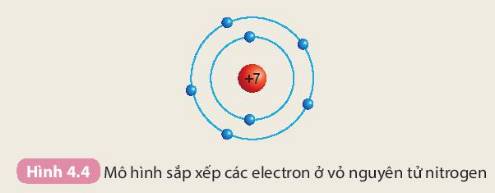
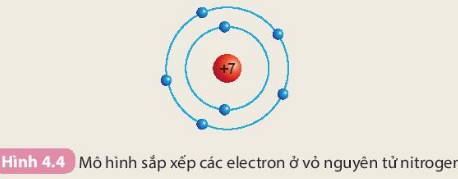
Các số điền hàng nitrogen lần lượt là: 7 - 7 - 2 - 5

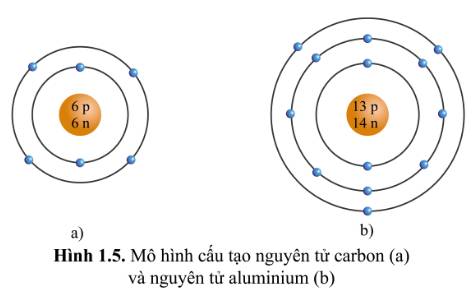
Hình 1.5
a)
-Cấu Tạo nguyên tử Carbon
+nguyên tử Carbon có hai lớp electron
+lớp thứ nhất có 2 electron
+lớp thứ hai có 4 electron
b) -Cấu Tạo nguyên tử Alumunium
+ nguyên tử Alumunium có 3 lớp electron
+ lớp thứ nhất có 2 electron
+ lớp thứ hai có 8 electron
+ lớp thứ ba có 3 electron

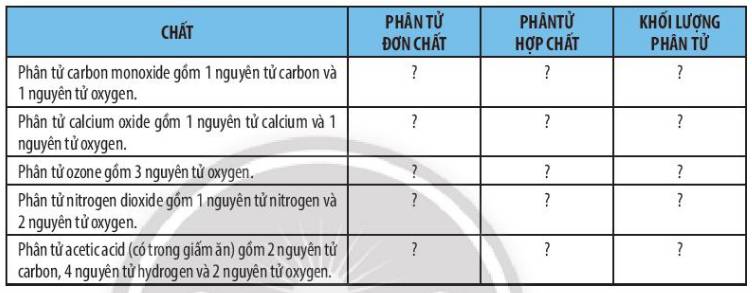
| Chất | Phân tử đơn chất | Phân tử hợp chất | Khối lượng phân tử |
| Phân tử carbon monoxide gồm 1 nguyên tử carbon và 1 nguyên tử oxygen | S | Đ | 28 |
| Phân tử calcium oxide gồm 1 nguyên tử calcium và 1 nguyên tử oxygen | S | Đ | 56 |
| Phân tử ozone gồm 3 nguyên tử oxygen | Đ | S | 48 |
| Phân tử nitrogen dioxide gồm 1 nguyên tử nitrogen và 2 nguyên tử oxygen | S | Đ | 46 |
| Phân tử acetic acid (có trong giấm ăn) gồm 2 nguyên tử carbon, 4 nguyên tử hydrogen và 2 nguyên tử oxygen | S | Đ | 60 |

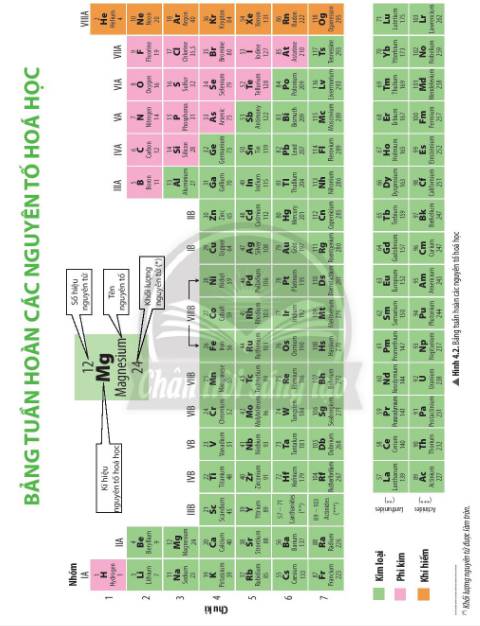
Dựa vào Hình 4.2, bảng tuần hoàn được cấu tạo gồm các ô nguyên tố được sắp xếp thành các hàng và cột.
- Các ô nguyên tố được sắp xếp lần lượt theo chiều điện tích hạt nhân tăng dần.
- Các nguyên tố hóa học có cùng số lớp electron trong nguyên tử được xếp thành một hàng.
- Các nguyên tố có số electron lớp ngoài cùng bằng nhau được xếp thành một cột.

1:
Nguyên tử Li, Na có cũng số electron ở lớp ngoài cùng
Nguyên tử F, Cl có cũng số electron ở lớp ngoài cùng
2: Số electron lớp ngoài cùng của nguyên tử các nguyên tố chính là số thứ tự nhóm của các nguyên tố

1. Nguyên tử nguyên tố H , nguyên tử nguyên tố He có 1 lớp e
Nguyên tử nguyên tố Li, Be, C, N có 2 lớp e.
2. STT chu kì của nguyên tử nguyên tố H, He (1) < STT chu kì của nguyên tử nguyên tố Li, Be, C, N (2)

- Sự thay đổi số electron ở lớp ngoài cùng trong cùng 1 hàng khi đi từ trái sang phải:
+ Hàng thứ 1: Số electron ở lớp ngoài cùng tăng dần từ 1 đến 2
+ Hàng thứ 2: Số electron ở lớp ngoài cùng tăng dần từ 1 đến 8
+ Hàng thứ 3: Số electron ở lớp ngoài cùng tăng dần từ 1 đến 8
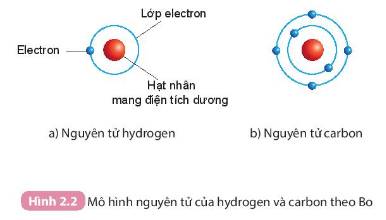

Áp dụng mô hình nguyên tử của Bo
- Nguyên tử hydrogen:
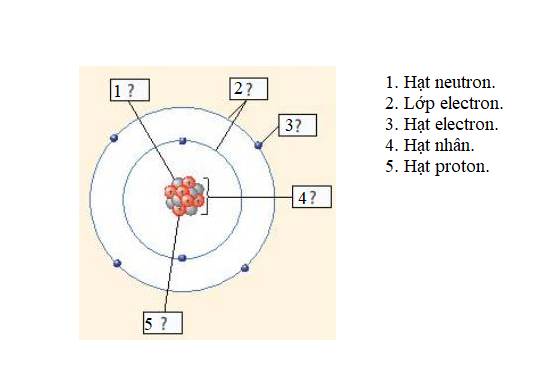
+ Hạt nhân nằm ở tâm, mang điện tích dương
+ Có 1 electron (mang điện tích âm) nằm ở lớp thứ nhất, quay xung quanh hạt nhân
- Nguyên tử carbon:
+ Hạt nhân nằm ở tâm, mang điện tích dương
+ Có 2 lớp electron và 6 electron phân bố ở các lớp: lớp thứ nhất có 2 electron, lớp thứ 2 có 4 electron. Các electron quay xung quanh hạt nhân.