Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Na + H2O ---> NaOH + 1/2H2;
x x x/2
NaOH + HCl ---> NaCl + H2O;
0,1 0,1
Dung dịch X gồm NaCl và NaOH dư;
Số mol NaOH dư = x - 0,1 mol; lượng NaOH dư được trung hòa bằng 0,02 mol HCl nên: x - 0,1 = 0,02 hay x = 0,12 mol.
Vậy: m = 23.0,12 = 2,76 g; V = 0,06.22,4 = 1,344 lít.

a, \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: M + 2H2O → M(OH)2 + H2
Mol: 0,1 0,1 0,1
\(\Rightarrow M_M=\dfrac{4}{0,1}=40\left(g/mol\right)\)
⇒ M là canxi (Ca)
\(C\%_{ddCa\left(OH\right)_2}=\dfrac{0,1.74.100\%}{500}=1,48\%\)
b) \(m_{Ca\left(OH\right)_2}=200.1,48=2,96\left(g\right)\Rightarrow n_{Ca\left(OH\right)_2}=\dfrac{2,96}{74}=0,04\left(mol\right)\)
PTHH: Ca(OH)2 + 2HCl → CaCl2 + 2H2O
Mol: 0,04 0,08
\(V_{ddHCl}=\dfrac{0,08}{2}=0,04\left(l\right)=40\left(ml\right)\)

a) Ta có \(m_{muôi}=m_{KL}+m_{Cl^-}\\ \Leftrightarrow m_{Cl^-}=m_{muôi}-m_{KL}=14,25-3,6=10,65g\\ \Rightarrow n_{Cl^-}=\dfrac{10,65}{35,5}=0,3mol\)
Theo bảo toàn nguyên tố Cl: \(n_{HCl}=n_{Cl^-}=0,3mol\)
Theo bảo toàn nguyên tố H: \(n_{H_2}=\dfrac{1}{2}\cdot n_{HCl}=\dfrac{1}{2}\cdot0,3=0,15mol\\ \Rightarrow V=0,15\cdot22,4=3,36l\)
Ta có PTHH: \(M+2HCl\rightarrow MCl_2+H_2\uparrow\)
----------------0,15-------------------------0,15---(mol)
\(\Rightarrow M=\dfrac{3,6}{0,15}=24\)(g/mol) => M là Magie (Mg)
b) \(n_{CuO}=\dfrac{16}{80}=0,2mol\)
Ta có quá trình phản ứng:
\(CuO+H_2\rightarrow Cu+H_2O\)
-0,15---0,15-----0,15----------(mol)
\(\Rightarrow a=m_{CuO\left(dư\right)}+m_{Cu}=\left(16-0,15\cdot80\right)+64\cdot0,15=13,6g\)

1. Gọi hóa trị kim loại là n và số mol là a mol. Ta có: Ma = 7.
2M + 2nHCl \(\rightarrow\) 2MCln + nH2\(\uparrow\)
Khối lượng dung dịch sau phản ứng tăng 6,75 gam nên:
7 - 0,5na2 = 6,75 hay na = 0,25.
Lập tỉ lệ: \(\frac{M}{n}=\frac{Ma}{na}=28\)Vậy M= 28n
Ta lập bảng sau:
|
N |
1 |
2 |
3 |
|
M |
28 (loại) |
56 (nhận) |
84 (loại) |
Vậy kim loại M là Fe.
2. Gọi số mol: Fe = b và FexOy = c mol. Ta có 56b + (56x + 16y)c = 6,28.
Fe + 4HNO3 \(\rightarrow\) Fe(NO3)3 + NO \(\uparrow\) + 2H2O
3FexOy + (12x - 2y)HNO3 \(\rightarrow\)3xFe(NO3)3 + (3x - 2y)NO\(\uparrow\)+ (6x - y)H2O
Ta có: 4b + \(\frac{\left(12x-2y\right)c}{3}=0,34\)và b +\(\frac{\left(3x-2y\right)c}{3}=0,055\)
Từ đây tính được: b = 0,05 mol; xc = 0,045 mol và yc = 0,06 mol.
Lập tỉ lệ: \(\frac{x}{y}=\frac{xc}{yc}=\frac{3}{4}\)Vậy công thức oxit là Fe3O4.
Số oxi hóa của sắt trong oxit là\(+\frac{8}{3}\).hóa trị của sắt là II và III (FeO.Fe2O3).
Nghĩ là v k bt đúng k nhờ thây xem qua nha

a)
M + 2HCl → MCl2 + H2
nH2 = \(\dfrac{3,584}{22,4}=\)0,16 mol => nM = 0,16 mol
<=> MM = \(\dfrac{3,84}{0,16}\)= 24 (g/mol) => M là magie (Mg).
b) 8Mg + 20HNO3 → 8Mg(NO3) + 2NO + N2 + 10H2O
Từ tỉ lệ phương trình , gọi số mol N2 là x => nNO = 2x mol
=> V(NO + N2) =3x.22,4 =1,344
<=> x =0,02
=> VN2 = 0,02.22,4 =0,448 lít , VNO= 0,04.22,4 = 0,896 lít

41.
Gọi n là hóa trị của M
2M + nH2SO4 \(\rightarrow\)M2(SO4)n + nH2
M + nHCl \(\rightarrow\) MCln +\(\frac{n}{2H2}\)
nH2=\(\frac{8,064}{22,4}\)=0,36 mol
Ta óc : nM=\(\frac{nH2}{\frac{n}{2}}\)=\(\frac{0,72}{n}\) \(\rightarrow\) M M=\(\frac{6,48}{\frac{0,72}{n}}\)=9n thỏa mãn n=3
\(\rightarrow\) M M=27 \(\rightarrow\)Al
44.
Gọi n là hóa trị của M
M + nHCl \(\rightarrow\)MCln + \(\frac{n}{2}\) H2
BTKL: m dung dịch tăng lên=mM -mH2=m-mH2=0,95m
\(\rightarrow\)mH2=0,05m \(\rightarrow\) nH2=0,025m
Ta có:nM=\(\frac{nH2}{\frac{n}{2}}\)=\(\frac{0,025m}{\frac{n}{2}}\)=\(\frac{0,05m}{n}\)
\(\rightarrow\)M M=\(\frac{m}{\frac{0,05m}{n}}\)=20n thỏa mãn n=2
\(\rightarrow\) M M=40\(\rightarrow\) Ca
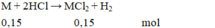



\(2M+3Cl_2\rightarrow2MCl_3\\ n_{Cl_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\\ \Rightarrow n_M=\dfrac{2.0,075}{3}=0,05\left(mol\right)\\ M+2HCl\rightarrow MCl_2+H_2\\ n_{HCl}=2n_M=2.0,05=0,1\left(mol\right)\\ \Rightarrow V=V_{ddHCl}=\dfrac{0,1}{2}=0,05\left(l\right)=50\left(ml\right)\)