Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đề 15:
1) Theo đề bài , ta có:
NTK(Y)= 2.NTK(Ca)= 2.40=80 (đvC)
=> Nguyên tố Y là brom, KHHH là Br.
2) - Đơn chất là chất do 1nguyên tố tạo thành.
VD: O3; Br2 ; Cl2;......
- Hợp chất là những chất do 2 hay nhiều nguyên tố hóa học trở lên tạo thành.
VD: NaCl, KMnO4, CuSO4, H2O;....
3) Khôi lượng mol? tự trả lời đi !
a) Khối lượng mol của phân tử gồm 2C và 4H
Có nghĩa là khối lượng mol của C2H4
\(M_{C_2H_4}\)= 2.12+4.1=28 (g/mol)
\(M_{H_2S}\)=2.1+32=34(g/mol)

a)C+O2→CO2.
b)Áp dụng định luật bảo toàn khối lượng:
\(m_C+m_{O_2}\xrightarrow[]{}m_{CO_2}\)
\(m_{CO_2}=9+24\)
\(m_{CO_2}=33\left(kg\right)\)

Zn+2HCl=>ZnCl2+H2
nZn=0,05 mol=nH2
H2+CuO=>Cu+H2O
=>nCu=0,05mol =>mCu=0,05.64=3,2g
Trong pứ trên Zn và H2 là chất khử
HCl và CuO là chất oxh
2. mNaCl thu đc=150.3,5%=5,25g
Cho 13gam Zn tác dụng với dung dịch HCL vừa đủ Dẫn toàn bộ khí thu được qua CuO nung nóng
a, Viết PT hoá học của CÁC phản ứng
b, Tính khối lượng Cu thu được sau phản ứng

Bài 6: Lấy ví dụ 3 hiện tượng vật lý, 3 hiện tượng hóa học?
Vật lí:
+ Làm chảy lỏng thủy tinh để tạo thành hình lọ hoa
+ Hòa tan đường vào nước được dung dịch nước đường
+ Khi đun nước, nước sôi và bay hơi
Hóa học:
+ Khi nung đá vôi chuyển thành vôi sống và khí cacbon
+ Sắt để lâu trong không khí bị dỉ
+ Cho Zn vào dung dịch HCl thu được muối kẽm clorua và khí hidro thoát ra.
Bài 7: Cho đinh sắt vào dung dịch axit clohiđric ta thấy có bọt khí sủi lên, đinh sắt tan dần
a. Cho biết dấu hiệu để nhận biết có phản ứng hóa học xảy ra?
------> có bọt khí sủi lên và đinh sắt tan
b. Viết phương trính bằng chữ của phản ứng, biết sản phẩm tạo thành là: Sắt(II) clorua và
hiđro
Sắt + Axit clohidric ----> Sắt (II) clorua+hidro
Bài 8: Khi đốt than cháy, có xảy ra phản ứng hóa học: C + O 2 ---> CO2
a. Cho biết khối lượng than bằng 9 kg, khối lượng oxi tác dụng là 24 kg. Hãy tính khối
lượng khí cacbonic tạo thành.
Áp dụng định luật bảo toàn khối lượng:
\(m_C+m_{O_2}=m_{CO_2}\)
\(\Rightarrow m_{CO_2}=9+24=33g\)
b. Nếu khối lượng của cacbon tác dụng bằng 6kg, khối lượng khí cacbonic thu được là 22
kg thì khối lượng khí oxi cần cho phản ứng là bao nhiêu?
Áp dụng định luật bảo toàn khối lượng:
\(m_C+m_{O_2}=m_{CO_2}\)
\(\Rightarrow m_{O_2}=22-6=16g\)
Góp ý: Nếu bổ sung thì cmt dưới câu tl nha chứ đừng có tl tiếp :v

Zn+2HCl->Zncl2+H2
0,4----0,8----0,4----0,4
n Zn=0,4 mol
VH2=0,4.22,4=8,96l
m ZnCl2=0,4.136=54,4g
2H2+O2-to>2H2O
0,4------0,2----0,4
n O2=0,2 mol
=>pứ hết
=>m H2O=0,4.18=7,2g
a.b.\(n_{Zn}=\dfrac{26}{65}=0,4mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,4 0,4 0,4 ( mol )
\(m_{ZnCl_2}=0,4.136=54,4g\)
\(V_{H_2}=0,4.22,4=8,96l\)
c.\(n_{O_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\)
0,4 = 0,2 ( mol )
0,4 0,2 0,4 ( mol )
\(m_{H_2O}=0,4.18=7,2g\)
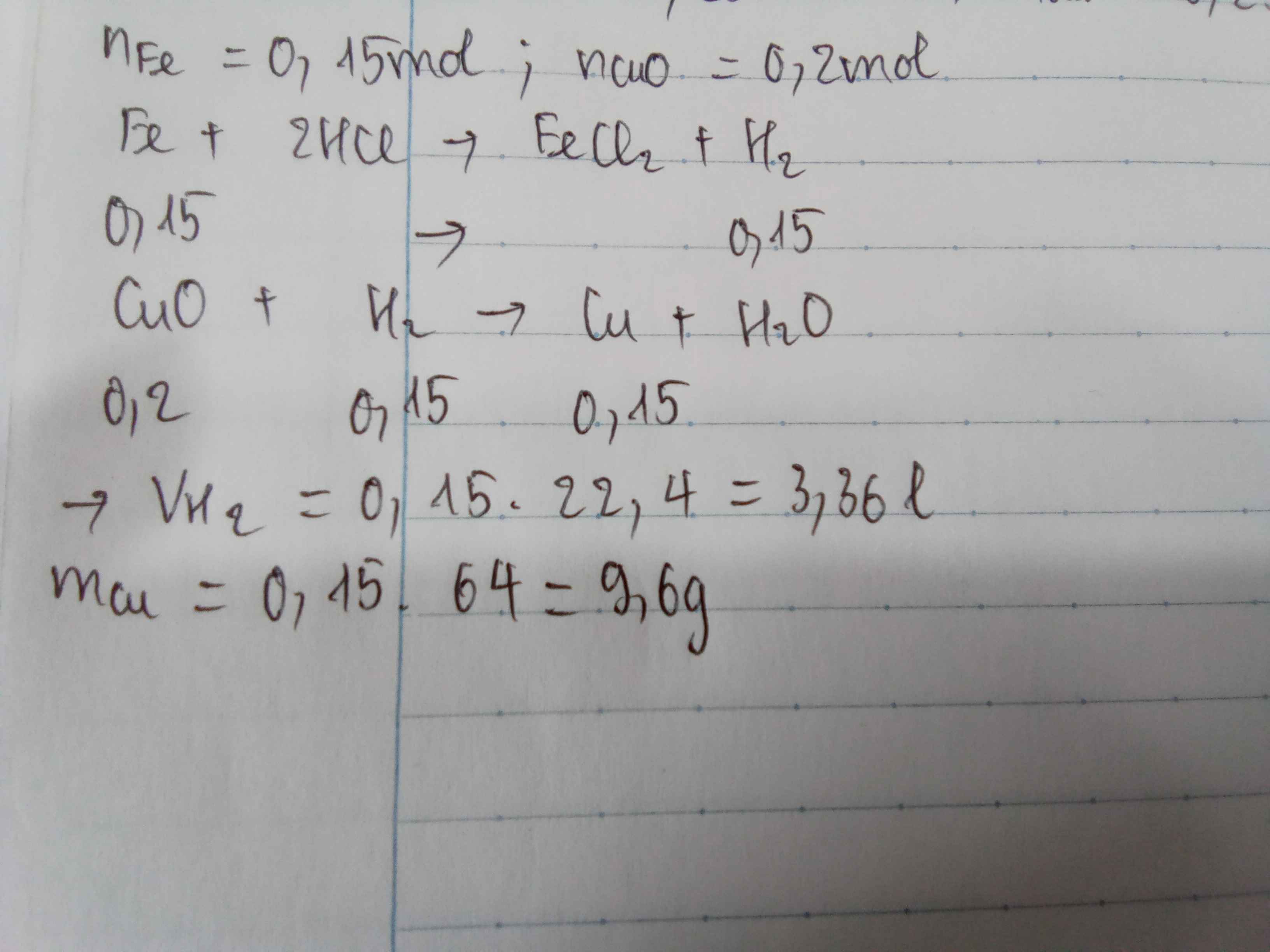

1) \(Fe+2HCl->FeCl_2+H_2\)
\(n_{Fe}=\frac{8,4}{56}=0,15mol\)
\(n_{H_2}=n_{Fe}=0,15mol\)
\(V_{H_2}=0,15.22,4=3,36l\)
-\(CuO+H_2->Cu+H_2O\)
\(n_{CuO}=\frac{16}{80}=0,2mol\)
Vì: \(\frac{0,2}{1}>\frac{0,15}{1}\)=>CuO dư, H2 hết
\(n_{Cu}=n_{H_2}=0,15mol\)
\(m_{Cu}=0,15.64=9,6g\)
2) C+O2->CO2
b) \(n_C=\frac{9}{12}=0,75mol\)
\(n_{O_2}=\frac{24}{32}=0,75mol\)
=> 2 chất phản ứng hết.
\(n_{CO_2}=n_C=0,75mol\)
\(m_{CO_2}=0,75.44=16,8kg\)
b) \(n_C=\frac{6}{12}=0,5mol\)
\(n_{O_2}=n_C=0,5mol\)
\(m_{O_2}=0,5.32=16kg\)