Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt kim loại là M, oxit là MO
Giả sử có 1 mol MO phản ứng, 1 mol H2SO4 phản ứng:
MO + H2SO4 -> MSO4 + H2O
C% = mct / mdd . 100%
10% = 1 . 98 / mdd . 100%
-> mDd H2SO4 = 980 g
Theo định luật bảo toàn khối lượng ta có:
Mdd = mMO + mddH2SO4 = (M + 16) + 980
= M + 996
C%muối = m chất tan muối/ m dd muối . 100%
15.17% = (M + 96) / (M + 996) * 100%
M = 64.95 g
M là Zn
Công thức oxit ZnO

Chọn C
Gọi công thức của oxit hóa trị II là RO
Đặt mol RO = 1 (mol)
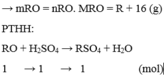
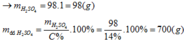
![]()
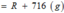
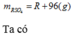

Vậy công thức của oxit kim loại là MgO

Gọi CTHH oxit kim loại là \(RO\)
Giả sử có 1mol oxit pứ
\(RO+H_2SO_4\rightarrow RSO_4+H_2O\)
\(1-\rightarrow1---\rightarrow1\)
\(m_{ddH_2SO_4}=\dfrac{1.98}{4,9}\cdot100=2000\left(g\right)\\ m_{ddRSO_4}=1\left(R+16\right)+2000=2016+R\left(g\right)\\ C_{\%RSO_4}=\dfrac{1\left(R+96\right)}{2016+R}\cdot100=5,88\%\\ \Rightarrow R\approx24\left(g/mol\right)\)
Vậy R là Mg

CT oxit : MO
Đặt số mol oxit phản ứng là 1 mol
\(MO+H_2SO_4\rightarrow MSO_4+H_2O\)
\(m_{ddH_2SO_4}=\dfrac{1.98}{15,8\%}=620,25\left(g\right)\)
\(m_{ddsaupu}=620,25+M+16=M+636,25\left(g\right)\)
Ta có : \(C\%_{MSO_4}=\dfrac{M+96}{M+636,25}.100=22,959\)
=> M=65 (Zn)
=> Oxit kim loại : ZnO (Kẽm oxit)

a/ CT oxit: $CuO$
b/ Vậy CT X: $CuSO_4.5H_2O$
Giải thích các bước giải:
Gọi công thức oxit là: $MO$
Số mol oxit là a mol
$MO+H_2SO_4\to MSO_4+H_2O$
Theo PTHH
$n_{H_2SO_4}=n_{MSO_4}=n_{MO}=a\ mol$
$⇒m_{dd\ H_2SO_4}=\dfrac{98a.100}{24,5}=400a$
$⇒m_{dd\ A}=a.(M+16)+400a = aM+416a$
$m_{MSO_4}=a.(M+96)$
Do nồng độ muối là 33,33% nên:
$\dfrac{a.(M+96)}{aM+416a}.100\%=33,33\\⇒M=64$
Vậy M là Cu, công thức oxit: $CuO$
b.
Trong 60 gam dung dịch muối A có:
$m_{CuSO_4}=\dfrac{60.33,33}{100}=20g$
Gọi công thức tinh thể tách ra là: $CuSO_4.nH_2O$
Khối lượng dung dịch còn lại là:
$60-15,625=44,375g ⇒ m_{CuSO_4\ trong\ dd}=\dfrac{44,375.22,54}{100}=10g$
$⇒m_{CuSO_4\ trong\ tinh\ thể}=20-10=10g$
$⇒n_{tinh\ thể}=n_{CuSO_4}=0,0625\ mol$
$⇒M_{tinh\ thể}=15,625:0,0625=250⇒n=5$
Vậy CT X: $CuSO_4.5H_2O$

a) Gọi công thức oxit là: MO
Số mol oxit là a mol
MO+H2SO4→MSO4+H2O
Theo PTHH
nH2SO4=nMSO4=nMO=a mol
⇒mdd H2SO4=98a.100/24,5=400a
⇒mdd A=a.(M+16)+400a=aM+416a
mMSO4=a.(M+96)
Do nồng độ muối là 33,33% nên:
a.(M+96)/aM+416a.100%=33,33⇒M=64
Vậy M là Cu, công thức oxit: CuO

a)Giả sử có 1 mol MO phản ứng
\(MO+2HCl\rightarrow MCl_2+H_2O\)
1----------->2----------->1----------->1
=> \(m_{ddHCl}=\dfrac{2.36,5}{10\%}=730\left(g\right)\)
\(m_{ddsaupu}=\left(M+16\right)+730=M+746\left(g\right)\)
=> \(C\%_{MCl_2}=\dfrac{M+71}{M+746}.100=12,34\)
=> M=24 (Mg)
b) Giả sử có 1 mol M2On phản ứng
\(M_2O_n+2nHCl\rightarrow2MCl_n+nH_2O\)
1---------------->2n-------------->2----------->n
=> \(m_{ddHCl}=\dfrac{2n.36,5}{10\%}=730n\left(g\right)\)
\(m_{ddsaupu}=\left(2M+16n\right)+730n=2M+746n\left(g\right)\)
=> \(C\%_{MCl_2}=\dfrac{2\left(M+35,5n\right)}{2M+746n}.100=12,34\)
Chạy nghiệm n=1,2,3
n=1 => M=12 (loại)
n=2 => M=24 (Mg)
n=3 => M=36 (loại)

CTHH cần tìm : $R_2O_3$
Coi $n_{H_2SO_4} = 3(mol)$
R2O3 + 3H2SO4 → R2(SO4)3 + 3H2O
1..............3..................1..................................(mol)
Ta có :
$m_{dd\ H_2SO_4} = \dfrac{3.98}{10\%} = 2940(gam)$
$m_{dd\ sau\ pư} = 2R + 16.3 + 2940 = 2R + 2988(gam)$
Suy ra :
$C\% = \dfrac{2R + 96.3}{2R + 2988}.100\% = 12,9\%$
$\Rightarrow R = 56(Fe)$
Vậy oxit là $Fe_2O_3$

\(MO+H_2SO_4->MSO_4+H_2O\\ m_{ddH_2SO_4}=100g\left(tự.chọn\right)\\ C\%_{sau}=\dfrac{11,8}{100}=\dfrac{\dfrac{100.0,1}{98}\left(M+96\right)}{\dfrac{100.0,1}{98}\left(M+16\right)+100}\\ M=24\left(Mg\right)\\ CT:MgO\)
Đặt kim loại là M, oxit là MO
Giả sử có 1 mol MO phản ứng, 1 mol H2SO4 phản ứng:
MO + H2SO4 -> MSO4 + H2O
C% = mct / mdd . 100%
10% = 1 . 98 / mdd . 100%
-> mDd H2SO4 = 980 g
Theo định luật bảo toàn khối lượng ta có:
Mdd = mMO + mddH2SO4 = (M + 16) + 980
= M + 996
C%muối = m chất tan muối/ m dd muối . 100%
15.17% = (M + 96) / (M + 996) * 100%
M = 64.95 g
M là Zn
Công thức oxit ZnO
Oh, thanks!