Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Có thể xem công thức Fe3O4 là FeO.Fe2O3 nên hỗn hợp X có thể được xem như gồm FeO và Fe2O3.
Gọi a là số mol FeO, b là số mol Fe2O3 của 0,5 m gam X.
FeO + H2SO4 --->FeSO4 + H2O
Fe2O3 + 3H2SO4 ---> Fe2(SO4)3 + 3H2O
từ khối lượng muối khan ở phần 1, ta có phương trình
152a + 400b = 31,6 gam (1)
Phần 2 khi cho Cl2 vào thì xảy ra pu:
FeSO4 + 0,5 Cl2 ---> 1/3 Fe2(SO4)3 + 1/3 FeCl3
--> khối lượng muối ở phần 2 = 400a/3 + 162,5a/3 + 400b = 33,375 gam
--> 562a + 1200b = 100,125 (2)
Từ (1) và (2) suy ra :
a =0,0502358 mol
b = 0,0599153 mol
--> Khối lượng hỗn hợp X = 2 x (72 x 0,0502358 + 160 x 0,0599153) = 26,712448 gam
a.
Phương trình
+ Khi hòa A bằng axit H2SO4 loãng
FeO + H2SO4 \(\rightarrow\) FeSO4 + H2O (1)
Fe2O3 + 3H2SO4 \(\rightarrow\) Fe2(SO4)3 + 3H2O (2)
Fe3O4 + 4H2SO4 \(\rightarrow\) Fe2(SO4)3 + FeSO4+ 3H2O (3)
Sau phản ứng dung dịch chỉ có 2 muối (x+z)mol FeSO4 và (y+z) mol Fe2(SO4)3
+ Khi sục khí Cl2 vào dung dịch sau phản ứng chỉ có FeSO4 phản ứng
6FeSO4 + 3Cl2 \(\rightarrow\) 2FeCl3 + 2Fe2(SO4)3 (4)
b.
Theo bài ta có hệ phương trình
\(\begin{cases}72x+160y+232z=m\text{/}2\\152\left(x+z\right)+400\left(y+z\right)=31,6\\187,5\left(x+z\right)+400\left(y+z\right)=33,375\end{cases}\)\(\begin{matrix}\left(I\right)\\\left(II\right)\\\left(III\right)\end{matrix}\)
Từ II, III ta có x+z= 0,05; y+z=0,06
Mặt khác từ I ta có m=2.[ 72(x+z) + 160(y+z)]=26,4 gam
Vậy m= 26,4g
\(C_{FeSO_4}\)=0,2M; \(C_{Fe_2\left(SO_4\right)_3}\)=0,24M

X + O2 → Y
Bảo toàn khối lượng có mO2 = 0,48 g → nO2 = 0,015 mol
Quy đổi Y thành kim loại và oxi
Ta có 4H+ + 4e + NO3- → 2H2O + NO
2H+ + O2- → H2O
→ nH+ = 4nNO + 2nO =4.0,03 + 2.0,03= 0,18 mol
Bảo toàn nguyên tố H thì nHNO3 = 0,18 mol
bài2
Ta có: nCO= 0,8 mol; nSO2= 0,9 mol
MxOy + yCO → xM + yCO2 (1)
Ta thấy đáp án M là Fe hoặc Cr nên M có số oxi hóa cao nhất là +3
2M + 6H2SO4 → M2(SO4)3+ 3SO2+ 6H2O (2)
Theo PT (2): nM= 2/3.nSO2= 0,6 mol
Theo PT (1):
x/y=nM/nCO=0,6/0,8=3/4 => Oxit là Fe3O4

1) Ptpư:
2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2
Fe + 2HCl \(\rightarrow\) FeCl2 + H2
Cu + HCl \(\rightarrow\) không phản ứng
=> 0,6 gam chất rắn còn lại chính là Cu:
Gọi x, y lần lượt là số mol Al, Fe
Ta có:
3x + 2y = 2.0,06 = 0,12
27x + 56 y = 2,25 – 0,6 = 1,65
=> x = 0,03 (mol) ; y = 0,015 (mol)
=> \(\%Cu=\frac{0,6}{2,25}.100\%=26,67\%\); \(\%Fe=\frac{56.0,015}{2,25}.100\%=37,33\%\); %Al = 36%
2) \(n_{SO_2}=\frac{1,344}{22,4}=0,06mol\); m (dd KOH) = 13,95.1,147 = 16 (gam)
=> mKOH = 0,28.16 = 4,48 (gam)=> nKOH = 0,08 (mol)=> \(1<\)\(\frac{n_{KOH}}{n_{SO_2}}<2\)
=> tạo ra hỗn hợp 2 muối: KHSO3: 0,04 (mol) và K2SO3: 0,02 (mol)
Khối lượng dung dịch sau pu = 16 + 0,06.64 = 19,84 gam
=> \(C\%\left(KHSO_3\right)=\frac{0,04.120}{19,84}.100\%\)\(=24,19\%\)
\(C\%\left(K_2SO_3\right)=\frac{0,02.158}{19,84}.100\%\)\(=15,93\%\)

Theo đề bài ta có bột S dư nên Fe, Zn tác dụng hết với S.
a)Phương trình hóa học của phản ứng.
Zn + S -> ZnS Fe + S -> FeS
x mol x mol y mol y mol
ZnSO4 + H2SO4 -> ZnSO4 + H2S
x mol x mol
FeSO4 + H2SO4 -> FeSO4 + H2S
x mol y mol
Ta có hệ phương trình :
Giải hệ phương trình => x = 0,04 (mol), y = 0,02 (mol).
Vậy mZn = 0,04.65 = 2,6g
mFe = 0,02.56 = 1,12g.
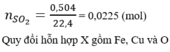
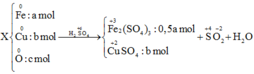
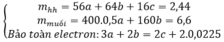
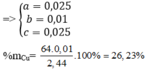






A) Zn + 2HCl ------> ZnCl2 + H2 (1)
Mg + 2HCl ------> MgCl2 + H2 (2)
Gọi x, y lần lượt là số mol của Zn, Mg
Theo đề bài ta có : \(\left\{{}\begin{matrix}65x+24y=11,3\\x+y=\frac{6,72}{22,4}=0,3\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\Rightarrow\%m_{Zn}=\frac{0,1.65}{11,3}.100=57,52\%\)
\(\Rightarrow\%m_{Mg}=100-57,52=42,48\%\)
B) Theo PT (1) : n ZnCl2 = n Zn =0,1 (mol)
\(\Rightarrow m_{ZnCl_2}=0,1.136=13,6\left(g\right)\) Theo PT (2) : n MgCl2 = n Mg =0,2 (mol) \(\Rightarrow m_{MgCl_2}=0,1.95=9,5\left(g\right)\) C)11,3 g hh X gồm 0,1 mol Zn ; 0,2 mol Mg => 5,65g hh X chứa 0,05 mol Zn ; 0,1 mol Mg \(n_T=\frac{3,36}{22,4}=0,15\left(mol\right)\) Quá trình nhường e : Zn-------> Zn 2+ + 2e 0,05........................0,1 Mg-------> Mg 2+ + 2e 0,1............................0,2 Quá trình nhận e : S+6 + ne -------> S+(6-n) ............0,15n..................0,15...... Bảo toàn e : 0,1 + 0,2 = 0,15n => n =2 => Quá trình nhận e : S+6 + 2e -------> S+4 => T là SO2 Khi cho SO2 vào dd NaOH dư => Tạo muối trung hòa SO2 + 2NaOH ------> Na2SO3 + H2O 0,15...............................0,15 => m Na2SO3 = 0,15 . 126 = 18,9 (g)