Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Zn+2HCl---->ZnCl2+H2
b) n H2=4,48/22,4=0,2(mol)
n Zn=n ZnCl2=n H2=0,2(mol)
m Zn=0,2.65=13(g)
m Zncl2=0,2.136=27,2(g)
c) CuO+H2---->Cu+H2O
n CuO=24/80=0,3(mol)
--->CuO dư
n CuO=n H2=0,2(mol)
n CuO dư=0,3-0,2=0,1(g)
m CuO dư=0,1.80=8(g)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2____________0,2____0,2
\(n_{H2}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
\(m_{Zn}=0,2.65=13\left(g\right)\)
\(m_{ZnCl2}=0,2.\left(65+71\right)=27,2\left(g\right)\)
\(PTHH:CuO+H_2\rightarrow Cu+H_2O\)
Ban đầu :0,3____0,2____________
Phứng: 0,2______0,2__________
Sau phứng :0,1___0___________
\(n_{CuO}=\frac{24}{80}=0,3\left(mol\right)\)
Vậy CuO dư
\(m_{CuO_{du}}=0,1.80=8\left(g\right)\)

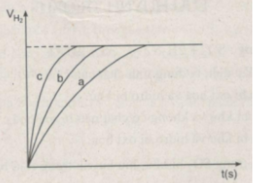
Thể tích khí hiđro :
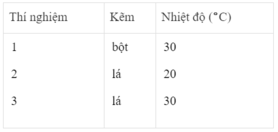
Sau các thí nghiệm, kẽm còn dư. Như vậy, thể tích khí hiđro được sinh ra phụ thuộc vào lượng H 2 SO 4 tham gia phản ứng
n H 2 = n H 2 SO 4 = 2.50/1000 = 0,1 mol
Thể tích khí hiđro ở điều kiện phòng là :
V H 2 = 0,1 x 24 = 2,4l = 2400 cm 3
Ta ghi số 2400 cm 3 trên trục y, nơi giao điểm giữa trục y và đường ngang của 3 đường cong kéo dài (nét chấm trên đồ thị).

Zn + 2HCl => ZnCl2 + H2
Na2CO3 + 2HCl=> 2NaCl + H2O + CO2
MY = 0,5875.32 = 18,8
áp dụng sơ đồ đường chéo ta đc nH2 : nCO2 = 3:2
mà nH2 = nZn ; nCO2 = nNa2CO3
=> nZn = 3/2 nCO2
ta có \(65.\frac{3}{2}x+106x=4,07\left(g\right)\) => x= 0,02 mol => nZn =0,03
a. => % na2CO3 = \(\frac{0,02.106}{4,07}.100\%=52,088\%\)
=> % Zn = 47,912%
b. nHCl pư = 2 .nZn + 2. nNa2CO3 = 2.0,03+ 2.0,02 = 0,1
=> mHCl pư = 0,1.36,5 = 3,65 (g)
=> m HCl dùng = 3,65.120% = 4,38 (g)
=> mdd HCl = \(\frac{4,38.100}{25}=17,52\)
=> mdd = 4,07 + 17,52 - 0,03.2-0,02.44 = 20,65(g)
mHCl dư = 4,38 - 3,65 = 0,73(g)
C% HCl dư = \(\frac{0,73}{20,65}.100\%\) = 3,535%

\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,2__________0,2_______0,2
\(n_{Fe}=\frac{11,2}{56}=0,2\left(mol\right)\)
\(V_{H2}=0,2.22,4=4,48\left(l\right)\)
\(m_{FeCl2}=0,2.\left(56+71\right)=25,4\left(g\right)\)
\(CuO+H_2\rightarrow Cu+H_2O\)
______0,2____0,2______
\(m_{Cu}=0,2.64=12,8\left(g\right)\)

a. PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
\(n_{H_2}=\frac{6,72}{22,4}=0,3mol\)
Theo phương trình \(n_{Al}=n_{AlCl_3}=\frac{2}{3}n_{H_2}=0,2mol\)
\(\rightarrow m_{Al}=0,2.27=5,4g\)
\(\rightarrow m=5,4\)
b. \(m_{\text{muối}}=m_{AlCl_3}=0,2.133,5=26,7g\)
a)PTHH\(2AL+6HCL\rightarrow2ALCL_3+3H_2\uparrow\)
\(n_{H_2}=\frac{6,72}{22,4}=0,3mol\)
Theo phương trình:\(n_{AL}=n_{alcl_3}=\frac{2}{3}n_{H_2}=0,2mol\)
\(\rightarrow m_{AL}=0,2\cdot27=5,4g\)
\(\rightarrow m=5,4\)
b)\(m_{muối}=m_{alcl_3}=0,2\cdot133,5=26,7g\)

a) $n_{Mg} = \dfrac{4,8}{24} = 0,2(mol)$
$Mg + 2HCl \to MgCl_2 + H_2$
Theo PTHH :
$n_{HCl} = 2n_{Mg} = 0,4(mol) \Rightarrow m_{HCl} = 0,4.36,5 = 14,6(gam)$
b)
$n_{MgCl_2} = n_{Mg} = 0,2(mol) \Rightarrow m_{MgCl_2} = 0,2.95 = 19(gam)$
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ 0,2.......0,4........0,2.........0,2\left(mol\right)\\ a.m_{HCl}=0,4.36,5=14,6\left(g\right)\\ b.m_{MgCl_2}=0,2.95=19\left(g\right)\)

\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\ a.Mg+2HCl\rightarrow MgCl_2+H_2\\ n_{H_2}=n_{MgCl_2}=n_{Mg}=0,2\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\\ b.n_{HCl}=0,2.2=0,4\left(mol\right)\\ m_{ddHCl}=\dfrac{0,4.36,5.100}{7,3}=200\left(g\right)\\ c.m_{ddsau}=4,8+200-0,2.2=204,4\left(g\right)\\ C\%_{ddMgCl_2}=\dfrac{0,2.95}{204,4}.100\approx9,295\%\\ d.V_{ddHCl}=\dfrac{200}{1,05}=\dfrac{4000}{21}\left(ml\right)=\dfrac{4}{21}\left(l\right)\\ C_{MddHCl}=\dfrac{0,4}{\dfrac{4}{21}}=2,1\left(M\right)\)

số mol kẽm tham gia phản ứng là:\(n_{Zn}=\frac{m}{M}=\frac{6,5}{65}=0,1\left(mol\right)\)
PTHH:
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1 (mol)
a, thể tích khí hiđro thu được là:\(V_{H_2}=n_{H_2}\times22,4=0,1\times22,4=2,24\left(l\right)\)
b,khối lượng HCl cần dùng là:\(m_{HCl}=n_{HCl}\times M=0,2\times65=13\left(g\right)\)
thk nhá