
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Zn+2HCl->ZnCl2+H2
Zn+H2SO4->ZnSO4+H2
Fe+2HCl->FeCl2+H2
Fe+H2SO4->FeSO4+H2
\(Zn+2HCl\rightarrow ZnCl_2+H_2\\ Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ Fe+2HCl\rightarrow FeCl_2+H_2\)

a.
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
b.
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Thêm đk H2SO4 loãng chứ đặc nóng có thể giải phóng H2S, SO2,...

\(Zn + 2HCl \to ZnCl_2 + H_2\\ Zn + H_2SO_4 \to ZnSO_4 + H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ Fe + H_2SO_4 \to FeSO_4 + H_2\\ n_{Fe} = n_{Zn} = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)\\ m_{Fe} = 0,1.56 = 5,6(gam) ; m_{Zn} = 0,1.65 = 6,5(gam)\)

Hãy viết các phương trình hóa học sau đây:
a/ Nhiệt phân thuốc tím KMnO4
2KMNO4-to>K2MnO4+MnO2+O2
b/ Điều chế khí hydrogen (hidro) từ kim loại sắt và hydrochloride acid (axit clohidric) HCl
Fe+2HCl->FeCl2+H2
c/ Điện phân nước
2H2O-đp->2H2+O2
d/ Phản ứng giữa P2O5. và nước
P2O5+3H2O->2H3PO4
e/ Đốt cháy kim loại kẽm trong khí oxigen (oxi)
2Zn+O2-to>2ZnO
`a)` `2KMnO_4` $\xrightarrow[]{t^o}$ `K_2MnO_4 + MnO_2 + O_2`
`b) Fe + 2HCl -> FeCl_2 + H_2`
`c)` `2H_2O` $\xrightarrow[]{đpnc}$ `2H_2 + O_2`
`d) P_2O_5 + 3H_2O -> 2H_3PO_4`
`e) 2Zn + O_2` $\xrightarrow[]{t^o}$ `2ZnO`

a. Phương trình hóa học có thể điều chế hiđro.
Zn + 2HCl → ZnCl2 + H2
Fe + H2SO4 (loãng) → FeSO4 + H2
Zn + H2SO4 → ZnSO4 + H2
Fe + 2HCl → FeCl2 + H2
b. Số mol khí hiđro là: n = 0,1 (mol)
Khối lượng kẽm cần dùng là: m = 0,1x65 = 6,5 (g)
Khối lượng sắt cần dùng là: m = 0,1x56 = 5,6 (g).
Phan Thùy Linh tại sao lại số mol của H2 bằng 0,1 (vậy số liệu 2,24 l đang ở đâu, làm sao có kết quả này).
Khi viết m, viết n em có biết khối lượng của cái gì hay là số mol của cái gì đâu. dù đã dẫn ở lời giải nhưng vẫn phải viết chứ.
Đối với những phản ứng điều chế khí thì khí thường bay hơi nên phải có chiều mũi tên đi lên nhé.
Đối với phản ứng số (3) thì Zn chỉ phản ứng được với "H2SO4 (loãng)" thôi.

a) Zn + 2HCl --> ZnCl2 + H2
b) \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
_____0,15<-------------------0,15
=> mZn = 0,15.65 = 9,75(g)
c) \(n_{HCl}=\dfrac{3,65}{36,5}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
__________0,1------------->0,05
=> VH2 = 0,05.22,4 = 1,12(l)

a) PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
b) Ta có: \(n_{Zn}=\dfrac{97,5}{65}=1,5\left(mol\right)=n_{H_2}\)
\(\Rightarrow V_{H_2}=1,5\cdot22,4=33,6\left(l\right)\)
c) Khử 120 gam gì vậy bạn ??
a) PTHH: Zn+2HCl→ZnCl2+H2↑Zn+2HCl→ZnCl2+H2↑
b) Ta có: nZn=97,565=1,5(mol)=nH2nZn=97,565=1,5(mol)=nH2
⇒VH2=1,5⋅22,4=33,6(l)
c) ???
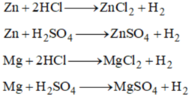
\(Zn+2HCl->ZnCl_2+H_2\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)