Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Theo thời gian, nồng độ có xu hướng tăng dần
=> Đồ thị mô tả sự thay đổi nồng độ theo thời gian của sản phẩm HCl
b) Đơn vị của tốc độ phản ứng trong trường hợp này là phút (min).

Fe2O3 + 2Al → 2Fe + Al2O3
Phản ứng làm tăng nhiệt độ môi trường xung quanh, tỏa nhiệt lớn, lên đến 2500 oC

- Nồng độ chất phản ứng giảm dần theo thời gian
- Nồng độ chất sản phẩm tăng dần theo thời gian

- Sự hô hấp cung cấp oxygen cho các phản ứng oxi hóa chất béo, chất đường, tinh bột,... trong cơ thể con người đó là các phản ứng giải phóng năng lượng
- Năng lượng kèm theo các phản ứng dùng để cung cấp năng lượng cho các hoạt động

- Để đánh giá mức độ nhanh hay chậm của một phản ứng hóa học, người ta dùng đại lượng: tốc độ phản ứng
- Cách tính: Cho phản ứng tổng quát:
aA + bB → cC + dD
Biểu thức tốc độ trung bình của phản ứng:
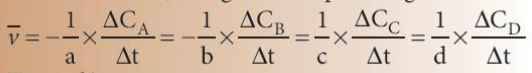
Trong đó:
\(\overline{v}\): tốc độ trung bình của phản ứng
∆C = C2 – C1: sự biến thiên nồng độ
∆t = t2 – t1: biến thiên thời gian
C1, C2 là nồng độ của một chất tại 2 thời điểm tương ứng t1, t2

1.
- Từ F2 đến I2, tính oxi hóa của các halogen giảm dần
=> Khả năng hoạt động của các đơn chất halogen giảm dần
=> Xu hướng phản ứng với hydrogen giảm dần
2.
- Dựa vào Bảng 12.2 ta nhận thấy: Từ F đến I, năng lượng liên kết của halogen với hydrogen giảm dần
=> Khả năng halogen liên kết với hydrogen giảm dần
=> Xu hướng phản ứng của các đơn chất halogen với hydrogen giảm dần từ F2 đến I2

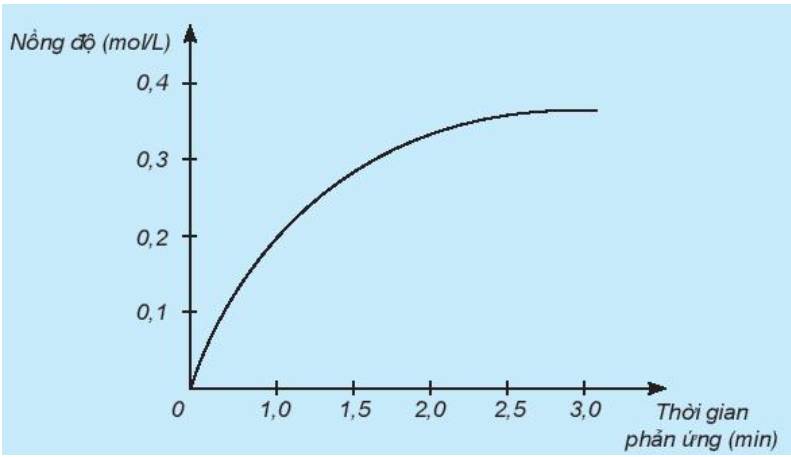 a) Đồ thị này mô tả sự thay đổi nồng độ theo thời gian của chất nào?
a) Đồ thị này mô tả sự thay đổi nồng độ theo thời gian của chất nào?



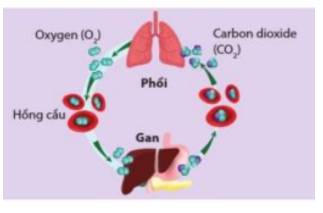
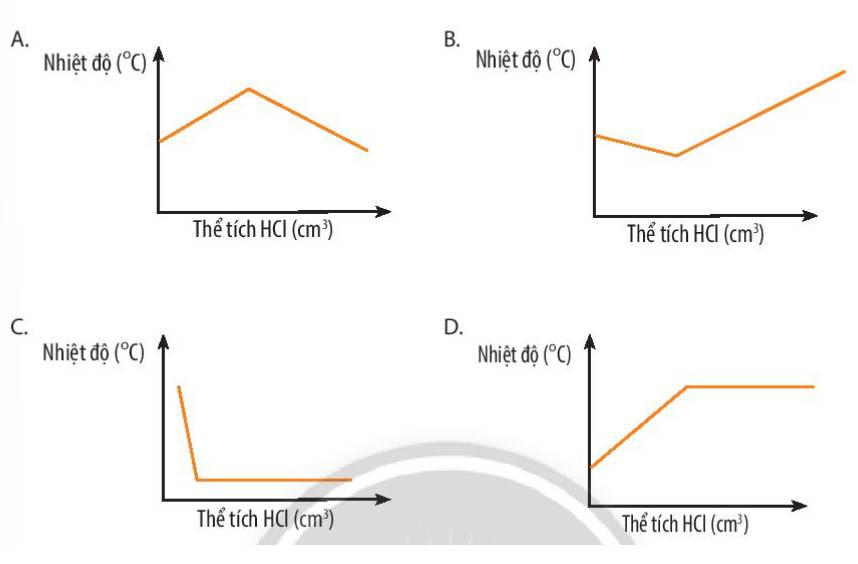



- Phản ứng có kèm theo sự thay đổi năng lượng dưới dạng nhiệt năng đóng vai trò quan trọng trong đời sống:
+ Cung cấp nhiệt cho các nhu cầu đun nấu thức ăn
+ Giảm nhiệt độ của môi trường xung quanh