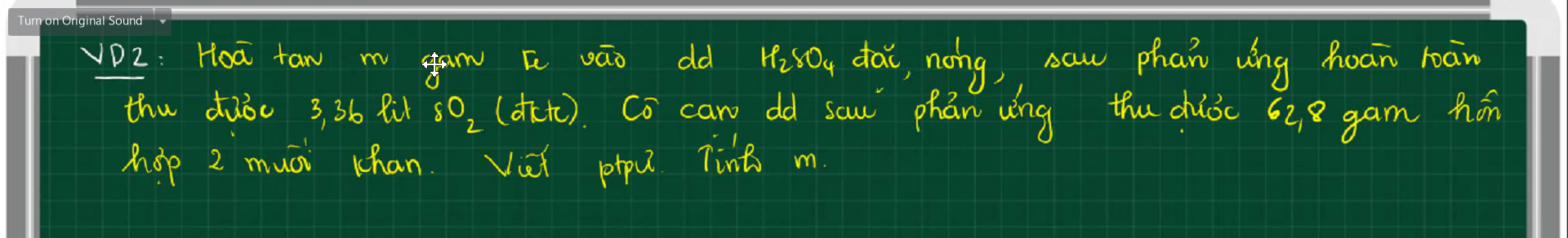Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


CuO + H2SO4 \(\rightarrow\)CuSO4 + H2O (1)
Cr2O3 + 3H2SO4 \(\rightarrow\)Cr2(SO4)3 + 3H2O (2)
Đặt nCuO=a
nCr2O3=b
Ta có :
\(\left\{{}\begin{matrix}80a+152b=69,2\\160a+392b=169,2\end{matrix}\right.\)
=>a=0,2;b=0,35
mCuO=80.0,2=16(g)
mCr2O3=69,2-16=53,2(g)
b;Theo PTHH 1 và 2 ta có:
nCuO=nH2SO4=0,2(mol)
3nCr2O3=nH2SO4=1,05(mol)
nCuO=nCuSO4=0,2(mol)
nCr2O3=nCr2(SO4)3=0,35(mol)
mH2SO4=(1,05+0,2).98=122,5(g)
mdd H2SO4=122,5:\(\dfrac{1,96}{100}=6250\left(g\right)\)
mCuSO4=0,2.160=32(g)
mCr2(SO4)3=392.0,35=137,2(g)
C% dd CuSO4=\(\dfrac{32}{6250+69,2}.100\%=0,5\%\)
C% dd Cr2(SO4)3=\(\dfrac{137,2}{6250+69,2}.100\%=2,17\%\)


$2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O(1)$
$Fe_2(SO_4)_3 + Fe\ to 3FeSO_4(2)$
Gọi $n_{Fe_2(SO_4)_3} = a(mol) ; n_{FeSO_4} = b(mol)$
Ta có : $400a + 152b = 62,8(1)$
$n_{SO_2} = 0,15(mol)$
$n_{Fe_2(SO_4)_3(1)} = \dfrac{1}{3}n_{SO_2} = 0,05(mol)$
$n_{Fe_2(SO_4)_3(2)} = \dfrac{1}{3}n_{FeSO_4} = \dfrac{b}{3}$
Suy ra:
$0,05 - \dfrac{b}{3} = a(2)$
Từ (1)(2) suy ra $a = \dfrac{45}{112} ; b = -1,055<0$
=> Sai đề

X: Fe3O4
Y: FeCl2
Z: FeCl3
T: Fe(OH)2
U: Fe(OH)3
A: NaCl (hoặc H2O)
B: H2O (hoặc NaCl)
D: H2 (hoặc Cl2)
E: Cl2 (hoặc H2)
F: NaOH
G: HCl
PTHH:
a) NaCl + H2O -dpmn----> 1/2 H2 + 1/2 Cl2 + NaOH
H2 + Cl2 -to-> 2 HCl
HCl + NaOH -> NaCl + H2O
b) 3 Fe +2 O2 -to->Fe3O4
Fe3O4 + 8 HCl -> FeCl2 +2 FeCl3 + H2O
FeCl2 + 2 NaOH -> Fe(OH)2 + 2 NaCl
FeCl3 +3 NaOH -> Fe(OH)3 + 3NaCl
Chúc em học tốt!

Gọi CTC là FexOy
\(n_{Fe}=0,1\left(mol\right)\)
\(Fe_xO_y+yCO-t^0->xFe+yCO_2\uparrow\)
0,1/x.....................................0,1
\(M_{Fe_xO_y}=56x+16y=\dfrac{8}{\dfrac{0,1}{x}}\)
\(\Leftrightarrow56x+16y=80x\)
\(\Leftrightarrow16y=24x\)
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{16}{24}=\dfrac{2}{3}\Rightarrow\left\{{}\begin{matrix}x=2\\y=3\end{matrix}\right.\)
CTHH : Fe2O3

mk có thể sử dụng cả 2 phương pháp
* đẩy nước thì đương nhiên rồi
*không khí có thể vì CO2 nặng hơn không khí

Bài 2 :
$n_{H_2SO_4} =0,52(mol)$
Gọi $n_{CuO} = a(mol) ; n_{MO} = b(mol)$
$\Rightarrow 80a + b(M + 16) = 20,8(1)$
$m_B = 64a + Mb = 18,56(2)$
$Cu + 2H_2SO_4 \to CuSO_4 +S O_2 + 2H_2O$
$M + 2H_2SO_4 \to MSO_4 + SO_2 + 2H_2O$
Theo PTHH : $2a + 2b = 0,52(3)$
Từ (1)(2)(3) suy ra vô nghiệm
Chứng tỏ oxit MO không bị khử bởi hidro
$m_B = 64a + b(M + 16) = 18,56(4)$
$MO + H_2SO_4 \to MSO_4 + H_2O$
$n_{H_2SO_4} = 2a + b = 0,52(5)$
Từ (1)(4)(5) suy ra a = 0,14 ; Mb = 5,76 ; b = 0,24
$\Rightarrow M = \dfrac{5,76}{0,24} = 24(Magie)$
b)
Cho hỗn hợp vào dung dịch NaOH lấy dư, lọc tách dung dịch :
- dung dịch : $NaOH,NaAlO_2$
- chất rắn : $CuO,MgO$
$2NaOH + 2Al + 2H_2O \to 2NaAlO_2 + 3H_2$
+) Sục $CO_2$ tới dư vào phần dung dịch, thu lấy kết tủa rồi nung ở nhiệt độ cao thì thu được $Al_2O_3$
$NaOH + CO_2 \to NaHCO_3$
$NaAlO_2 + 2H_2O + CO_2 \to Al(OH)_3 + NaHCO_3$
$2Al(OH)_3 \xrightarrow{t^o} Al_2O_3 + 3H_2O$
Nung phần chất rắn trong khí hidro ở nhiệt độ cao :
$CuO + H_2 \xrightarrow{t^o} Cu + H_2O$
Cho hỗn hợp chất rắn sau khi nung vào dung dịch HCl, lọc tách dung dịch :
- dung dịch : $MgCl_2$
- chất rắn : $Cu$
+) Nung chất rắn trong khí oxi lấy dư, thu được CuO$
$2Cu +O_2 \xrightarrow{t^o} 2CuO$
+) Cho phần dung dịch vào dung dịch NaOH lấy dư, thu lấy kết tủa nung ở nhiệt độ cao :
$MgCl_2 + 2NaOH \to Mg(OH)_2 + 2NaCl$
$Mg(OH)_2 \xrightarrow{t^o} MgO + H_2O$