Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
b, \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}=0,3\left(mol\right)\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
c, \(n_{AlCl_3}=n_{Al}=0,2\left(mol\right)\Rightarrow m_{AlCl_3}=0,2.133,5=26,7\left(g\right)\)

Giaỉ:
Ta có:
nZn=\(\frac{m_{Zn}}{M_{Zn}}=\frac{3,25}{65}=0,05\left(mol\right)\)
a) PTHH: Zn+ 2HCl -> ZnCl2 + H2
b) Theo PTHH và đề bài, ta có:
\(n_{ZnCl_2}\)= nZn = \(n_{H_2}\) = 0,05 (mol)
Khối lượng muối ZnCl2 tạo thành sau khi phản ứng kết thúc :
\(m_{ZnCl_2}=n_{ZnCl_2}.M_{ZnCl_2}\)= 0,05.126=6,3 (g)
Thể tích của khí H2 (đktc):
\(V_{H_2\left(đktc\right)}=n_{H_2}.22,4=0,05.22,4=1,12\left(l\right)\)

a/ PTHH: Zn + 2HCl ===> ZnCl2 + H2
b/ nZn = 16 / 65 = 0,25 mol
=> nH2 = nZn = 0,25 mol
=> VH2(đktc) = 0,25 x 22,4 = 5,6 lít
c/ nHCl = nZn = 0,25 mol
=> mHCl = 0,25 x 36,5 = 9,125 gam

Số mol của Zn là :
n=m:M=2,6:65=0,04(mol)
Số mol của H2 là
nH2=nZn=0,04(mol)
Thể tích của H2 là
V=n.22.4=0,04.22,4
=0,896(l)=896ml
Số mol của ZnCl2 là
nZnCl2=nZn=0,04(mol)
Khối lượng của ZnCl2 là
m=n.M=0,04.136=5,44(g)
PTHH: Zn + 2HCl ===> ZnCl2 + H2
nZn = 2,6 / 65 = 0,04 (mol)
=> nH2 = nZn = 0,04 (mol)
=> VH2(đktc) = 0,04 x 22,4 = 0,896 lít
=> nZnCl2 = nZn = 0,04 mol
=> mZnCl2 = 0,04 x 136 = 5,44 gam

\(n_{Zn}=\dfrac{32,5}{65}=0,5(mol)\\ a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ b,n_{H_2}=n_{Zn}=0,5(mol)\\ \Rightarrow V_{H_2(phản ứng)}=0,5.22,4=11,2(l)\\ \Rightarrow V_{H_2(thực tế)}=11,2.80\%=8,96(l)\)

a) Số mol kẽm tham gia phản ứng : \(n_{Zn}=\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{16,25}{65}=0,25\left(mol\right)\).
PTHH : \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Mol : 1 : 2 : 1 : 1
Mol : 0,25 → 0,5 → 0,25 → 0,5
Suy ra, số mol dung dịch Axit Clohidric \(HCl\) tham gia phản ứng là \(n_{HCl}=0,5\left(mol\right)\).
Khối lượng dung dịch đã dùng : \(m_{HCl}=n_{HCl}.M_{HCl}=\left(0,5\right).\left(36,5\right)=18,25\left(g\right)\).
b) Từ câu a, suy ra số mol khí Hidro sinh ra là \(n_{H_2}=0,25\left(mol\right)\).
Thể tích khí Hydro sinh ra là : \(V_{H_2}=n_{H_2}.22,4=\left(0,25\right).\left(22,4\right)=5,6\left(l\right)\)

nZn = \(\dfrac{13}{65}\)= 0,2mol
Zn + 2HCl -> ZnCl2 + H2
0,2->0,4 ->0,2
=>mHCl = 0,4 . 36,5 = 14,6 g
=>VH2 = 0,2 . 22,4 = 4,48 (l)
a) ta có nZn= \(\dfrac{13}{65}\)= 0,2( mol)
PTPU
Zn+ 2HCl\(\rightarrow\) ZnCl2+ H2
0,2...0,4.....................0,2..
b) mHCl= 0,4. 36,5=14,6( g)
c) VH2= 0,2. 22,4= 4,48( lít)
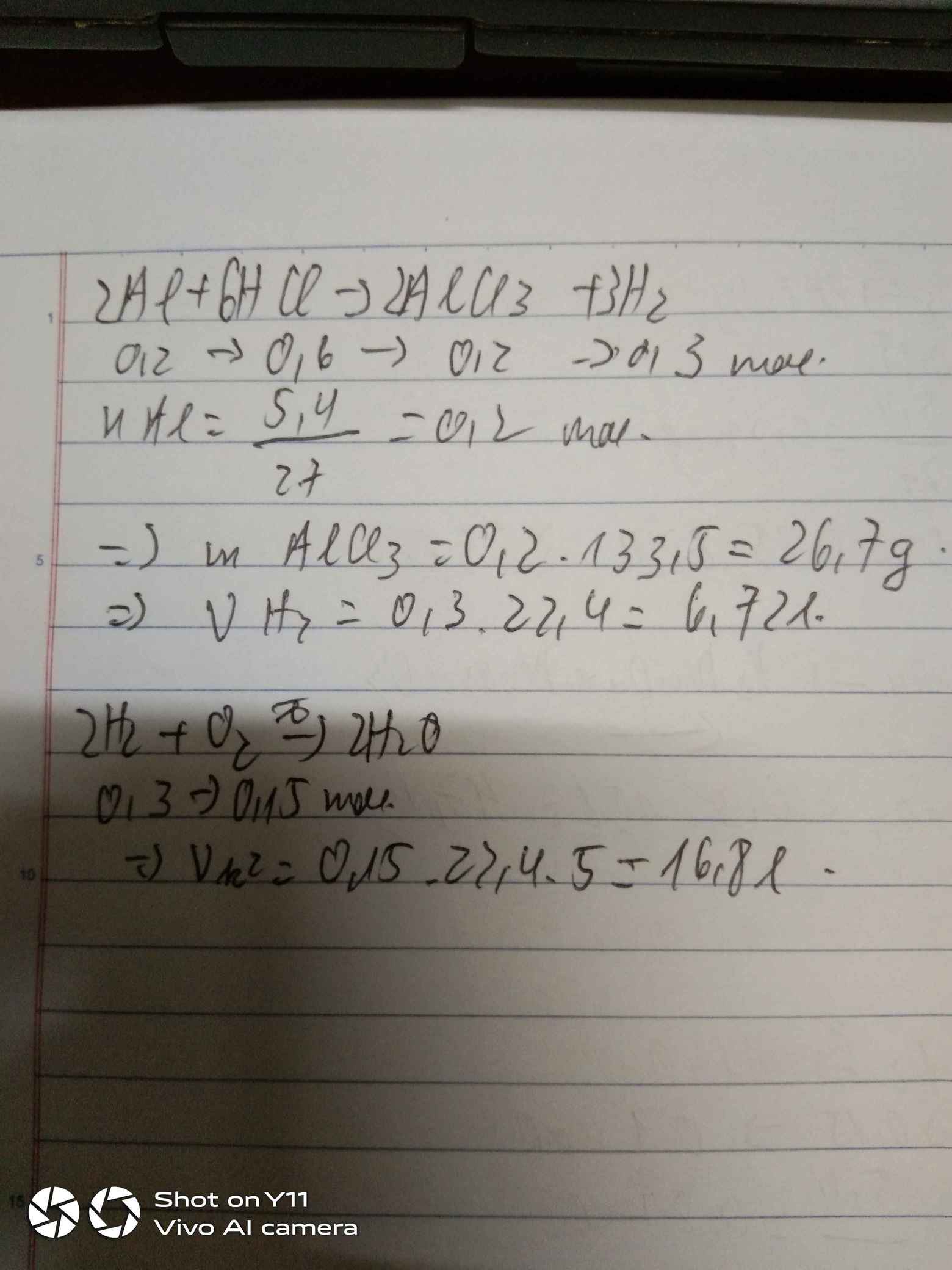
Bài 1.
a/ PTHH: Zn + 2HCl ===> ZnCl2 + H2
b/ nZn = 32,5 / 65 = 0,5 mol
=> nH2 = nZn = 0,5 mol
=> VH2(đktc) = 0,5 x 22,4 = 11,2 lít
Bài 2/
a/ PTHH: 2Al + 6HCl ==> 2AlCl3 + 3H2
b/ nAl = 4,05 / 27 = 0,15 mol
=> nH2 = 0,225 mol
=> VH2(đktc) = 0,225 x 22,4 = 5,04 lít
=> nAlCl3 = 0,15 mol
=> mAlCl3 = 0,15 x 133,5 = 20,025 gam