Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, \(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}=0,15\left(mol\right)\Rightarrow V_{H_2}=0,15.22,4=3,36\left(l\right)\)
b, Có lẽ đề hỏi bao nhiêu gam đồng thay vì "bao nhiêu gam sắt" bạn nhỉ?
\(n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,25}{1}>\dfrac{0,15}{1}\), ta được CuO dư.
Theo PT: \(n_{Cu}=n_{H_2}=0,15\left(mol\right)\Rightarrow m_{Cu}=0,15.64=9,6\left(g\right)\)

a,\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,2 0,4 0,2
b, \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
c, \(m_{HCl}=0,4.36,5=14,6\left(g\right)\)

\(n_{Fe}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.2.......0.4....................0.2\)
\(V_{H_2}=0.2\cdot22.4=4.48\left(l\right)\)
\(m_{HCl}=0.4\cdot36.5=14.6\left(g\right)\)
PTHH : \(Fe+2HCl-->FeCl_2+H_2\uparrow\) (1)
\(n_{Fe}=\dfrac{m}{M}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
Từ (1) => \(n_{Fe}=n_{H_2}=0.2\left(mol\right)\)
=> \(V_{H2\left(đktc\right)}=n.22,4=0,2.22,4=4,48\left(l\right)\)
Từ (1) => \(2n_{Fe}=n_{HCl}=0.4\left(mol\right)\)
=> \(m_{HCl}=n.M=0,4.\left(1+35.5\right)=14.6\left(g\right)\)

nFe = 16,8/56 = 0,3 (mol)
PTHH: Fe + 2HCl -> FeCl2 + H2
Mol: 0,3 ---> 0,6 ---> 0,3 ---> 0,3
VH2 = 0,3 . 24,79 = 7,437 (l)
mHCl = 0,6 . 36,5 = 21,9 (g)
PTHH: CuO + H2 -> (t°) Cu + H2O
Mol: 0,3 <--- 0,3 ---> 0,3
mCu = 0,3 . 64 = 19,2 (g)
mFe = 16,8: 56 =0,3(mol)
pthh : Fe + 2HCl --> FeCl2 + H2 (1)
0,3 ->0,6-----------------> 0,3 (mol)
=> VH2 (đkc) = 0,3 . 24,79 ( l)
=> mHCl = 0,6 . 35,5 = 21,9 (g)
pthh : CuO + H2 -t--> Cu+ H2O
0,3<-----0,3 (mol)
=>mCu = 0,3 . 64 = 19,2 (g)

nFe = \(\dfrac{11,2}{56}=0,2\left(mol\right)\)
Pt: Fe + 2HCl ---> FeCl2 + H2
....0,2.....0,4............0,2........0,2
mHCl cần dùng = 0,4 . 36,5 = 14,6 (g)
Pt: CuO + H2 --to--> Cu + H2O
................0,2.............0,2
mCu thu được = 0,2 . 64 = 12,8 (g)
a) Pt : Fe + 2HCl -----> FeCl2 + H2 (1)
0,2-->0,4------------------>0,2
b)nFe = 11,2 : 56 = 0,2 (mol)
- Theo pt(1) : nHCl = 2nFe=2*0,2=0,4 (mol)
mHCl = n*M= 0,4*36,5=14,6 (g)
Vậy khối lượng HCl cần dùng là 14,6g
c) Ta có pt : CuO + H2 ----> Cu + H2O (2)
0,2------>0,2
- Theo pt(2): nCu= nH2= 0,2 (mol)
mCu= n*M= 0,2*64=11,2 (g)
Vậy khi dẫn toàn bộ lượng khí H2 sinh ra đi qua CuO đã được đun nóng thi thu được 11,2 g đồng

\(nAl=\dfrac{13,5}{27}=0,5\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
2 6 2 3 (mol)
0,5 1,5 0,5 0,75 (mol)
a. \(VH_2=0,75.22,4=16,8\left(l\right)\)
b.
\(FeO+H_2\rightarrow Fe+H_2O\)
1 1 1 1 (mol)
0,75 0,75 0,75 0,75
\(m_{Fe}=0,75.42\left(g\right)\)

a, \(Fe+2HCl\rightarrow FeCl_2+H_2\)
b, \(n_{Fe}=\dfrac{3,36}{56}=0,06\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Fe}=0,06\left(mol\right)\Rightarrow V_{H_2}=0,06.22,4=1,344\left(l\right)\)
c, \(n_{Fe_2O_3}=\dfrac{4}{160}=0,025\left(mol\right)\)
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Xét tỉ lệ: \(\dfrac{0,025}{1}>\dfrac{0,06}{3}\), ta được Fe2O3 dư.
Theo PT: \(n_{Fe_2O_3\left(pư\right)}=\dfrac{1}{3}n_{H_2}=0,02\left(mol\right)\Rightarrow n_{Fe_2O_3\left(dư\right)}=0,025-0,02=0,005\left(mol\right)\)
\(\Rightarrow m_{Fe_2O_3\left(dư\right)}=0,005.160=0,8\left(g\right)\)
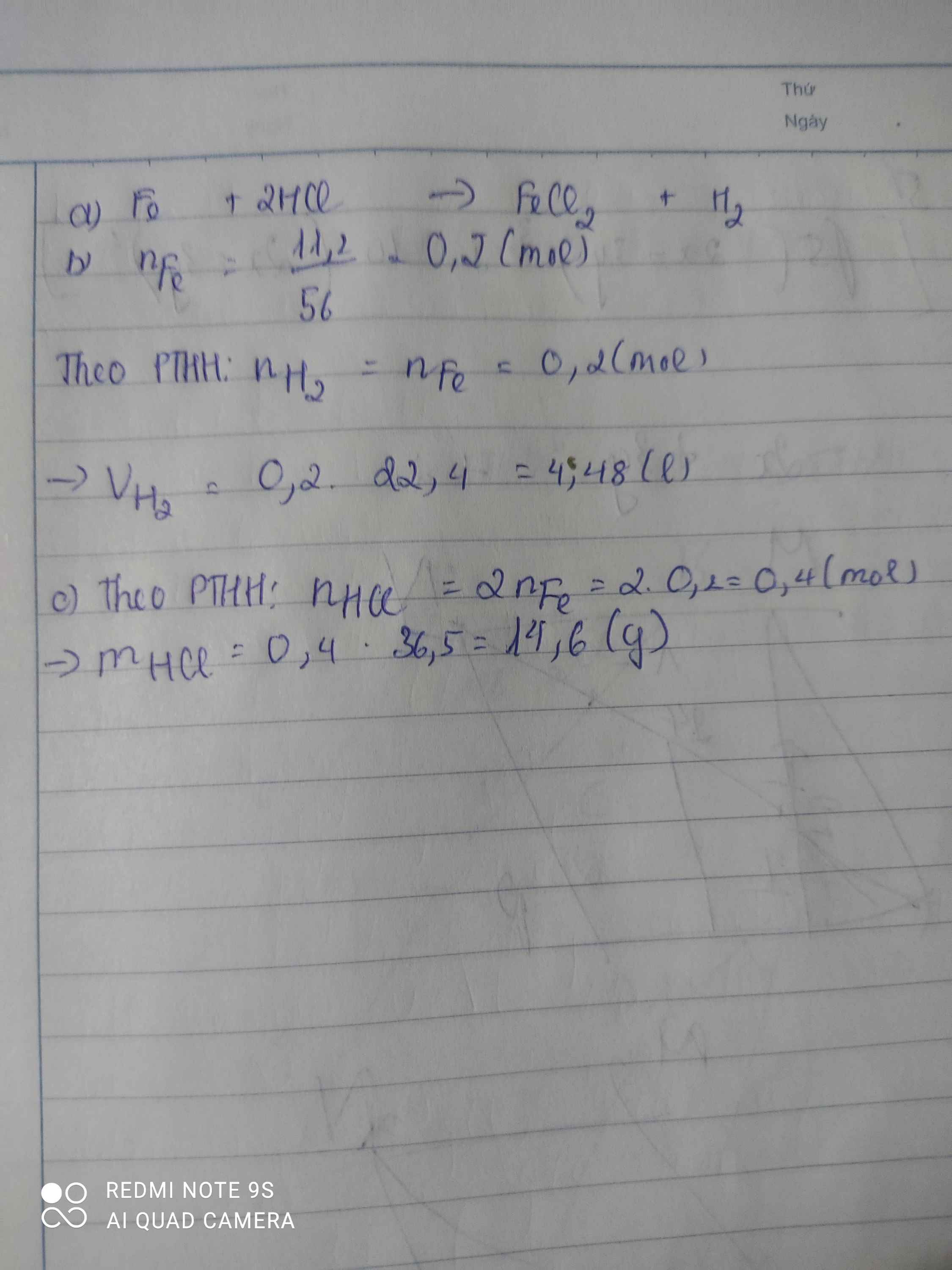
a) \(Fe+2HCl\rightarrow FeCl_2+H_2\)
b) \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Theo PTHH: \(n_{HCl}=2n_{Fe}=0,4\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
c) Theo PTHH: \(n_{FeCl_2}=n_{H_2}=n_{Fe}=0,2\left(mol\right)\)
\(\Rightarrow m_{FeCl_2}=0,2.127=25,4\left(g\right)\)
d) \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
e) \(n_{CuO}=\dfrac{24}{80}=0,3\left(mol\right)\)
PTHH: \(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,2}{1}\Rightarrow CuO\) dư
Theo PTHH: \(n_{Cu}=n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,2.64=12,8\left(g\right)\)