Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Bài giảng học thử
Video không hỗ trỡ trên thiết bị của bạn!
Bài 4. Chất béo (P1) - Hóa học lớp 9 - cô Hương Giang
Video không hỗ trỡ trên thiết bị của bạn!
Chuyên đề 2. Các oxit của cacbon (P2) - Ôn luyện Hóa học lớp 9 - cô Trịnh Mỹ Hạnh
Video không hỗ trỡ trên thiết bị của bạn!
Chuyên đề 9. Tính theo phương trình hóa học (tiết 2 - P1) - Ôn luyện Hóa học lớp 9 - cô Trịnh Mỹ Hạnh
Video không hỗ trỡ trên thiết bị của bạn!
Chuyên đề 4. Bazơ (P1) - Ôn luyện Hóa học lớp 9 - cô Trịnh Mỹ Hạnh
Video không hỗ trỡ trên thiết bị của bạn!
Bài 1. Tính chất của kim loại (P1) - Hóa học lớp 9 - cô Hương Giang

Tham khảo :
1. Tác dụng với phi kim
a) Tác dụng với oxi
Al bền trong không khí ở nhiệt độ thường do có lớp màng oxit Al2O3 rất mỏng bảo vệ.
b) Tác dụng với phi kim khác
2. Tác dụng với axit
+ Axit không có tính oxi hóa: dung dịch axit HCl, H2SO4 loãng
2Al + 6HCl → 2AlCl3 + 3H2↑
+ Axit có tính oxi hóa mạnh: dung dịch HNO3 loãng, HNO3 đặc, nóng và H2SO4 đặc, nóng.
Nhôm bị thụ động hoá trong dung dịch HNO3 đặc, nguội hoặc H2SO4 đặc nguội.
3. Tác dụng với oxit kim loại( Phản ứng nhiệt nhôm)
Lưu ý: Nhôm chỉ khử oxit của các kim loại đứng sau nhôm
4. Tác dụng với nước
- Phá bỏ lớp oxit trên bề mặt Al (hoặc tạo thành hỗn hống Al-Hg thì Al sẽ phản ứng với nước ở nhiệt độ thường)
2Al + 6H2O → 2Al(OH)3↓ + 3H2↑
5. Tác dụng với dung dịch kiềm
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
6. Tác dụng với dung dịch muối
- Al đẩy được kim loại đứng sau ra khỏi dung dịch muối của chúng:

Dùng quỳ tím:
+ Chuyển màu là \(H_2SO_4,HCl\)
+ Không chuyển màu là nước cất
Dùng \(BaCl_2\):
+ Tạo phản ứng kết tủa: \(H_2SO_4\)
+ Không phản ứng: \(HCl\)
\(PTHH:H_2SO_4+BaCl_2\rightarrow BaSO_4+2HCl\)

Câu 1:
+ Tác dụng với kim loại: O2 oxi hóa được hầu hết các kim loại trừ Ag, Au, Pt
2Cu+O2to→2CuO2Cu+O2→to2CuO
+ Tác dụng với Hiđro, Phản ứng có thể gây nổ mạnh nếu tỉ lệ phản ứng O2:H2 = 1:2
O2+2H2to→2H2OO2+2H2→to2H2O
+ Tác dụng với một số phi kim khác:
4P+5O2to→2P2O54P+5O2→to2P2O5
+ Tác dụng với một số hợp chất:
C2H5OH+3O2to→2CO2+3H2OC2H5OH+3O2→to2CO2+3H2O
Câu 2:
+ Phản ứng hóa hợp là PƯHH trong đó có một chất mới được tạo thành từ hai hay nhiều chất ban đầu.
3Fe+2O2to→Fe3O43Fe+2O2→toFe3O4
+ Phản ứng phân hủy là PƯHH trong đó có 2 hay nhiều chất được tạo thành từ một chất ban đầu.
2KClO3
Câu 2:
+ Phản ứng hóa hợp là PƯHH trong đó có một chất mới được tạo thành từ hai hay nhiều chất ban đầu.
3Fe+2O2to→Fe3O43Fe+2O2→toFe3O4
+ Phản ứng phân hủy là PƯHH trong đó có 2 hay nhiều chất được tạo thành từ một chất ban đầu.
2KClO3to→3O2↑+2KCl

Phản ứng của kim loại với phi kim:
- Tác dụng với oxi: \(2Cu+O_2\rightarrow2CuO\)
- Tác dụng với phi kim khác: \(4Fe+3O_2\rightarrow2Fe_2O_3\)
Phản ứng của kim loại với dd axit: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Phản ứng của kim loại với dd muối: \(Zn+CuSO_4\rightarrow ZnSO_4+CU\)

1: Tác dụng được với nước:
Na2O + H2O -> 2NaOH
2: Tác dụng đươc với axit
Na2O + HCl -> NaCl + H2O
3: Tác dụng được với oxit axit
Na2O + SO2 -> Na2SO3
Tính chất hóa học:
- Na\(_2\)O là 1 oxit bazơ nên nó có đầy đủ tính chất hóa học của một oxit bazơ như:
+ Tác dụng với nước.
+ Tác dụng với oxit axit.
+ Tác dụng với axit . . .
1. Tác dụng với nước → dung dịch bazơ
- Na\(_2\)O tan được trong nước tạo thành dung dịch trong suốt, không màu không mùi, không vị. Dung dịch này có tính ăn mòn như làm mòn da, làm mòn vải . . . nên nó còn có tên gọi khác là xút ăn da.
Na\(_2\)O + H\(_2\)O → 2NaOH
2. Tác dụng với oxit axit → muối:
Ở trong môi trường bình thường Na\(_2\)O sẵn sàng tác dụng với những oxit axit khác để tạo thành hợp chất mới là muối.
Na\(_2\)O + CO\(_2\) → Na\(_2\)CO\(_3\)
3. Tác dụng với dung dịch axit → thành muối và giải phóng nước.
Na\(_2\)O + 2HCl → 2NaCl + H\(_2\)O
4. Tác dụng với oxi → peoxit; supeoxit.

tham khảo:
le_linh06/03/2020
Đáp án:
Tính chất hóa học của oxit
1. Oxit bazơ
- Tác dụng với nước: Một số oxit bazơ tác dụng với nước tạo thành dung dịch bazơ (kiềm)
VD: Na2O + H2O → 2NaOH
BaO + H2O → Ba(OH)2
Những oxit bazơ tác dụng với nước và do đó cũng tan được trong nước là:
Na2O, K2O, CaO, BaO, Li2O, Rb2O, Cs2O, SrO
- Tác dụng với axit:
Oxit bazơ + axit → muối + nước
VD: Fe2Fe2 O33 + 3H22 SO44 → Fe22 (SO44) 33 +3H22O
- Tác dụng với oxit axit: Một số oxit bazơ, là những oxit bazơ tan trong nước tác dụng với oxit axit tạo thành muối.
2. Oxit axit
-Tác dụng với nước tạo thành dung dịch axit
Oxit axit + nước -> axit
CO2CO2 + H22 O -> H22 CO33
- Tác dụng với dung dịch bazơ tạo thành muối và nước
SO33 + 2NaOH -> Na22SO44 +H22O
- Tác dụng với 1 số oxit bazơ tạo thành muối
CO22 +CaO -> CaCO3
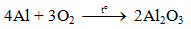
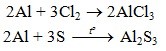
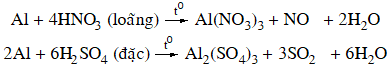
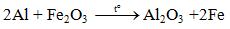
okay đợi xíu
Nhôm tác dụng với phi kim:
+) Nhôm tác dụng với oxi
PTHH : 4Al + 3O2 --nt---> 2Al2O3
+) Nhôm tác dụng với phi kim khác
PTHH: 2Al + 3S --nt---> Al2S3
Nhôm tác dụng với dd axit ( HCl, H2SO4 )
PTHH : 2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2 ↑
Nhôm tác dụng với dd muối
PTHH : 2Al + 3CuSO4 ----> Al2(SO4)3 + 3Cu
Nhôm tác dụng với dd kiềm
PTHH : 2Al + 2NaOH + 2H2O ----> 2NaAlO2 + 3H2 ↑