Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1, PTHH :
(1) S + O2 --> SO2
(2) SO2 + NaOH --> NaHSO3
(3) SO2 + 2 NaOH --> Na2SO3 + H2O
Phần I : tác dụng với dung dịch CaCl2 sinh kết tủa .
=> X có chứa Na2SO3.
Phần II tác dụng với dung dịch Ca(OH)2 sinh nhiều kết tủa hơn.
=> dung dịch X có muối NaHSO3
(4) Na2SO3 + CaCl2 --> CaSO3 + 2NaCl
(5) Na2SO3 + Ca(OH)2 -->CaSO3 + 2NaOH
(6) NaHSO3 + Ca(OH)2 --> CaSO3 + NaOH + H2O
\(n_S=\dfrac{a}{32}\left(mol\right)\), nNaOH = 0,2 b ( mol)
Theo bài ra : d > c .
Theo (2),(3), để SO2 tác dụng với dung dịch NaOH sinh 2 loại muối thì :
\(1< \dfrac{n_{NaOH}}{n_S}< 2\)
\(=>1< \dfrac{6,4b}{a}< 2\)
\(=>3,2b< a< 6,4b\)
...

- Phần 1 tác dụng với Br2: nBr2 = 16:160 = 0,1 mol
C2H2 + 2Br2 → C2H2Br4
0,05 ← 0,1 (mol)
- Đặt số mol khí mỗi phần như sau:
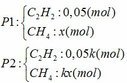
+ Số mol hỗn hợp khí X là: nX = 11,2:22,4 = 0,5 mol
Ta có: n khí P1 + n khí P2 = nX => 0,05 + x + 0,05k + kx = 0,5 <=> (x + 0,05)k = 0,45 - x
=> 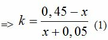
+ Đốt cháy phần 2:
C2H2 + 2,5O2 → t ∘ 2CO2 + H2O
0,05k → 0,1k→ 0,05k (mol)
CH4 + 2O2 → t ∘ CO2 + 2H2O
kx → kx → 2kx (mol)
Sản phẩm cháy gồm
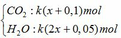
dẫn qua dung dịch Ba(OH)2 dư:
CO2 + Ba(OH)2 → BaCO3↓ + H2O
k(x+0,1) → k(x+0,1) (mol)
Khối lượng dung dịch giảm: m dd giảm = mBaCO3 – mCO2 – mH2O
=> 197k(x+0,1) – 44k(x+0,1) – 18k(2x+0,05) = 69,525
=> 153k(x+0,1) – 18k(2x+0,05) = 69,525
=> k(117x+14,4) = 69,525
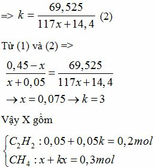
CaC2 + 2H2O → Ca(OH)2 + C2H2
0,2 ← 0,2 (mol)
Al4C3 + 12H2O → 4Al(OH)3 + 3CH4
0,1 ← 0,1 (mol)
Giá trị của m là: m = mCaC2 + mAl4C3 = 0,2.64 + 0,1.144 = 27,2 gam
Phần trăm thể tích các khí trong X là:

tác dụng với AgNO3 trong NH3 dư:
C2H2 + 2AgNO3 + 2NH3 → Ag2C2↓ + 2NH4NO3
0,15 → 0,15 (mol)
Khối lượng kết tủa thu được là: mAg2C2 = 0,15.240 = 36 gam

Ta có :
$n_{CO_2} = n_{CaCO_3} = \dfrac{10}{100} = 0,1(mol)$
$\Rightarrow n_{H_2O} = \dfrac{7,1 - 0,1.44}{18} = 0,15(mol)$
Bảo toàn C, H :
$n_C = n_{CO_2} = 0,1(mol)$
$n_H = 2n_{H_2O} = 0,3(mol)$
$\Rightarrow n_O = \dfrac{2,3 - 0,1.12 - 0,3}{16} = 0,05(mol)$
$n_C : n_H : n_O = 0,1 : 0,3 : 0,05 = 2 : 6 : 1$
Vậy CTPT của X có thể là $C_2H_6O$

Nhiệt phân hỗn hợp, ta có PTPƯ:
BaCO3 BaO + CO2
MgCO3 MgO + CO2
Al2O3 không
Chất rắn Khí D: CO2.
+ Hòa tan A vào H2O dư, ta có PTPƯ:
BaO + H2O Ba(OH)2
MgO + H2O không
Al2O3 + Ba(OH)2 Ba(AlO2)2 + H2O
Kết tủa
+ Khi cho dung dịch B tác dụng với CO2 dư:
Ba(AlO2)2 + 2CO2 + 4H2O 2Al(OH)3 + Ba(HCO3)2
+ Hòa tan C vào dung dịch NaOH dư, ta có PTPƯ:
MgO + NaOH không
Al2O3 + 2NaOH 2NaAlO2 + H2O
(Vì kết tủa C cho vào dung dịch NaOH dư có tan một phần chứng tỏ C có Al2O3 dư; phần không tan là MgO).

Tính toán theo PTHH :
Fe3O4 + 8 HCl → 2 FeCl3 + FeCl2 + 4 H2O
FeCl2 + ½ Cl2 → FeCl3
FeCl2 + 3 AgNO3 → 2 AgCl + Ag + Fe(NO3)3
FeCl3 + 3 AgNO3 → 3 AgCl + Fe(NO3)3
Bảo toàn khối lượng
m2 – 0,5 m1 = m Cl2 ( lưu ý hỗn hợp chia làm 2 phần nên muối phản ứng ở mỗi phần là 0,5 m1 )
m2 – 0,5 m1 = m Cl2 => m Cl2 = 1,42 => n Cl2 = 0,02 mol
Theo PTHH : n FeCl2 = n Cl2 . 2 = 0,04 mol
Theo PTHH : n FeCl2 . 2 = n FeCl3 = 0,08 mol
Theo PTHH : n AgCl = 2 . nFeCl2 + 3 . n FeCl3 = 0,08 .3 + 0,04 .2 = 0,32 mol
n Ag = n FeCl2 = 0,04 mol
=> m Chất rắn = m Ag + m AgCl = 0,04 . 108 + 0,32 . 143,5 = 50,24 g
phản ứng của Fe2+ + Ag+ → Fe+3 + Ag

Câu 1 :
+ Dùng H2 khử MO :
MO + H2 -----------> M + H2O (1)
+ Theo đề bài : mH2SO4 ( trong dd 90%) = 15,3 . 90 /100 = 13,77 ( g)
+ Sau khi hấp thụ nước thì C% dd H2SO4 giảm xuống 86,34 %
=> mdd H2SO4 ( sau khi hấp thụ nước từ 1 ) = 13,77 . 100 % :86,34 % = 15,9485754 ( g)
=> m H2O được hấp thụ = 15,9485754 - 15,3 =0,6485754 (g)
=> n H2O được hấp thụ = 0,6485754 / 18 = 0,036
=> nH2O tạo ra ở (1) = 0,036 : 90% = 0,04 (mol)
=> nM = nMO (Pư) = 0,04 (mol )
+Hòa tan các chất rắn còn lại trong ống bằng dd HCl vừa đủ :
MgO + 2HCl ➜ MgCl2 + H2O (2)
Al2O3 + 6HCl ➜ 2AlCl3 + 3H2O (3)
=> dd B gồm : MgCl2 và AlCl3
Sau khi hòa tan, còn lại 2,56 gam M
=> MM = 2,56/0,04 = 64 ( Cu)
=> M là Cu
+ Lấy 1/10 dd B cho tác dụng với dd NaOH dư:
MgCl2 + NaOH ➜ Mg(OH)2 + NaCl (4)
AlCl3 + 3NaOH ➜ 3NaCl + Al(OH)3 (5)
Al(OH)3 + NaOH ➞ NaAlO2 + 2H2O (6)
+ Lọc kết tủa , nung đến khi khối lượng không đổi :
Mg(OH)2 ➜ MgO + H2O (7)
+ Thu được 0,28 g chất rắn
=> n MgO = 0,28 / 40 = 0,007 (mol )
+Theo (4)(7) :
1/10 nMgCl2 = 0,007 (mol)
=> n MgCl2 =0,007. 10 = 0,07 (mol)
+ Theo (2) :
n MgO = 0,07 (mol)
+ nCuO = 0,04 : 80% = 0,05 (mol)
=> %mMgO = 40 . 0,07 / 16,2 . 100% = 17,28 %
%mCuO = 80 . 0,05 /16,2 .100% = 24,69%
%mAl2O3= (16,2 - 0,05.64 - 0,07.40) / 16,2 .100% = 58,03%
P/S: mỏi tay quá @@

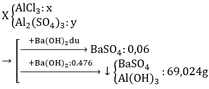
Cho Ba(OH)2 vào muối Al sẽ có 2TH sau:
TH1: kết tủa Al(OH)3 chưa bị hòa tan
Al3+ + 3OH– → Al(OH)3↓
→ nAl(OH)3 = nAl3+ → nAl(OH)3 = xn + 0,04n
TH2: kết tủa Al(OH)3 bị hòa tan một phần
Al3+ + 3OH– → Al(OH)3↓
(xn + 0,04n)→ 3(xn + 0,04n) (xn + 0,04n)
Al(OH)3 + OH– → AlO2– + 2H2O
0,952 – 3(xn + 0,04n) ←0,952
→ nAl(OH)3 = 4xn + 0,16n – 0,952



C2H4, C3H6, C4H8 cùng là anken nên có công thức chung là CnH2n
2CO + O2 → 2CO2↑ (1)
x → x (mol)
2H2 + O2 → 2H2O (2)
y → y (mol)
CnH2n + O2 → nCO2 + 2nH2O (3)
Sản phẩm cháy thu được gồm có CO2 và H2O.
Khi hấp thụ vào dd Ca(OH)2: 0,04 mol thu được dung dịch Y, thêm từ từ Ba(OH)2 vào dung dịch Y thu được kết tủa của các ion kim loại => CO2 phản ứng với Ca(OH)2 theo phương trình:
CO2 + Ca(OH)2 → CaCO3↓ + H2O (4)
CO2 + Ca(OH)2 → Ca(HCO3)2 + H2O (5)
Dd Y chứa Ca(HCO3)2
BaCl2 + Ca(HCO3)2 → CaCO3↓ + BaCO3↓ + H2O (6)
m1 = mCaCO3(4)
m2 = mCaCO3(5) + mBaCO3
=> m1 + m2 = ∑ mCaCO3↓ + mBaCO3 = 6,955 (g) (*)
BTNT Ca: => ∑nCaCO3↓ = ∑ nCa(OH)2 (4+5) = 0,04 (mol)
Từ (*)

=> nCaCO3(6) = nBaCO3 = 0,015 (mol)
=> nCaCO3(4) = ∑nCa(OH)2 – nBaCO3 = 0,04 – 0,015 = 0,025 (mol)
BTNT C => ∑ nCO2 = ∑ nCaCO3 + nBaCO3 = 0,04 + 0,015 = 0,055 (mol)
Khối lượng dd Y tăng 0,82 gam so với dd Ca(OH)2 ban đầu
=> mCO2 + mH2O – mCaCO3(4) = 0,82
=> mH2O = 0,82 + 0,025.100 – 0,055.44 = 0,9 (g)
=> nH2O = 0,9 : 18 = 0,05 (mol)
BTKL ta có: mhhX + mO2 = mCO2 + mH2O
=> mO2 = 0,055.44 + 0,9 – 0,92 = 2,4 (g) => nO2 = 0,075 (mol)
BTNT O: nO( trong CO) + 2nO2 = 2nCO2 + nH2O
=> nO( trong CO) = 2.0,055 + 0,05 – 0,075.2 = 0,01 (mol) => nCO = 0,01 (mol)
Từ PTHH (1), (2), (3) ta thấy khi đốt cháy CnH2n luôn cho nH2O = nCO2 => sự chênh lệch mol CO2 và mol H2O là do đốt cháy CO và H2
=> nCO2 – nH2O = x – y = 0,055 – 0,05 = 0,005 (mol)
Mặt khác: nCO – nH2 = x – y = 0,005 (mol)
=> nH2 = nCO – 0,005= 0,01 – 0,005 = 0,055 (mol)
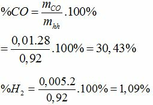
$n_{SO_2} = n_S = \dfrac{a}{32}(mol)$
$n_{NaOH} = 0,2b(mol)$
Ta thấy : d > c
Chứng tỏ X gồm hai muối $Na_2SO_3$ và $NaHSO_3$
Suy ra :
$1 < n_{NaOH} : n_{SO_2} < 2$
$⇔ 1< 0,2b : \dfrac{a}{32} < 2$
$⇔ \dfrac{a}{32} < 0,2b < \dfrac{a}{16}$
$⇔ \dfrac{5a}{32} < b < \dfrac{5a}{16}$