Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Có lẽ đoạn đề ". có 50 gam... 13,6 gam." bị thừa bạn nhỉ?
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\Rightarrow n_H=0,3.2=0,6\left(mol\right)\)
\(n_{CO_2}=\dfrac{26,4}{44}=0,6\left(mol\right)=n_C\)
⇒ mC + mH = 0,6.12 + 0,6.1 = 7,8 (g) < 9,4 (g)
→ X gồm C, H và O.
⇒ mO = 9,4 - 7,8 = 1,6 (g) \(\Rightarrow n_O=\dfrac{1,6}{16}=0,1\left(mol\right)\)
Gọi CTPT của X là CxHyOz.
⇒ x:y:z = 0,6:0,6:0,1 = 6:6:1
Mà: CTPT của X trùng với CTĐGN.
→ X là C6H6O.
- X có pư với NaOH → CTCT: C6H5OH.
\(n_X=\dfrac{4,7}{94}=0,05\left(mol\right)\), \(n_{NaOH}=0,1.1=0,1\left(mol\right)\)
PT: \(C_6H_5OH+NaOH\rightarrow C_6H_5ONa+H_2O\)
Xét tỉ lệ: \(\dfrac{0,05}{1}< \dfrac{0,1}{1}\), ta được NaOH dư.
Chất rắn thu được sau cô cạn gồm: NaOH dư và C6H5ONa.
Theo PT: \(n_{NaOH\left(pư\right)}=n_{C_6H_5ONa}=n_{C_6H_5OH}=0,05\left(mol\right)\)
\(\Rightarrow n_{NaOH\left(dư\right)}=0,1-0,05=0,05\left(mol\right)\)
⇒ m chất rắn = 0,05.40 + 0,05.116 = 7,8 (g)

Đáp án C
Vì sản phẩm sau phản ứng gồm H2O (hấp thụ bởi bình 1) và CO2 (hấp thụ bởi bình 2) nên X chứa C, H và có thể có O. Gọi công thức phân tử của X là CxHyOz.

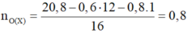
Vì hóa hơi hoàn toàn 5,2 gam X thu được thể tích bằng với thể tích của 1,6 gam O2 trong cùng điều kiện
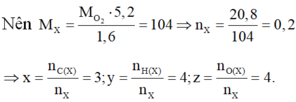
Vậy X là C3H4O4.

Có 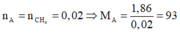
Số mol chất A đem đốt cháy là: x = 0,1 mol
![]()
![]()
0,2 0,2
![]()
0,4 0,2
![]()
0,2 0,2
Suy ra nCO = 0,6(mol).
![]() .
.
Do đó trong phân tử của A có 1 nguyên tử N.
Gọi công thức phân tử của A là CxHyOzN
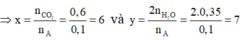
Ta lại có: 6.12 + 7 + 16z + 14 = 93 => z = 0
Vậy chất A có công thức phân tử là C6H7N.
Đáp án D.

\(n_{CO_2}=\dfrac{30}{100}=0,3\left(mol\right)\)
=> \(n_{H_2O}=\dfrac{17,25-0,3.44}{18}=0,225\left(mol\right)\)
Bảo toàn C: nC = 0,3 (mol)
Bảo toàn H: nH = 0,45 (mol)
=> \(n_O=\dfrac{6,45-0,3.12-0,45.1}{16}=0,15\left(mol\right)\)
Xét nC : nH : nO = 0,3 : 0,45 : 0,15 = 2 : 3 : 1
=> CTPT: (C2H3O)n
Xét \(M=\dfrac{3,44}{\dfrac{1,12}{28}}=86\left(g/mol\right)\)
=> n = 2
=> CTPT: C4H6O2
=> B
\(n_C=n_{CO_2}=n_{CaCO_3}=\dfrac{30}{100}=0,3\left(mol\right)\\ m_{H_2O}=m_{bình.tăng}-m_{CO_2}=17,25-0,3.44=4,05\left(g\right)\\ \Rightarrow n_{H_2O}=\dfrac{4,05}{18}=0,225\left(mol\right)\Rightarrow n_H=0,225.2=0,45\left(mol\right)\\ n_X=n_{N_2}=\dfrac{1,12}{28}=0,04\left(mol\right)\\ \Rightarrow M_X=\dfrac{3,44}{0,04}=86\left(\dfrac{g}{mol}\right)\\ n_{X\left(ban.đầu\right)}=\dfrac{6,45}{86}=0,075\left(mol\right)\\ m_C+m_H=0,3.12+0,45.1=4,05\left(g\right)< 6,45\left(g\right)\\ \Rightarrow X.có.O\\ Đặt:C_aH_bO_c\left(a,b,c:nguyên,dương\right)\\ m_O=6,45-4,05=2,4\left(g\right)\\ a:b:c=0,3:0,45:\dfrac{2,4}{16}=2:3:1\\ \Rightarrow CTTN:\left(C_2H_3O\right)_k\\ \Leftrightarrow43k=86\\ \Leftrightarrow k=2\)
=> CTPT: C4H6O2
Vậy chọn B

Đáp án B
nX = nO2 (0,32g) = 0,01 (mol) => MX = 42 (g/mol)
mb1 tăng = mH2O = 0,54 (g) => nH2O = 0,03 (mol)
mb2 tăng = mCO2 = 1,32 (g) => nCO2 = 0,03 (mol)
Gọi CTPT X: CxHy
=> x = nCO2/ nX = 3
y = 2nH2O/nX = 6
=> CTPT X: C3H6

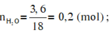
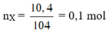
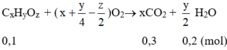

Ta có: \(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\Rightarrow n_H=0,2.2=0,4\left(mol\right)\)
\(n_C=n_{CO_2}=n_{CaCO_3}=\dfrac{30}{100}=0,3\left(mol\right)\)
⇒ mC + mH = 0,3.12 + 0,4.1 = 4 (g) < 10,4 (g)
→ A chứa C, H và O.
⇒ mO = 10,4 - 4 = 6,4 (g) ⇒ nO = 0,4 (mol)
Gọi CTPT của A là CxHyOz.
⇒ x:y:z = 0,3:0,4:0,4 = 3:4:4
→ CTPT của A có dạng (C3H4O4)n.
Mà: \(n_{A\left(5,2\left(g\right)\right)}=n_{O_2}=\dfrac{1,6}{32}=0,05\left(mol\right)\Rightarrow M_A=\dfrac{5,2}{0,05}=104\left(g/mol\right)\)
\(\Rightarrow n=\dfrac{104}{12.3+4+16.4}=1\)
Vậy: CTPT của A là C3H4O4.