Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: m dd tăng = mCO2 - m kết tủa = 5,5 - 12,5 = -7
→ dd giảm 7 (g)
Đáp án: D

a/ nBa(OH)2 = 0,1 x 0,3 = 0,03 mol
=> nOH- = 0,03 x 2 = 0,06 mol
nKOH = 0,1 x 0,3 = 0,03 mol
=> nOH- = 0,03 x 1 = 0,03 mol
PTHH:
2Na + 2H2O ===> 2NaOH + H2
x............x.......................x
=> nOH- = x (mol)
=> Tổng số mol của OH- = 0,06 + 0,03 + x = 0,09 + x (mol)
Lại có: nAl2(SO4)3 = 0,25 x 0,1 = 0,025 mol
Khi cho từ từ dung dịch X vào 250 ml dung dịch Al2(SO4)3 thì xảy ra :
3OH- + Al3+ ===> Al(OH)3 \(\downarrow\)
0,15......0,05...............0,05
SO42+ + Ba2+ ===> BaSO4 \(\downarrow\)
0,03......0,03...............0,03
Để lượng kết tủa thu được là lớn nhất
=> nOH- = 0,09 + x = 0,15
=> x = 0,06 mol
=> mNa = 0,06 x 23 = 1,38 gam
=> mkết tủa = 0,03 x 233 +0,05 x 78 = 10,89 gam
b/ nCO2 = 1,68 / 22,4 = 0,075 mol
=> \(\frac{n_{CO2}}{n_{OH^-}}=\frac{0,075}{0,15}=\frac{1}{2}\)
=> Phản ứng tạo muối trung hòa
=> mmuối khan = 0,03 x 197 + 0,03 x 106 + 0,015 x 138 = 11,16 gam

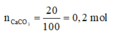
C O 2 + C a C O 3 + H 2 O → C a H C O 3 2
x……….x………..x
Theo PTHH ta có:
n C O 2 l t = x = n C a C O 3 =0,2mol
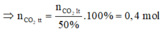
⇒ V C O 2 t t = 0,4.22,4 = 8,96 lit
Ta lại có:
C a O H 2 + C a H C O 3 2 → 2 C a C O 3 + 2 H 2 O
x………..x………2x
Vậy tối thiểu cần là x = 0,2 mol ⇒
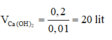
n C a C O 3 = 2x = 0,4 mol
⇒ m↓ = 0,4.100 = 40g
⇒ Chọn C.

Cho hỗn hợp (K, Li, Fe) vào dd CuCl2 dư.
\(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\)
\(Li+H_2O\rightarrow LiOH+\dfrac{1}{2}H_2\)
\(Fe+CuCl_2\rightarrow FeCl_2+Cu\)
\(CuCl_2+2KOH\rightarrow Cu\left(OH\right)_2+2KCl\)
\(CuCl_2+2LiOH\rightarrow Cu\left(OH\right)_2+2LiCl\)
\(FeCl_2+2KOH\rightarrow Fe\left(OH\right)_2+2KCl\)
\(FeCl_2+2LiOH\rightarrow Fe\left(OH\right)_2+2LiCl\)
\(A:Cu\left(OH\right)_2,Fe\left(OH\right)_2\)
\(B:KCl,LiCl,CuCl_2\)
\(D:H_2\)
Cho dd B pư với dd AgNO3 dư thu được kết tủa E và dd F
\(KCl+AgNO_3\rightarrow KNO_3+AgCl\)
\(LiCl+AgNO_3\rightarrow LiNO_3+AgCl\)
\(CuCl_2+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2AgCl\)
\(E:AgCl\)
\(F:KNO_3,LiNO_3,Cu\left(NO_3\right)_2\)
Cho kết tủa A nung trong không khí đến khối lượng không đổi thu được chất rắn G
\(Cu\left(OH\right)_2\underrightarrow{^{^{t^0}}}CuO+H_2O\)
\(4Fe\left(OH\right)_2+O_2\underrightarrow{^{^{t^0}}}2Fe_2O_3+4H_2O\)
\(G:CuO,Fe_2O_3\)
Dẫn khí D qua chất rắn G nung nóng thu được một chất rắn duy nhất.
\(CuO+H_2\underrightarrow{^{^{t^0}}}Cu+H_2O\)
\(Fe_2O_3+3H_2\underrightarrow{^{^{t^0}}}2Fe+3H_2O\)
Chổ này có gì nhầm lẫn thì phải , nếu như CuCl2 dư thì lượng Fe sẽ phản ứng hoàn toàn với CuCl2 tạo FeCl2 , nguyên tố Fe đi xuyên suốt đề bài rồi em !

Gọi số mol 2 muối trên lần lượt là a, b. Ta có:
- Số mol ion CO3(2-) là a+b
Số mol ion H+ =số mol HCl = 0,4. Do thêm từ từ HCl vào dd muối nên:
H+ + CO3(2-) -------> HCO3(-) (1)
Vì có khí thoát ra nên xảy ra phản ứng 2 => CO3(2-) hết
H+ + HCO3(-) -------> CO2 + H2O (2)
Do
Do dd Y tạo kết tủa với Ca(OH)2 nên dd Y có chứa ion HCO3- => sau (2) H+ hết, HCO3- dư => mol H+ (2) = mol CO2 =0,1 => mol H+(1)=a+b=0,4 - 0,1 = 0,3
Giải hệ: a+b = 0,3
106a + 138b = 35
ta được a = 0,2 b = 0,1 => khối lượng mỗi muối ^-^
- dd Y chứa 0,3 - 0,1 = 0,2 mol ion HCO3-
HCO3- + OH- ------> CO3(2-) + H2O
Ca2+ + CO3(2-) -----> CaCO3
Mol CaCO3 = mol CO3(2-) = mol HCO3- =0,2 => Khối lượng kết tủa^-^

\(n_{Fe}=\dfrac{6,5}{56}=\dfrac{13}{112}mol\)
\(m_{CH_3COOH}=\dfrac{90\cdot20\%}{100\%}=18g\Rightarrow n_{CH_3COOH}=0,3mol\)
\(Fe+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Fe+H_2\uparrow\)
\(\dfrac{13}{112}\) 0,3 0 0
\(\dfrac{13}{112}\) \(\dfrac{13}{56}\) \(\dfrac{13}{112}\) \(\dfrac{13}{112}\)
0 \(\dfrac{19}{280}\) \(\dfrac{13}{112}\) \(\dfrac{13}{112}\)
a)\(m_{\left(CH_3COO\right)_2Fe}=\dfrac{13}{112}\cdot174=20,2g\)
\(m_{H_2}=\dfrac{13}{112}\cdot2=\dfrac{13}{56}g\)
\(m_{dd\left(CH_3COO\right)_2Fe}=6,5+90-\dfrac{13}{56}=96,27g\)
\(C\%=\dfrac{20,2}{96,27}\cdot100\%=20,98\%\)