Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
\(FeO + CO \xrightarrow{t^o} Fe + CO_2\\ FeO + H_2 \xrightarrow{t^o} Fe + H_2O\\ CuO + CO \xrightarrow{t^o} Cu + CO_2\\ CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\\)
b) Khối lượng hỗn hợp giảm chính là khối lượng O(oxit) phản ứng .
\(H_2 + O_{oxit} \to H_2O\\ CO + O_{oxit} \to CO_2\\ n_{O(oxit)} = n_{H_2} + n_{CO} = \dfrac{5,6}{22,4} = 0,25(mol)\\ \Rightarrow a = m_O = 0,25.16 = 4(gam)\)

m(tăng) = mO = 0,32 (g)
nO = 0,32/16 = 0,02 (mol)
=> nhh khí = 0,02 (mol)
=> Vhh khí = 0,02 . 22,4 = 0,448 (l)

a/ Gọi số mol của CO và H2 lần lược là x, y thì ta có
\(n_{hhk}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(x+y=0,5\left(1\right)\)
Tỉ khối của hỗn hợp khí so với khí oxi là 0,55.
\(\Rightarrow\dfrac{28x+2y}{x+y}=0,55.32=17,6\)
\(\Leftrightarrow3y=2x\left(2\right)\)
Từ (1) và (2) ta có hệ: \(\left\{{}\begin{matrix}x+y=0,5\\3y=2x\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=0,3\\y=0,2\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,3}{0,5}.100\%=60\%\\\%V_{H_2}=100\%-60\%=40\%\end{matrix}\right.\)
b/ Khối lượng chất rắn giảm đi đúng bằng khối lượng O thêm vào để tạo CO2, H2O.
\(\Rightarrow n_O=0,5\left(mol\right)\)
\(\Rightarrow a=0,5.16=8\left(g\right)\)

- Cho phản ứng xảy ra hoàn toàn (2 chất trong A có sắt và oxit khác oxit sắt ban đầu)
\(yH_2+Fe_xO_y\rightarrow\left(t^o\right)xFe+yH_2O\left(1\right)\\ Fe+2HCl\rightarrow FeCl_2+H_2\left(2\right)\\ n_{H_2\left(2\right)}=n_{Fe\left(2\right)}=n_{Fe\left(1\right)}=0,3\left(mol\right)\\ n_{O\left(trong.oxit\right)}=n_{H_2O}=n_{H_2}=0,4\left(mol\right)\\ BTKL:m_{H_2}+m_{oxit}=m_A+m_{H_2O}\\ \Leftrightarrow0,4.2+m=28,4+18.0,4\\ \Leftrightarrow m=34,8\left(g\right)\\ b,x:y=0,3:0,4=3:4\Rightarrow x=3;y=4\\ \Rightarrow CTHH:Fe_3O_4\)

\(a) n_{Fe_3O_4} = a(mol) ; n_{CuO} = b(mol)\\ \Rightarrow 232a + 80b = 117,6(1)\\ Fe_3O_4 + 4H_2 \xrightarrow{t^o} 3Fe + 4H_2O\\ CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ n_{H_2} = 4a + b = \dfrac{40,32}{22,4}=1,8(2)\\ (1)(2)\Rightarrow a = 0,3 ;b = 0,6\\ \%m_{Fe_3O_4} = \dfrac{0,3.232}{117,6}.100\% =59,18\%\\ \%m_{CuO} = 100\%-59,18\% = 40,82\%\)
\(b)\\ n_{Fe} = 3a = 0,9(mol)\\ n_{Cu} = b = 0,6(mol)\\ \%m_{Fe} = \dfrac{0,9.56}{0,9.56+0,6.64}.100\% = 56,76\%\\ \%m_{Cu} = 100\% - 56,76\% = 43,24\%\)

Phương trình hóa học:
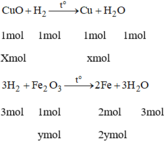
Gọi x là số mol của CuO
y là số mol của F e 2 O 3 .
Ta có: 80x + 160y = 16 (1)
Khối lượng hỗn hợp giảm do oxit tạo thành kim loại:
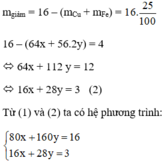
Giải hệ phương trình ta được:
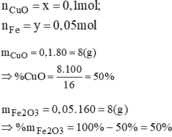

CuO + CO => Cu + CO2
PbO + CO => Pb + CO2
CuO + H2 => Cu + H2O
PbO + H2 => Pb + H2O
n khí = nCO + nH2 = V/22.4 = 13.44/22.4 = 0.6 (mol)
Theo ĐLBTKL:
mCuO + mPbO + m khí = mCu + mPb + mH2O + mCO2
Vì khi phản ứng kết thúc => lượng khí CO2 thoát ra => khối lượng hh giảm
mCO2 = n.M = a
nCO2 = nCO (Mà nH2 + nCO = 0.6)
Đề có thiếu gì không nhỉ
ko thiếu đâu bn ơi