Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) \(n_{CO_2}=\dfrac{6,6}{44}=0,15\left(mol\right)\Rightarrow n_C=0,15\left(mol\right)\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\Rightarrow n_H=0,4\left(mol\right)\)
=> \(n_O=\dfrac{3-0,15.12-0,4.1}{16}=0,05\left(mol\right)\)
Xét nC : nH : nO = 0,15 : 0,4 : 0,05 = 3 : 8 : 1
=> CTPT: (C3H8O)n
Mà MA = 60 g/mol
=> n= 1
=> CTPT: C3H8O
b)
(1) \(CH_3-CH_2-CH_2OH\)
(2) \(CH_3-CH\left(OH\right)-CH_3\)
c)
PTHH: \(2CH_3-CH_2-CH_2OH+2Na\rightarrow2CH_3-CH_2-CH_2ONa+H_2\)
\(2CH_3-CH\left(OH\right)-CH_3+2Na\rightarrow2CH_3-CH\left(ONa\right)-CH_3+H_2\)

a)
Do sau khi đốt cháy A thu được các sản phẩm chứa C, H, O
=> A chứa C, H và có thể có O
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
=> nC = 0,3 (mol)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\)
=> nH = 0,6 (mol)
Xét mC + mH = 0,3.12 + 0,6.1 = 4,2 (g) < 7,4 (g)
=> A chứa C, H, O
\(n_O=\dfrac{7,4-4,2}{16}=0,2\left(mol\right)\)
Xét nC : nH : nO = 0,3 : 0,6 : 0,2 = 3 : 6 : 2
=> CTPT: (C3H6O2)n
Mà MA = 4,625.16 = 74 (g/mol)
=> n = 1
=> CTPT: C3H6O2
b)
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,3------>0,3
=> mCaCO3 = 0,3.100 = 30 (g)
a) Gọi công thức phân tử của A là CxHyOz.
a ax a.
y\2 (mol)
Ta có :
(mol) ;
(mol)
=> mO = 7,4 – 0,3.12 -0,3.2 = 3,2g
=>có oxi
; nO = 0,2 (mol)
=> x : y : z = 3 : 6 : 2
công thức phân tử của X là C3H6O2
=>MA=74 g\mol
->CTHH :C3H6O2
b)
C3H6O2+7\2O2-to>3CO2+3H2O
0,3----------------------------0,3
CO2+Ca(OH)2->CaCO3+H2O
0,3-----------------------0,3 mol
=>m CaCO3=0,3.100=30g

(a) Gọi CTPT của các chất là CxHyOz
M<170 => mC<170.55,8% => 12x<94,86 => x<7,9
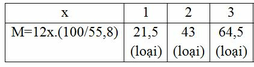
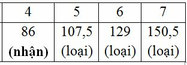
Vậy CTPT có dạng: C4HyOz (y≤10)(Do M là các số nguyên và là số chẵn)
Ta có: 12.4 + y + 16z = 86 => y + 16z = 38
+ z = 1: y = 22 (loại)
+ z = 2: y = 6 (nhận)
Vậy CTPT của các chất là: C4H6O2
b) A, B đều có nhóm CH3 và phản ứng với NaHCO3 tạo khí và chỉ có B có đồng phân hình học nên cấu tạo của A và B là:
A: CH2=C(CH3)-COOH
B: CH3-CH=CH-COOH
F, H, K có phản ứng với NaHCO3 tạo khí nên F, H, K là các axit.
- G là hợp chất không bền và chuyển hóa ngay thành G’ (G và G’ có cùng công thức phân tử) và khi oxy hóa bằng H2CrO4, hợp chất G’ chuyển hóa thành F nên G’ và F có cùng số nguyên tử C
C: CH3COOCH=CH2
F: CH3COOH
G: CH2=CH-OH
G’: CH3CHO
- H có phản ứng với NaHCO3 tạo khí nên H là axit. Mặt khác, phản ứng của H với bạc nitrat trong amoniac chỉ tạo thành các chất vô cơ nên H là HCOOH
D: HCOOCH2-CH=CH2
H: HCOOH
I: CH2=CH-CH2-OH
- L bị oxi hóa tạo HCOOH nên L là CH3OH
E: CH2=CH-COOCH3
K: CH2=CH-COOH
L: CH3OH
(1) CH2=C(CH3)-COOH (A) + NaHCO3 → CH2=C(CH3)-COONa + H2O + CO2
(2) CH3-CH=CH-COOH (B) + NaHCO3 → CH3-CH=CH-COONa + H2O + CO2
(3) CH3COOCH=CH2 (C) + NaOH → CH3COONa + CH3CHO (G’)
(4) CH3COONa + HCl → CH3COOH (F) + NaCl
(5) HCOOCH2-CH=CH2 (D) + NaOH → HCOONa + CH2=CH-CH2-OH (I)
(6) HCOONa + HCl → HCOOH (H) + NaCl
(7) CH2=CH-COOCH3 (E) + NaOH → CH2=CH-COONa + CH3OH (L)
(8) CH2=CH-COONa + HCl → CH2=CH-COOH (K) + NaCl
(9) CH3CHO + H2CrO4 → CH3COOH + H2CrO3
(10) CH3OH + 2H2CrO4 → HCOOH + 2H2CrO3 + H2O
(11) HCOOH + 2AgNO3 + 4NH3 + H2O → (NH4)2CO3 + 2Ag + 2NH4NO3
(c) Phản ứng polime hóa của A và C:
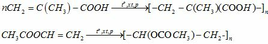
(d)


Gọi công thức phân tử của A, B là C x H y O
Phương trình hoá học:
C x H y O + (x +y/4 -1/2) O 2 → x CO 2 + y/2 H 2 O
n CO 2 = 17,6/44 = 0,4 mol; n H 2 O = 9/18 = 0,5 mol (1)
m C = 0,4.12 = 4,8 gam; m H = 0,5.2 = 1g (2)
Từ (1), (2)
→ x : y : 1 = 4,8/12 : 1/1 : 1,6/16 = 0,4 : 1 : 0,1
Vậy m O = 7,4 - 4,8 - 1,0 = 1,6 (gam)
=> Công thức phân tử của A, B là C 4 H 10 O
Ta có M A , B = 74 (g/mol)
n A , B = 7,4/74 = 0,1 mol
Khi phản ứng với Na có khí bay ra → trong A, B có nhóm OH.
Phương trình hoá học :
C 4 H 9 OH + Na → C 4 H 9 ONa + 1/2 H 2
Vậy số mol có nhóm OH là 2 n H 2 = 2. 0,672/22,4 = 0,06 < n A , B
→ trong A, B có 1 chất không có nhóm OH → Cấu tạo tương ứng là
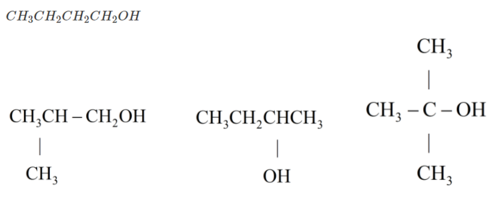
Chất không có nhóm OH :
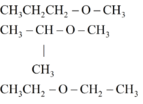

Vì A làm quỳ tím chuyển sang màu đỏ nên A là một axit → Trong phân tử A có nhóm -COOH.
Vậy công thức cấu tạo của A là CH 3 -COOH.

CxHyOz+(x+\(\dfrac{y}{4}-\dfrac{Z}{2}\))O2-to>xCO2+y\2H2O
Theo đề bài ta có : nC = nCO2 = 1,12/22,4 = 0,05(mol) ; nH = 2nH2O=(2.1,35)/18 =0,15(mol)
Ta có : mC + mH = 0,05.12 + 0,15 = 0,75 < 1,15(g)
=> Trong HC có chứa O
=> mO = 1,15-0,75 = 0,4(g) => nO = 0,025(mol)
Đặt CTTQ là CxHyOz
ta có tỉ lệ : x:y:z = nC : nH : nO = 0,05 : 0,15 : 0,025 = 2:6:1
=> CTPT của HCHC là C2H6O

a, - Đốt A thu CO2 và H2O → A chứa C và H, có thể có O.
Ta có: \(n_{CO_2}=\dfrac{6,6}{44}=0,15\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\Rightarrow n_H=0,2.2=0,4\left(mol\right)\)
⇒ mC + mH = 0,15.12 + 0,4.1 = 2,2 (g) < mA
→ A chứa C, H và O.
⇒ mO = 3 - 2,2 = 0,8 (g) \(\Rightarrow n_O=\dfrac{0,8}{16}=0,05\left(mol\right)\)
b, Gọi CTPT của A là CxHyOz.
⇒ x:y:z = 0,15:0,4:0,05 = 3:8:1
→ CTPT của A có dạng (C3H8O)n
\(\Rightarrow n=\dfrac{60}{12.3+1.8+16}=1\)
Vậy: CTPT của A là C3H8O.
c, CTCT: CH3CH2CH2OH
CH3CH(OH)CH3
d, PT: \(CH_3CH_2CH_2OH+Na\rightarrow CH_3CH_2CH_2ONa+\dfrac{1}{2}H_2\)
\(CH_3CH\left(OH\right)CH_3+Na\rightarrow CH_3CH\left(ONa\right)CH_3+\dfrac{1}{2}H_2\)

Chất A chứa C, H, O khi đốt cháy sẽ sinh ra CO 2 và H 2 O . Khi qua bình 1 đựng H 2 SO 4 đặc thì H 2 O bị hấp thụ. Vậy khối lượng H 2 O là 1,8 gam. Qua bình 2 có phản ứng :
Ca OH 2 + CO 2 → CaCO 3 ↓+ H 2 O
Theo phương trình : n CO 2 = n CaCO 3 = 10/100 = 0,1 mol
Vậy khối lượng cacbon có trong 3 gam A là 0,1 x 12 = 1,2 (gam).
Khối lượng hiđro có trong 3 gam A là 0,1 x 2 = 0,2 (gam).
Khối lượng oxi có trong 3 gam A là 3 - 1,2 - 0,2 = 1,6 (gam).
Gọi công thức phân tử của A là C x H y O z
Ta có :
60 gam A → 12x gam C → y g H → 16z gam O
3 gam → 1,2 gam → 0,2 gam → 1,6 gam
x = 1,2x60/36 = 2; y = 60x0,2/3 = 4
z = 1,6x60/48 = 2
→ Công thức phân tử của A là C 2 H 4 O 2