Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi CT của muối halogen là MA2, số mol của muối là 2x (mol)
\(\rightarrow2Mx+4Ax=2,08\left(1\right)\)
- Phần 1: Kết tủa là AgA : 2x (mol)
\(\rightarrow2x\left(108+A\right)1,435\left(g\right)\left(2\right)\)
- Phần 2: Kết tủa là MCO3: x (mol)
\(\rightarrow\left(M+60\right)x=0,985\left(3\right)\)
- Từ (1) , (2) , (3) [coi các ẩn là x,Ax,Mx ] \(\rightarrow x=0,005\left(mol\right)\)
\(Ax=0.1775\rightarrow A=35,5\) . Vậy A là Cl
\(Mx=0,685\rightarrow M=137\) . Vậy M là Ba

Đáp án C
Gọi công thức muối cần tìm là MX2.
Khi cho 150 gam dung dịch X tác dụng với dung dịch Na2CO3 dư có phản ứng:
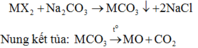
Do đó khí hấp thụ vào dung dịch KOH là CO2.
Vì sau phản ứng trong dung dịch vẫn còn KOH nên sản phẩm tạo thành là K2CO3:
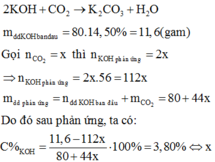 = 0,75
= 0,75

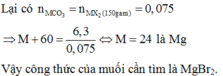

gọi số mol của hỗn hợp muối là \(\begin{cases}X_2CO_3:2x\\XHCO_3:2y_{ }\\XCl:2z\end{cases}\)
gọi số mol HCl : a mol
ptpu : X2CO3 + 2HCl = 2XCl + CO2 + H2O
XHCO3 + HCl = XCl + CO2 + H2O
khí B : CO2 có số mol = 0,4 mol = 2x + 2y (1)
dd A gồm : \(\begin{cases}XCl:2\left(2x+y+z\right)\\HCl_{dư}=a-4x-2y\end{cases}\)
Phần 1 : hh A + AgCl = kết tủa
kết tủa ở đây chính là AgCl => số mol AgCl = 0,48 mol
=> z + \(\frac{a}{2}\)=0,48 => a = (0,48 -z) / 2 (2)
Phần 2 : nKOH = 0,1 = \(\frac{1}{2}\)nHCl dư => a -4x -2y = 0,2 (3)
hốn hợp muối gồm : \(\begin{cases}XCl:2x+y+z\\KCl:0,1\end{cases}\)
m hỗn hợp muối = 29,68 = (2x + y+z) .(X+35,5) = 29,68 -39.0,1 = 22,23 (4)
từ (2) thay vào (3) => (2x + y +z) = 0,38 (5)
từ (5) thay vào (4) ta tìm được X = 23 => X là Na
Đến đây bạn tự giải câu b nhé

nAg=0,01 mol
NaX+AgN03------->NaN03+AgX,áp dụng bảo toàn nguyên tố Ag,nAg sau=nAg truoc
0,01--------------------------------0,01
MNaX=1,03/0,01=103------------------->X=80------->Br

\(RX_2+2AgNO_3\rightarrow2AgX+R\left(NO_3\right)_2\)
\(Fe+RX_2\rightarrow R+FeCl_2\)
\(n_{AgX}=\frac{5,74}{108+M_X}\left(mol\right)\)
\(n_{Fe}=n_R=\frac{2,87}{108+M_X}\left(mol\right)\)
\(M_R.\frac{2,87}{108+M_X}-56.\frac{1,87}{108+M_X}=0,16\)
\(M_R.2,87-160,72=17,28+0,16M_X\)
\(\Rightarrow M_X=35,5M_R=64\)
Vậy X là Cl , R là Cu
Công thức hóa học là CuCl2

