Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1)
CTHH MXn
\(n_{X_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
=> \(n_{MX_n}=\dfrac{0,08}{n}\left(mol\right)\)
=> \(n_{AgX}=0,08\left(mol\right)\)
=> \(M_{AgX}=\dfrac{11,48}{0,08}=143,5\left(g/mol\right)\) => MX = 35,5 (g/mol)
=> X là Cl
2)
\(n_{MCl_n}=\dfrac{0,08}{n}\left(mol\right)\)
\(n_M=\dfrac{0,96}{M_M}\left(mol\right)\)
=> \(\dfrac{0,08}{n}=\dfrac{0,96}{M_M}\)
=> MM = 12n (g/mol)
Xét n = 1 => Loại
Xét n = 2 => MM = 24 (g/mol) => M là Mg
Xét n = 3 => Loại
Vậy M là Mg
M' có hóa trị II
\(n_{O_2}=\dfrac{4,162-0,96-2,242}{32}=0,03\left(mol\right)\)
PTHH: 2Mg + O2 --to--> 2MgO
0,04-->0,02------>0,04
2M' + O2 --to--> 2M'O
0,02<-0,01------>0,02
=> MM' = \(\dfrac{2,242}{0,02}=112\left(g/mol\right)\)
a) \(\left\{{}\begin{matrix}\%n_M=\dfrac{0,04}{0,04+0,02}.100\%=66,67\%\\\%n_{M^{\cdot}}=100\%-66,67\%=33,33\%\end{matrix}\right.\)
b) \(\dfrac{M_M}{M_{M^{\cdot}}}=\dfrac{24}{112}=\dfrac{3}{14}\)
c) \(n_O=0,06\left(mol\right)\)
=> \(n_{H_2O}=0,06\left(mol\right)\)
=> \(n_{H_2SO_4}=0,06\left(mol\right)\)
=> \(C_{M\left(H_2SO_4\right)}=\dfrac{0,06}{0,5}=0,12M\)

Điện phân 125 ml dung dịch X có 6,4 gam kim loại ở catot
Suy ra :
Điện phân 250 ml dung dịch X có \(\dfrac{250.6,4}{125} = 12,8\) gam kim loại ở catot
\(\Rightarrow m_{halogenua} = 27 - 12,8 = 14,2(gam)\\ \Rightarrow m_{Ag(trong\ kết\ tua)} = 57,4 - 14,2 = 43,2\\ \Rightarrow n_{Ag} = \dfrac{43,2}{108} = 0,4(mol)\)
CTHH của kết tủa : AgX
\(\Rightarrow M_{AgX} = 108 + X = \dfrac{57,4}{0,4} = 143,5 \\ \Rightarrow X = 35,5(Cl)\)
X: RCln
\(n_{Cl} = 0,4 \Rightarrow n_{muối} = \dfrac{0,4}{n}(mol)\\ \Rightarrow M_{muối} = R + 35,5n = \dfrac{27}{\dfrac{0,4}{n}} = 67,5n\\ \Rightarrow R = 32n\)
Với n = 1 thì R = 64(Cu)
Vậy muối là CuCl2

Đáp án C
Gọi công thức muối cần tìm là MX2.
Khi cho 150 gam dung dịch X tác dụng với dung dịch Na2CO3 dư có phản ứng:
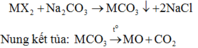
Do đó khí hấp thụ vào dung dịch KOH là CO2.
Vì sau phản ứng trong dung dịch vẫn còn KOH nên sản phẩm tạo thành là K2CO3:
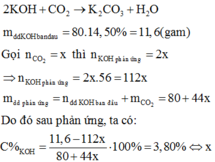 = 0,75
= 0,75

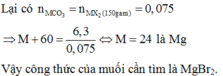

a, PTHH:
\(A+2HCl\rightarrow ACl_2+H_2\left(1\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\left(2\right)\)
\(AlCl_3+4NaOH\rightarrow NaAlO_2+3NaCl+2H_2O\)
b, Ta có \(n_{AlCl_3}=n_{NaAlO_2}=\dfrac{2,7}{82}=0,03\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Al}=n_{AlCl_3}=0,03\left(mol\right)\\n_{H_2\left(2\right)}=\dfrac{3}{2}n_{AlCl_3}=0,045\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Al}=27.0,03=0,81\left(g\right)\\n_A=n_{H_2\left(1\right)}=\dfrac{1,68}{22,4}-n_{H_2\left(2\right)}=0,03\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_A=2,49-0,81=1,68\left(g\right)\\n_A=0,03\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow M_A=\dfrac{1,68}{0,03}=56\left(g/mol\right)\Rightarrow A\) là \(Fe\)
c, \(m_{\text{muối}}=m_{FeCl_2}+m_{AlCl_3}\)
\(=127.n_{Fe}+133,5.n_{Al}\)
\(=127.0,03+133,5.0,03=7,815\left(g\right)\)

gọi số mol của hỗn hợp muối là \(\begin{cases}X_2CO_3:2x\\XHCO_3:2y_{ }\\XCl:2z\end{cases}\)
gọi số mol HCl : a mol
ptpu : X2CO3 + 2HCl = 2XCl + CO2 + H2O
XHCO3 + HCl = XCl + CO2 + H2O
khí B : CO2 có số mol = 0,4 mol = 2x + 2y (1)
dd A gồm : \(\begin{cases}XCl:2\left(2x+y+z\right)\\HCl_{dư}=a-4x-2y\end{cases}\)
Phần 1 : hh A + AgCl = kết tủa
kết tủa ở đây chính là AgCl => số mol AgCl = 0,48 mol
=> z + \(\frac{a}{2}\)=0,48 => a = (0,48 -z) / 2 (2)
Phần 2 : nKOH = 0,1 = \(\frac{1}{2}\)nHCl dư => a -4x -2y = 0,2 (3)
hốn hợp muối gồm : \(\begin{cases}XCl:2x+y+z\\KCl:0,1\end{cases}\)
m hỗn hợp muối = 29,68 = (2x + y+z) .(X+35,5) = 29,68 -39.0,1 = 22,23 (4)
từ (2) thay vào (3) => (2x + y +z) = 0,38 (5)
từ (5) thay vào (4) ta tìm được X = 23 => X là Na
Đến đây bạn tự giải câu b nhé

