Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A.
n Na 2 CO 3 = x; n NaHCO 3 = y; n CO 2 = 0,2 mol
Phương trình hóa học :
Na 2 CO 3 + 2HCl → 2NaCl + H 2 O + CO 2
NaHCO 3 + HCl → NaCl + CO 2 + H 2 O
Ta có hệ phương trình
x + y = 0,2
106x + 84y = 19
=> x = y = 0,1
m Na 2 CO 3 = 10,6g; m NaHCO 3 = 8,4g

\(Na_2CO_3+2HCl\rightarrow2NaCl+H_2O+CO_2\)
\(x\) 2x 2x x x
\(NaHCO_3+HCl\rightarrow NaCl+H_2O+CO_2\)
\(y\) y y y y
Ta có hệ:
\(\left\{{}\begin{matrix}106x+84y=19\\x+y=\dfrac{4,48}{22,4}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
\(m_{Na_2CO_3}=0,1\cdot106=10,6g\)
\(m_{NaHCO_3}=0,1\cdot84=8,4g\)
\(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2+H_2O\\ NaHCO_3+HCl\rightarrow NaCl+CO_2+H_2O\\ Đặt:n_{Na_2CO_3}=a\left(mol\right);n_{NaHCO_3}=b\left(mol\right)\left(a,b>0\right)\\ m_{hh.muối.ban.đầu}=19\left(g\right)\\ \Leftrightarrow106a+84b=19\left(1\right)\\ Mặt.khác:V_{CO_2\left(tổng\right)}=22,4a+22,4b=4,48\left(2\right)\\ \left(1\right),\left(2\right)\Rightarrow\left\{{}\begin{matrix}106a+84b=19\\22,4a+22,4b=4,48\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\\ \Rightarrow m_{NaHCO_3}=84.0,1=8,4\left(g\right)\\ m_{Na_2CO_3}=106.0,1=10,6\left(g\right)\)

\(n_{Fe} = a(mol) ; n_{Mg} = b(mol)\\ \Rightarrow 56a + 24b = 16,8 - 6,4 = 10,4(1)\\ Fe + 2HCl \to FeCl_2 + H_2\\ Mg + 2HCl \to MgCl_2 + H_2\\ n_{H_2} = a + b = \dfrac{6,72}{22,4} = 0,3(2)\)
Từ (1)(2) suy ra: a = 0,1 ; b = 0,2
Vậy :
\(\%m_{Fe} = \dfrac{0,1.56}{16,8}.100\% = 33,33\%\\ \%m_{Mg} = \dfrac{0,2.24}{16,8}.100\% = 28,57\%\\ \%m_{Cu} = 100\% - 33,33\% - 28,57\% = 38,1\%\)

Bài 1 :
Gọi
\(n_{Fe} = a(mol) ; n_{Zn} = b(mol)\\ Fe + 2HCl \to FeCl_2 + H_2\\ Zn + 2HCl \to ZnCl_2 + H_2\\ \)
Ta có :
\(\hept{\begin{cases}n_{H_2}=a+b=\frac{3,36}{22,4}=0,15\left(mol\right)\\m_{muoi}=127a+136b=19,5\left(gam\right)\end{cases}}\)
\(\Rightarrow\hept{\begin{cases}a=0,1\\b=0,05\end{cases}}\)\(\Rightarrow\hept{\begin{cases}m_{Fe}=0,1.56=5,6\left(gam\right)\\m_{Zn}=0,05.65=3,25\left(gam\right)\end{cases}}\)
Bài 2 :
\(\hept{\begin{cases}n_{BaCO_3}=a\left(mol\right)\\n_{BaSO_3}=b\left(mol\right)\end{cases}}\)
\(BaCO_3 + 2HCl \to BaCl_2 + CO_2 + H_2O\\ BaSO_3 + 2HCl \to BaCl_2 + SO_2 + H_2O\)
Ta có :
\(\hept{\begin{cases}m_{hh}=197a+217b=20,5\left(gam\right)\\n_{khí}=n_{CO_2}+n_{SO_2}=a+b=\frac{2,24}{22,4}=0,1\left(mol\right)\end{cases}}\)
Suy ra: a = 0,06 ; b = 0,04
\(\%m_{BaCO_3} = \dfrac{0,06.197}{20,5}.100\% =57,66\%\\ \%m_{BaSO_3} = 100\%- 57,66\%=42,34\%\)

Theo bảo toàn e + đề bài ta có :
\(3x=0,15.2;2y=0,3\)
Với x, y lần lượt là số mol của Al và Cu)
=> x = 0,1 ; y = 0,15 ; => m = 0,1.27 + 0,15.64 = 12,3
Vì Cu đứng sau H trong dãy hoạt động nên ko đẩy đc H khỏi axit nên Cu ko tác tác dụng với HCl nhưng Al thì có(vậy h2 thoát ra là của Al pư)
nH2=3.36/22.4=0.15mol
PTHH: 2Al + 6HCl ---> 2AlCl3 + 3H2
0.1 0.15
m=n*M=>0.1*27=2.7g (1)
Ta biết Al,Fe,Cr thụ động với h2so4 và HNO3 đặc nguội nên trong X chỉ có Cu pư:
nNO2=V*22.4=>6.72/22.4=0.3 mol
PTHH: Cu +4 HNO3 -> Cu(NO3)2 + 2NO2 + 2H2O
0.15 0.3
mCu=0.15*64=9.6g (2)
Từ (1),(2) =>m X =2.7+9.6=12.3g
OH dear,giải xong mệt quá zzzzzzz, chúc em học tốt

$n_{H_2} = \dfrac{1,792}{22,4} = 0,08(mol)$
$n_{HCl} = 0,2(mol)$
$2Na + 2H_2O \to 2NaOH + H_2$
$Na_2O + H_2O \to 2NaOH$
$NaOH + HCl \to NaCl + H_2O$
Theo PTHH :
$n_{Na} = 2n_{H_2} = 0,16(mol)$
$2n_{Na_2O} + n_{Na} = n_{NaOH} = n_{HCl} = 0,2$
$\Rightarrow n_{Na_2O} = 0,02(mol)$
$\%m_{Na} = \dfrac{0,16.23}{5}.100\% = 73,6\%$
$\%m_{Na_2O} = \dfrac{0,02.62}{5}.100\% = 24,8\%$

- Đặt \(\left\{{}\begin{matrix}n_{C_2H_5OH}=a\left(mol\right)\\n_{CH_3COOH}=b\left(mol\right)\end{matrix}\right.\) \(\Rightarrow46a+60b=33,2\left(1\right)\)
\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
a) \(2C_2H_5OH+2Na\rightarrow2C_2H_5ONa+H_2\)
2 2 1 (mol)
a a a/2 (mol)
\(2CH_3COOH+2Na\rightarrow2CH_3COONa+H_2\)
2 2 1 (mol)
b b b/2 (mol)
Từ hai PTHH trên ta có: \(\dfrac{a}{2}+\dfrac{b}{2}=n_{H_2}=0,3\Rightarrow a+b=0,6\left(2\right)\)
(1), (2) ta có hệ phương trình: \(\left\{{}\begin{matrix}46a+60b=33,2\\a+b=0,6\end{matrix}\right.\)
Giải ra ta được: \(a=0,2\left(mol\right);b=0,4\left(mol\right)\)
b) \(m_{C_2H_5OH}=n.M=0,2\times46=9,2\left(g\right)\)
\(m_{CH_3COOH}=n.M=0,4\times60=24\left(g\right)\)
c) \(m_{C_2H_5ONa}=n.M=0,2\times68=13,6\left(g\right)\)
\(m_{CH_3COONa}=n.M=0,4\times82=32,8\left(g\right)\)

a) Các phương trình phản ứng:
C2H4 + Br2 → C2H4Br2
C2H2 + 2Br2 → C2H2Br4
C2H2 + Ag2O → C2Ag2 + H2O
Hay
C2H2 + 2AgNO3 + 2NH3 → C2Ag2 + 2NH4NO3
b) Gọi a, b, c lần lượt là số mol của CH4, C2H4, C2H2 trong 4,3gam hỗn hợp T.
– Số mol Br2 = 0,15 (mol); số mol kết tủa = số mol C2H2 = 0,075 (mol); số mol T = 0,3 (mol). Do đó nT = 4nC2H2
– Ta có hệ phương trình:
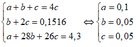
– Suy ra % thể tích mỗi khí trong T:
%VCH4 = 50%; %VC2H2 = %VC2H4 = 25%
\(n_{CO_2}=\dfrac{V_{CO_2}}{22,4}=\dfrac{6,72}{22,4}=0,3mol\)
Gọi \(n_{Na_2CO_3}\) là x \(\Rightarrow m_{Na_2CO_3}=106x\)
\(n_{NaHCO_3}\) là y \(\Rightarrow m_{NaHCO_3}=84y\)
\(Na_2CO_3+HCl\rightarrow2NaCl+H_2O+CO_2\)
x x ( mol )
\(NaHCO_3+HCl\rightarrow NaCl+H_2O+CO_2\)
y y ( mol )
Ta có:
\(\left\{{}\begin{matrix}106x+84y=29,6\\x+y=0,3\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
\(\Rightarrow m_{Na_2CO_3}=106.0,2=21,2g\)
\(\Rightarrow m_{NaHCO_3}=84.0,1=8,4g\)
=> Chọn B