Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a.b.c.\(n_{Zn}=\dfrac{m}{M}=\dfrac{13}{65}=0,2mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2 0,2 0,2 ( mol )
\(m_{ZnCl_2}=n.M=0,2.136=27,2g\)
\(V_{H_2}=n.22,4=0,2.22,4=4,48l\)
d.\(n_{CuO}=\dfrac{m}{M}=\dfrac{32}{80}=0,4mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,4 > 0,2 ( mol )
0,2 0,2 0,2 ( mol )
\(m_{chất.rắn}=m_{CuO\left(dư\right)}+m_{Cu}=0,2.80+0,2.64=16+12,8=28,8g\)
\(\%m_{CuO}=\dfrac{16}{28,8}.100=55,55\%\)
\(\%m_{Cu}=100\%-55,55\%=44,45\%\)

a) PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
b) Ta có: \(n_{Zn}=\dfrac{26}{65}=0,4\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=0,8mol\\n_{H_2}=0,4mol\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{HCl}=0,8\cdot36,5=29,2\left(g\right)\\V_{H_2}=0,4\cdot22,4=8,96\left(l\right)\end{matrix}\right.\)

a) Zn + 2HCl →ZnCl2 + H2
b) nZn = 6,5/65 = 0,1 mol . Theo tỉ lệ pư => nH2 = nZn = nZnCl2 =0,1 mol <=> VH2(đktc) = 0,1.22,4 = 2,24 lít.
c) mZnCl2 = 0,1 . 136 = 13,6 gam
d) nHCl =2nZn = 0,2 mol => mHCl = 0,2.36,5= 7,3 gam
Cách 2: áp dụng định luật BTKL => mHCl = mZnCl2 + mH2 - mZn
<=> mHCl = 13,6 + 0,1.2 - 6,5 = 7,3 gam

\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(n_{Zn}=\dfrac{13}{65}=0.2\left(mol\right)\)
\(\Leftrightarrow n_{ZnCl_2}=0.2\left(mol\right)\)
\(m_{ZnCl_2}=0.2\cdot136=27.2\left(g\right)\)

\(n_{Zn}=\dfrac{3,25}{65}=0,05mol\)
a)\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,05 0,1 0,05 0,05
b)\(m_{ZnCl_2}=0,05\cdot136=6,8g\)
c)\(V_{H_2}=0,05\cdot22,4=1,12l\)

a) PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
b+c) Áp dụng Định luật bảo toàn khối lượng:
\(m_{Zn}+m_{HCl}=m_{ZnCl_2}+m_{H_2}\)
\(\Rightarrow m_{ZnCl_2}=m_{Zn}+m_{HCl}-m_{H_2}=6,5+7,3-1=12,8\left(g\right)\)
Có 3 lọ mất nhãn đựng 3 dung dịch không màu NaCl H2SO4 K2SO4 trình bày phương pháp hóa học để nhận ra các chất trên. Viết phương trình phản ứng.

\(n_{HCl}=0,25.2=0,5\left(mol\right)\\ a,PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ b,n_{Zn}=n_{H_2}=n_{ZnCl_2}=\dfrac{0,5}{2}=0,25\left(mol\right)\\ m_{Zn}=0,25.65=16,25\left(g\right)\\ c,V_{H_2\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\)
Không biết đúng không nữa;-;;;
a) PTHH: Zn + 2HCl -> ZnCl2 + H2
b) HCl=250ml=0,25l
n2HCl= V/22,4= 0,5/22,4= 0,02(mol)
Zn + 2HCl -> ZnCl2 + H2
1 2 1 1
0,01 <-0,5--------------> 0,01
mZn= n.M= 0,01.65= 0,65(gam)
c) VH2=n . 22,4= 0,01 . 22,4= 0,224(l)
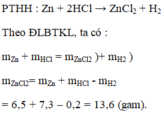
a) PTHH: Zn + 2HCl ===> ZnCl2 + H2
b) Số mol kẽm: nZn = \(\frac{26}{65}=0,4\left(mol\right)\)
Theo phương trình, nZnCl2 = nZn = 0,4 (mol)
=> Khối lượng ZnCl2 thu được: mZnCl2 = 0,4 x 136 = 54,4 gam
câu c) tính thể tích hiđro sinh ra ở ĐKTC
Giúp mk