Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Na+ H2O ------> NaOH+ 1/2H2
0.1.....0.1...............0.1.........0.05
nNaOH=0.1 mol
mH2O=47.8*1=47.8 g (m=D*V)
mdd=47.8+2.3=50.1 g
=>C%NaOH=\(\dfrac{40\cdot0.1\cdot100}{50.1}\)=7.98%
Sau phản ứng có khí H2 thoát ra khỏi dung dịch nên khối lượng dung dịch được tính như sau:
mdd = mNa + mH2O -mH2


C % N a O H = m N a O H m dd .100 % = 0,1.40 100 .100 % = 4 % .
Đáp án B

\(n_{K_2O}=\dfrac{11,28}{94}=0,12\left(mol\right)\)
PTHH :
\(K_2O+H_2O\rightarrow2KOH\)
0,12 0,24
\(m_{KOH}=0,24.56=13,44\left(g\right)\)
\(m_{ddKOH}=11,28+100=111,28\left(g\right)\)
\(C\%=\dfrac{13,44}{111,28}.100\%\approx12,08\%\)

\(n_{Na}=\dfrac{2.3}{23}=0.1\left(mol\right)\)
\(n_{HCl}=0.4\cdot2=0.8\left(mol\right)\)
\(NaOH+HCl\rightarrow NaCl+H_2O\)
\(0.8..............0.8\)
\(2Na+2H_2O\rightarrow2NaOH+H_{_{ }2}\)
\(0.1........................0.1\)
\(n_{NaOH}=0.1< 0.8\)
Đề nhầm lãn !

a) - Dung dịch A chứa chất tan NaOH
mddNaOH= 200(g)
=> C%ddNaOH= (4/200).100=2%
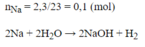

\(n_{Na}=\dfrac{2,3}{23}=0,1\left(mol\right)\)
Pt : \(2Na+2H_2O\rightarrow2NaOH+H_2|\)
2 2 2 1
0,2 0,2
\(n_{NaOH}=\dfrac{0,2.2}{2}=0,2\left(mol\right)\)
⇒ \(m_{NaOH}=0,2.40=8\left(g\right)\)
\(m_{ddspu}=2,3+100=102,3\left(g\right)\)
\(C_{ddNaOH}=\dfrac{8.100}{102,3}=7,82\)0/0
Chúc bạn học tốt