Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

2 M + 2 n H C l → 2 M C l n + n H 2
2/n <…...2 ………..mol
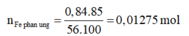
Vậy
⇒ n H 2 = n F e p ư = 0,01275 mol
⇒ V H 2 = 0,01275.22,4 = 0,2856 mol
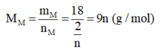
Nếu n = 1 thì M M = 9 → loại
Nếu n = 2 thì M M = 18 → loại
Nếu n = 3 thì M M = 27 → M là kim loại Al
⇒ Chọn C.

Khối lượng dung dịch HCl :
m dd = V x D = 100 x 1,05 = 105 (gam)
n HCl = 0,1 x 0,1 = 0,01 (mol)
Gọi hoá trị của kim loại M là n
Phương trình hoá học của phản ứng :
2M + 2nHCl → 2 MCl n + n H 2 (1)
Áp dụng định luật bảo toàn khối lượng
m + m HCl = m muối + m H 2
m = 105,11 + 0,01/2 x 2 - 105 = 0,12g
Theo phương trình hóa học (1) :
n M = 0,01/n mol → 0,01/n x M = 0,12 → M = 12n
Kẻ bảng
| n | 1 | 2 | 3 |
| M | 12 | 24 | 36 |
| loại | nhận | loại |
Vậy kim loại M là Mg.

1) Gọi công thức của oxit là AO. Số mol HCl là 0,4.1=0,4 (mol).
AO (0,2 mol) + 2HCl (0,4 mol) \(\rightarrow\) ACl2 + H2\(\uparrow\).
Phân tử khối của oxit là 8,0/0,2=40 (g/mol).
Vậy A là magie (Mg) và công thức hóa học của oxit là MgO.
2) Số mol MgCO3 và H2SO4 lần lượt là 8,4/84=0,1 (mol) và 0,5.1=0,5 (mol).
Các chất tan trong dung dịch sau phản ứng gồm MgSO4 (0,1 mol) và H2SO4 dư (0,4 mol) có nồng độ mol lần lượt là 0,1/0,5=0,2 (M) và 0,4/0,5=0,8 (M).
\(1,n_{HCl}=0,4.1=0,4\left(mol\right)\\ PTHH:AO+2HCl\rightarrow ACl_2+H_2O\\ Mol:0,2\leftarrow0,4\\ M_{AO}=\dfrac{8}{0,2}=40\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow A+16=40\\ \Leftrightarrow A=24\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow A.là.Mg\\ CTHH:MgO\)
\(2,n_{H_2SO_4}=1.0,5=0,5\left(mol\right)\\ PTHH:MgCO_3+H_2SO_4\rightarrow MgSO_4+CO_2\uparrow+H_2O\\ Mol:0,5\leftarrow0,5\rightarrow0,5\\ C_{M\left(MgSO_4\right)}=\dfrac{0,5}{0,5}=1M\)

Oxit kim loại M : M2O3
$M_2O_3 + 6HCl \to 2MCl_3 + 3H_2O$
2n M2O3 = n MCl3
<=> 2.40,8/(2M + 16.3) = 106,68/(M + 35,5.3)
<=> M = 27(Al)
Vậy kim loại M là Al

\(n_{H_2}=\dfrac{5,04}{22,4}=0,225\left(mol\right)\)
\(2X+2NaOH+2H_2O->2NaXO_2+3H_2\)
0,15<---------------------------------------0,225
=> \(M_X=\dfrac{7,8}{0,15}=52\left(g/mol\right)\)
=> X là Cr(Crom)
Cho 7,2 gam kim loại X có hóa trị II tác dụng vừa đủ với dung dịch H2SO4 loãng. Cô cạn dung dịch sau phản ứng thu được 36 gam muối. Hãy cho biết tên và kí hiệu hóa học của X.

Đáp án C.
Gọi nguyên tử khối của kim loại M cũng là M, có hóa trị là x, ta có:
n M = 18/M (mol); n HCl = 0,8 x 2,5 = 2 mol
Phương trình hóa học
2M + 2xHCl → 2 MCl x + x H 2
Có: 18/M x 2x = 4 → M = 9x
Xét bảng sau
| X | I | II | III |
| M | 9 | 18 | 27 |
Chỉ có kim loại hóa trị III ứng với M = 27 là phù hợp, kim loại M là nhôm (Al)

Kim loại cần tìm đặt là A.
=> CTHH oxit: A2O3
\(A_2O_3+H_2SO_4\rightarrow A_2\left(SO_4\right)_3+3H_2O\\ m_{ddsau}=10,2+331,8=342\left(g\right)\\ m_{A_2\left(SO_4\right)_3}=\dfrac{342}{100}.10=34,2\left(g\right)\\ n_{oxit}=\dfrac{34,2-10,2}{96.3-16.3}=0,1\left(mol\right)\\ M_{A_2O_3}=\dfrac{10,2}{0,1}=102\left(\dfrac{g}{mol}\right)=2M_A+48\left(\dfrac{g}{mol}\right)\\ \Rightarrow M_A=\dfrac{102-48}{2}=27\left(\dfrac{g}{mol}\right)\\ \Rightarrow A:Nhôm\left(Al=27\right)\\ \Rightarrow CTHH.oxit:Al_2O_3\)
.
.