Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

Cho hỗn hợp X vào dung dịch HCl lấy dư:
PTHH: Al2O3 + 6HCl → 2AlCl3 + 3H2O
MgO + 2HCl → MgCl2 + H2O
Fe + 2HCl → FeCl2 + H2
Dung dịch Y gồm: AlCl3, MgCl2, FeCl2, HCl dư
Khí Z là H2
Chất rắn A là Cu
Cho A tác dụng với H2SO4 đặc nóng.
PTHH: Cu + 2H2SO4(đặc, nóng) → CuSO4 + SO2 + 2H2O
Khí B là SO2
Cho B vào nước vôi trong lấy dư
PTHH: SO2 + Ca(OH)2 → CaSO3 + H2O
Kết tủa D là CaSO3
Cho dung dịch NaOH vào Y tới khi kết tủa lớn nhất thì dừng lại.
PTHH: NaOH + HCl → NaCl + H2O
3NaOH + AlCl3 → Al(OH)3 + 3NaCl
2NaOH + MgCl2 → Mg(OH)2 + 2NaCl
2NaOH + FeCl2 → Fe(OH)2 + 2NaCl
Chất rắn E là: Al(OH)3, Mg(OH)2, Fe(OH)2
Nung E trong không khí
Chất rắn G là Al2O3, MgO, Fe2O3

a) A chứa 3 muối là Mg(NO3)2, Al(NO3)3, NaNO3
PTHH:
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\)
\(Mg+2Fe\left(NO_3\right)_3\rightarrow Mg\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\)
\(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\)
\(Mg+Fe\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Fe\)
\(Mg+Zn\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Zn\)
B chứa các kim loại: Ag, Cu, Fe, Zn
b)
B chứa 4 kim loại: Ag, Cu, Fe, Zn
PTHH:
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\)
\(Mg+2Fe\left(NO_3\right)_3\rightarrow Mg\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\)
\(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\)
\(Mg+Fe\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Fe\)
\(Mg+Zn\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Zn\)
=> A chứa các muối: NaNO3, Mg(NO3)2, Al(NO3)3 và có thể có Zn(NO3)2
a) A chứa 3 muối là Mg(NO3)2, Al(NO3)3, NaNO3
PTHH:
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\)
\(Mg+2Fe\left(NO_3\right)_3\rightarrow Mg\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\)
\(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\)
\(Mg+Fe\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Fe\)
\(Mg+Zn\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Zn\)
\(3Mg+2Al\left(NO_3\right)_3\rightarrow3Mg\left(NO_3\right)_2+2Al\)
B chứa các kim loại: Ag, Cu, Fe, Zn và có thể có Al
b)
B chứa 4 kim loại: Ag, Cu, Fe, Zn
PTHH:
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\)
\(Mg+2Fe\left(NO_3\right)_3\rightarrow Mg\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\)
\(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\)
\(Mg+Fe\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Fe\)
\(Mg+Zn\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Zn\)
=> A chứa các muối: NaNO3, Mg(NO3)2, Al(NO3)3 và có thể có Zn(NO3)2

Fe3O4+4CO=>3Fe+ 4CO2
CuO+CO=>Cu+CO2
Cr B gồm Fe Cu
HH khí D gồm CO dư và CO2
CO2 +Ca(OH)2=>CaCO3+H2O
p/100 mol<= p/100 mol
2CO2+Ca(OH)2 => Ca(HCO3)2
p/50 mol
Ca(HCO3)2+ 2NaOH=>CaCO3+ Na2CO3+2H2O
p/100 mol p/100 mol
Tổng nCO2=0,03p mol=nCO
=>BT klg
=>m+mCO=mCO2+mB=>mB=m+0,84p-1,32p=m-0,48p
c) hh B Fe+Cu
TH1: Fe hết Cu chưa pứ cr E gồm Ag Cu
dd Z gồm Fe(NO3)2
Fe+2Ag+ =>Fe2+ +2Ag
TH2:Cu pứ 1p cr E gồm Cu và Ag
Fe+2Ag+ => Fe2+ +2Ag
Cu+2Ag+ =>Cu2+ +2Ag
Dd Z gồm 2 muối của Fe2+ và Cu2+

a)
2Al + 6HCl → 2AlCl3 + 3H2↑
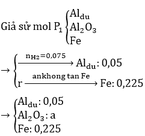
Pt: 2Al + 6H2SO4 → Al2(SO4)3 + 3SO2↑ + 6H2O
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Giả sử P2 = kP1
=> a=0.1
=> m = 128,8g
b)
2yAl + 3FexOy → yAl2O3 + 3xFe
0,1 0,225
=> 0,225y = 0,3x => 3y = 4x
=> Fe3O4







có: mphần 1= mphần 2= 0,75( g)
phần 1
2Al+ 6HCl\(\rightarrow\) 2AlCl3+ 3H2\(\uparrow\)
..a....................................1,5a.. mol
Fe+ 2HCl\(\rightarrow\) FeCl2+ H2\(\uparrow\)
.b...............................b.... mol
0,2g chất rắn chính là khối lượng Cu có trong phần 1
\(\Rightarrow\) mCu trong X= 0,2. 2= 0,4( g)
gọi a, b lần lượt là số mol của Al và Fe có trong phần 1
có: nH2= \(\frac{0,448}{22,4}\)= 0,02( mol)
mAl và Fe trong phần 1= 0,75- 0,2= 0,55( g)
ta có hệ pt:
\(\left\{{}\begin{matrix}27a+56b=0,55\\1,5a+b=0,02\end{matrix}\right.\)
\(\Rightarrow\) \(\left\{{}\begin{matrix}a=0,01\\b=0,005\end{matrix}\right.\)
\(\Rightarrow\) mAl trong X= 0,01. 27. 2= 0,54( g)
mFe trong X= 0,005. 56. 2= 0,56( g)
phần 2
có: nAgNO3= 0,08. 0,4= 0,032( g)
nCu(NO3)2= 0,5. 0,4= 0,2( mol)
Al+ 3AgNO3\(\rightarrow\) Al( NO3)3+ 3Ag (I)
Fe+ 2AgNO3\(\rightarrow\) Fe( NO3)2+ 2Ag (II)
Fe+ Cu( NO3)2\(\rightarrow\) Fe( NO3)2+ Cu (III)
theo ptpu(I) có: nAgNO3= 3nAl= 0,03( mol)
theo giả thiết: nAgNO3= 0,032( mol)
\(\Rightarrow\) AgNO3 dư tiếp tục phản ứng với Fe
\(\Rightarrow\) nAgNO3 pt(II)= 0,032- 0,03= 0,002( mol)
theo ptpu(II) có: nFe= \(\frac{1}{2}\)nAgNO3= 0,001( mol)
\(\Rightarrow\) nFe pt(III)= 0,005- 0,001= 0,004( mol)
theo ptpu(III) có: nCu(NO3)2= nFe= 0,004( mol)
theo giả thiết: nCu(NO3)2= 0,2( mol)
\(\Rightarrow\) Cu(NO3)2 còn dư; chất rắn A gồm Cu và Ag
theo ptpu(I) và(II) có: nAg= nAgNO3= 0,032( mol)
\(\Rightarrow\) mAg= 0,032. 108= 3,456( g)
theo ptpu(III) có: nCu= nFe= 0,004( mol)
\(\Rightarrow\) mCu= 0,004. 64+ 0,2= 0,456( g)
dung dịch B sau phản ứng chứa Al( NO3)3; Fe( NO3)2 và Cu( NO3)2 dư
theo ptpu(I) có: nAl(NO3)3= nAl= 0,01( mol)
theo ptpu(II) và(III) có: nFe(NO3)2= nFe= 0,005( mol)
có: nCu(NO3)2 dư= 0,2- 0,004= 0,196( mol)
\(\Rightarrow\) CM Al(NO3)3= \(\frac{0,01}{0,4}\)= 0,025M
CM Fe(NO3)2= \(\frac{0,005}{0,4}\)= 0,0125M
CM Cu(NO3)2= \(\frac{0,196}{0,4}\)= 0,49M
cảm ơn bạn