Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Về bản chất, phản ứng oxi hóa – khử là phản ứng xảy ra đồng thời quá trình nhường và quá trình nhận electron.
- Dấu hiệu để nhận ra loại phản ứng oxi hóa – khử là có sự thay đổi số oxi của các nguyên tử.
- Các bước lập phương trình hóa học của phản ứng oxi hóa – khử:
Bước 1: Xác định các nguyên tử có sự thay đổi số oxi hóa, từ đó xác định chất oxi hóa, chất khử
Nguyên tử Fe và C có sự thay đổi số oxi hóa, Fe là chất oxi hóa, C là chất khử
Bước 2: Biểu diễn quá trình oxi hóa, quá trình khử
Fe+3 + 3e → Fe0
C+2 → C+4 + 2e
Bước 3: Tìm hệ số thích hợp cho chất khử và chất oxi hóa dựa trên nguyên tắc tổng electron nhường bằng tổng electron nhận.
2x /Fe+3 + 3e → Fe0
3x /C+2 → C+4 + 2e
Bước 4: Đặt hệ số của chất oxi hóa và chất khử vào sơ đồ phản ứng.
Fe2O3+ 3CO \(\xrightarrow[]{t^oC}\) 2Fe + 3CO2
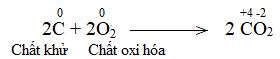
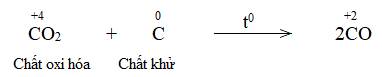
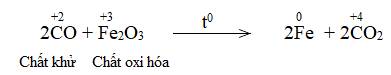
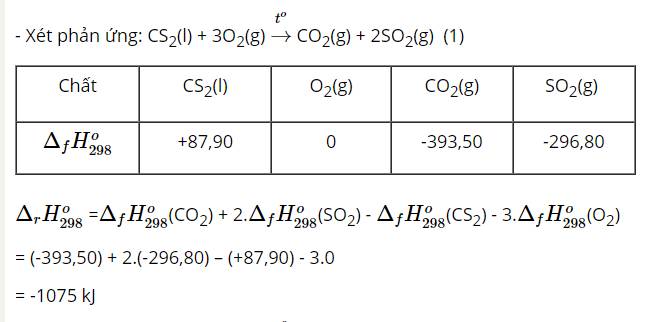

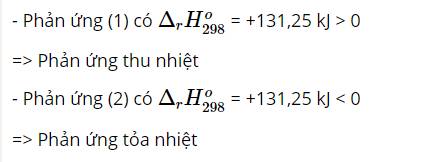

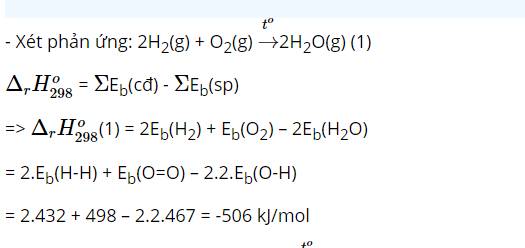

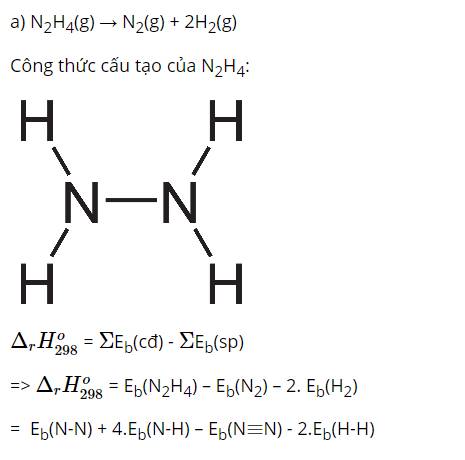
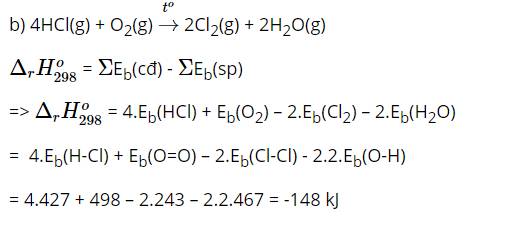

Các phản ứng oxi hóa – khử là: a; b; c và d.
a)
* Fe2O3 + CO \(\underrightarrow{t^o}\) FeO + CO2
Bước 1:
Bước 2:
Bước 3:
Bước 4:
Fe2O3 + CO \(\underrightarrow{t^o}\) 2FeO + CO2
Fe2O3 là chất oxi hóa.
CO là chất khử.
* FeO + CO \(\underrightarrow{t^o}\) Fe + CO2
Bước 1:
Bước 2:
Bước 3:
Bước 4:
FeO + CO \(\underrightarrow{t^o}\) Fe + CO2
FeO là chất oxi hóa.
CO là chất khử.
b)
* ZnS + O2 \(\underrightarrow{t^o}\) ZnO + SO2
Bước 1:
Bước 2:
Bước 3:
Bước 4:
2ZnS + 3O2 \(\underrightarrow{t^o}\) 2ZnO + 2SO2
* ZnO + C \(\underrightarrow{t^o}\) Zn + CO
Bước 1:
Bước 2:
Bước 3:
Bước 4:
ZnO + C to\(\underrightarrow{t^o}\) Zn + CO
ZnS là chất khử.
O2 là chất oxi hóa
c)
Bước 1:
Bước 2:
Bước 3:
Bước 4:
NaCl là chất khử.
H2O là chất oxi hóa.
d) C2H5OH + O2 \(\underrightarrow{t^o}\) CO2 + H2O
Bước 1:
Bước 2:
Bước 3:
Bước 4:
C2H5OH + 9/2O2 \(\underrightarrow{t^o}\) 2CO2 + 6H2O
C2H5OH là chất khử.
O2 là chất oxi hóa.