Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a)n_{NaOH}=0,5.0,2=0,1mol\\ n_{H_2SO_4}=0,3.1=0,3mol\\2 NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\\ \Rightarrow\dfrac{0,1}{2}< \dfrac{0,3}{1}\Rightarrow H_2SO_4.dư\\ 2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
0,1 0,05 0,05 0,1
\(C_M\) \(_{Na_2SO_4}=\dfrac{0,05}{0,2+0,3}=0,1M\)
\(C_M\) \(_{H_2SO_4}=\dfrac{0,3-0,05}{0,2+0,3}=0,5M\)
b) Vì H2SO4 dư nên quỳ tím hoá đỏ.

Câu 1:
PTHH: 2Al + 3H2SO4 ===> Al2(SO4)3 + 3H2
a)Vì Cu không phản ứng với H2SO4 loãng nên 6,72 lít khí là sản phẩm của Al tác dụng với H2SO4
=> nH2 = 6,72 / 22,4 = 0,2 (mol)
=> nAl = 0,2 (mol)
=> mAl = 0,2 x 27 = 5,4 gam
=> mCu = 10 - 5,4 = 4,6 gam
b) nH2SO4 = nH2 = 0,3 mol
=> mH2SO4 = 0,3 x 98 = 29,4 gam
=> Khối lượng dung dịch H2SO4 20% cần dùng là:
mdung dịch H2SO4 20% = \(\frac{29,4.100}{20}=147\left(gam\right)\)
nH2 = 6.72 : 22.4 = 0.3 mol
Cu không tác dụng với H2SO4
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2
0.2 <- 0.3 <- 0.1 <- 0.3 ( mol )
mAl = 0.2 x 56 = 5.4 (g)
mCu = 10 - 5.4 = 4.6 (g )
mH2SO4 = 0.3 x 98 = 29.4 ( g)
mH2SO4 20% = ( 29.4 x100 ) : 20 = 147 (g)

\(n_{NaOH}=\dfrac{50\cdot20\%}{40}=0.25\left(mol\right)\)
\(n_{HNO_3}=\dfrac{84\cdot15\%}{63}=0.2\left(mol\right)\)
\(NaOH+HNO_3\rightarrow NaNO_3+H_2O\)
Lập tỉ lệ :
\(\dfrac{0.25}{1}>\dfrac{0.2}{1}\Rightarrow NaOHdư\)
Vì : NaOH dư nên quỳ tím sẽ hóa xanh.
\(m_{dd}=50+84=134\left(g\right)\)
\(n_{NaNO_3}=0.2\left(mol\right)\)
\(n_{NaOH\left(dư\right)}=0.25-0.2=0.05\left(mol\right)\)
\(C\%_{NaNO_3}=\dfrac{0.2\cdot85}{134}\cdot100\%=12.68\%\)
\(C\%_{NaOH\left(dư\right)}=\dfrac{0.05\cdot40}{134}\cdot100\%=1.49\%\)

2KOH+CO2=K2CO3
nKOH=28/56=0,5mol
nCO2=56/22,4=2,5 mol
Ta có 0,5/2<2,5/1=> KOH dư
Cứ 1 mol CO2-----> 1 mol K2CO3
0,5 0,5
mK2cO3=0,5.138=69g
NaOH+HCl=NaCl+H2O
nnaOH=20/40=0,5 mol
nHCl=18,25/36,5=0,5 mol
Ta có 0,5/1=0,5/1 Cả 2 chất tham gia đều phản ứng hết Tức là sau phản ứng chỉ có dung dich naCl .====>Nacl không làm đỏi màu quỳ tím
Ca(OH)2+2HCl=CaCl2+2H2O
nCa(OH)2=0,1 mol
nHCl=365/36,5=10 mol
Ta có 0,1/1<10/2====>HCl dư
Vậy dung dịch của bạn học sinh thứ 2 làm đổi màu quỳ tím thành màu đỏ

a) Vì: mA < 400 (g) nên phải có khí thoát ra → muối có dạng MHSO4 và khí là: CO2
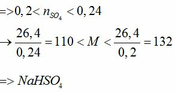
b)
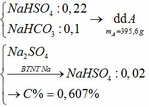
c) Tác dụng được với: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Fe, Fe(NO3)2
Pt: 2NaHSO4 + MgCO3 → Na2SO4 + MgSO4 + CO2↑ + H2O
2NaHSO4 + Ba(HSO3)2 → BaSO4 + Na2SO4 + SO2↑ + 2H2O
6NaHSO4 + Al2O3 → 3Na2SO4 + Al2(SO4)3 + 3H2O
2NaHSO4 + Fe(OH)2 → Na2SO4 + FeSO4 + 2H2O
2NaHSO4 + Fe → Na2SO4 + FeSO4 + H2↑
12NaHSO4 + 9Fe(NO3)2 → 5Fe(NO3)3 + 2Fe2(SO4)3 + 6Na2SO4 + 3NO↑ + 6H2O

a/ \(n_{KOH}=0,2.1=0,2\left(mol\right);n_{H_2SO_4}=0,3.1=0,3\left(mol\right)\)
PTHH: 2KOH + H2SO4 → K2SO4 + 2H2O
Mol: 0,2 0,1 0,1
Ta có: \(\dfrac{0,2}{2}< \dfrac{0,3}{1}\) ⇒ KOH hết, H2SO4 dư
b/ \(m_{H_2SO_4dư}=\left(0,3-0,1\right).98=19,6\left(g\right)\)
c/ Vdd sau pứ = 0,2 + 0,3 = 0,5 (l)
d/ \(C_{M_{ddK_2SO_4}}=\dfrac{0,1}{0,5}=0,2M\)
\(C_{M_{ddH_2SO_4dư}}=\dfrac{0,3-0,1}{0,5}=0,4M\)

\(n_{Ca\left(OH\right)_2}=0,2.1=0,2\left(mol\right)\\ n_{HCl}=\dfrac{73.10\%}{36,5}=0,2\left(mol\right)\\ Ca\left(OH\right)_2+2HCl\rightarrow CaCl_2+2H_2O\\ Vì:\dfrac{0,2}{2}< \dfrac{0,2}{1}\)
=> Ca(OH)2 dư
=> Dung dịch sau phản ứng có: Ca(OH)2 dư và CaCl2
\(m_{Ca\left(OH\right)_2\left(dư\right)}=\left(0,2-\dfrac{0,2}{2}\right).74=7,4\left(g\right)\)
- Nhúng quỳ tím vào dd thu được quỳ tím đổi màu xanh.
Câu 1 :
a ) \(K_2O+H_2SO_4\rightarrow K_2SO_4+H_2O\)
\(K_2SO_4+2HCl\rightarrow2KCl+H_2SO_4\)
\(KCl+NaOH\rightarrow KOH+NaCl\)
\(KOH+HCl\rightarrow KCl+H_2O\)
b) Ý b cũng tương tự ý a nha . Chỉ cần thay đổi 1 chút thôi .
Câu 2 :
Theo bài ra , ta có : \(\hept{\begin{cases}n_{NaOH}=\frac{200.10}{100.40}=0,5\left(mol\right)\\n_{H_2SO_4}=\frac{300.10}{100.98}\approx0,3\left(mol\right)\end{cases}}\)
+) \(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
Ta có : \(\frac{0,5}{2}=0,25< \frac{0,3}{1}=0,3\)
=> NaOH phản ứng hết , H2SO4 còn dư
=> Mọi tinh toán tính theo NaOH
+) Dung dịch tạo ra sau phản ứng không làm quỳ tím đổi màu .
b) \(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
Theo PTHH : 2 mol 1 mol 2 mol
Theo bài : 0,5 mol 0,25 mol 0,5 mol
\(\Rightarrow\hept{\begin{cases}m_{Na_2SO_4}=142.0,25=33,5\left(g\right)\\m_{H_2O}=18.0,5=9\left(g\right)\end{cases}}\)
Bài dưới cũng tương tự nha