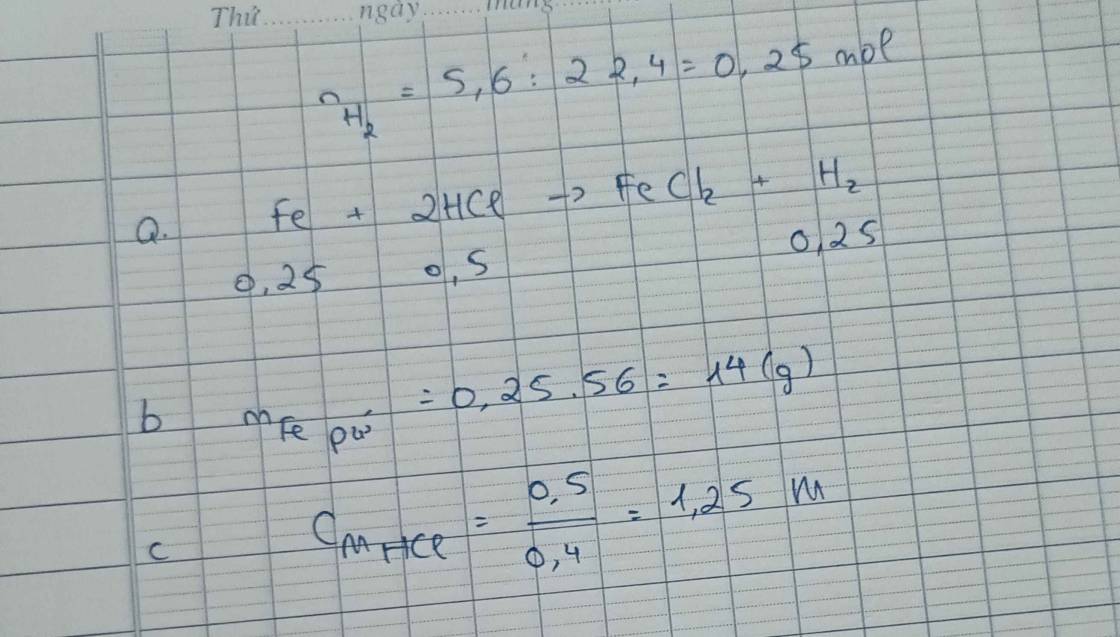Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Số mol khí H2 = 3,36 : 22,4 = 0,15 mol
a) Phương trình phản ứng:
Fe + 2HCl → FeCl2 + H2
Phản ứng 0,15 0,3 0,15 ← 0,15 (mol)
b) Khối lượng sắt đã phản ứng:
mFe = 0,15 . 56 = 8,4 g
c) Số mol HCl phản ứng:
nHCl = 0,3 mol; 50 ml = 0,05 lít
Nồng độ mol của dung dịch HCl: CM,HCl = \(\dfrac{0,3}{0,05}\) = 6M
a) 3Fe + 6HCL -> 2FeCl3 + 3H2
3 6 2 3 ( mol)
0,15 0,3 0,1 0,15 (mol)
Đổi 50ml = 0,05l
b) nH2 = \(\dfrac{V}{22,4}\)= \(\dfrac{3,36}{22,4}\)=0,15 (mol)
mFe= n.M = 0,15 . 56 = 8,4 (g)
c) CM HCL = \(\dfrac{n_{ct}}{V_{dd}}\)=\(\dfrac{0,3}{0,05}\)= 6 (mol/l)

\(n_{MgCO3}=\dfrac{8,4}{84}=0,1\left(mol\right)\)
a) Pt : \(2CH_3COOH+MgCO_3\rightarrow\left(CH_3COO\right)_2Mg+CO_2+H_2O|\)
2 1 1 1 1
0,2 0,1 0,1 0,1
b) \(n_{CH3COOH}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
⇒ \(m_{CH3COOH}=0,2.60=12\left(g\right)\)
\(C_{ddCH3COOH}=\dfrac{12.100}{200}=6\)0/0
\(n_{\left(CH3COO\right)2Mg}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ \(m_{\left(CH3COO\right)2Mg}=0,1.142=14,2\left(g\right)\)
\(m_{ddspu}=8,4+200-\left(0,1.44\right)=204\left(g\right)\)
\(C_{dd\left(CH3COO\right)2Mg}=\dfrac{14,2.100}{204}=6,96\)0/0
Chúc bạn học tốt

Số mol H2 = 2,24 : 22,4 = 0,1 mol.
a) Khi cho hỗn hợp (Zn, Cu) vào dung dịch H2SO4 loãng, chỉ có Zn phản ứng:
Zn + H2SO4 \(\rightarrow\) ZnSO4 + Н2
Phản ứng: 0,1 \(\leftarrow\) 0,1 (mol)
b) Chất rắn còn lại là Cu. mCu = 10,5 - 0,1 x 65 = 4 gam.
nkhí = 2,24 / 22,4 = 0,1 mol
a) Phương trình hóa học của phản ứng:
Zn + H2SO4 loãng → ZnSO4 + H2
nZn = 0,1 mol.
b) Khối lượng chất rắn còn lại: mZn = 6,5g
Khối lượng chất rắn còn lại: mCu = 10,5 – 6,5 = 4g.

nFe = = 0,1 mol; ns =
= 0,05 mol.
a) Phương trình hoá học: Fe + S FeS.
Lúc ban đầu: 0,1 0,05 0 (mol)
Lúc phản ứng: 0,05 0,05 0,05
Sau phản ứng: 0,05 0 0,05
Chất rắn A gồm FeS và Fe dư + HCl?
FeS + 2HCl → FeCl2 + H2S
Phản ứng: 0,05 0,1 0,05 0,05 (mol)
Fe + 2HCl → FeCl2 + H2
Phản ứng: 0,05 0,1 0,05 0,05 (mol).
Số mol HCl tham giá phản ứng = 0,1 + 0,1 = 0,2 mol.
Thể tích dung dịch HCl 1M dùng là: Vdd = =
= 0,2 lít.

a. PTHH: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
b. Có \(n_{Mg}=\frac{3,6}{24}=0,15mol\)
\(140ml=0,14l\)
\(n_{H_2SO_4}=0,14.1,2=0,168mol\)
Lập tỉ lệ \(\frac{n_{Mg}}{1}< \frac{n_{H_2SO_4}}{1}\)
Vậy Mg đủ, \(H_2SO_4\) dư
Theo phương trình \(n_{H_2SO_4}=n_{Mg}=0,15mol\)
\(\rightarrow n_{H_2SO_4\left(\text{(dư)}\right)}=0,168-0,15=0,018mol\)
\(\rightarrow m_{H_2SO_4\left(\text{(dư)}\right)}n.M=0,018.98=1,764g\)
c. MgSO\(_4\) là muối
Theo phương trình \(n_{MgSO_4}=n_{Mg}=0,15mol\)
\(\rightarrow m_{\text{muối}}=m_{MgSO_4}=n.M=0,15.120=18g\)
d. \(H_2\) là khí
Theo phương trình \(n_{H_2}=n_{Mg}=0,15mol\)
\(\rightarrow V_{H_2\left(ĐKTC\right)}=n.22,4=0,15.22,4=3,36l\)

gọi a là số mol của kẽm tham gia phản ứng:
PTHH: Zn+ CuSO4 \(\rightarrow\)ZnSO4 + Cu
a mol\(\rightarrow\)a mol \(\rightarrow\) a mol
theo đề bài cho độ giảm khối lượng của bản kẽm sau phản ứng là:
mZn tan - mCu bám = 65a- 64a = 50 - 49,81 = 0,18 ( mol)
a) khối lượng của kẽm tham gia phản ứng:
m= n x M = 0,18 x 65 = 11,7 (g)
b) Khối lượng của CuSO4 là
m= n x m = 0,18 x 160 = 28,8 g

nFe = 0,1 mol; nS = 0,05 mol
a) Phương trình phản ứng:
Fe + S → FeS (1)
nFe dư = 0,1 – 0,05 = 0,05 nên hỗn hợp chất rắn A có Fe và FeS.
Fe + 2HCl → FeCl2 + H2↑ (2)
FeS + 2HCl → FeCl2 + H2S↑ (3)
b) Dựa vào phương trình phản ứng (2) và (3), ta có:
nHCl= 0,1 + 0,1 = 0,2 mol
VHCl = 0,2 /1 = 0,2 lít.

Câu 7:
2Fe + 3Cl2 -to> 2FeCl3
FeCl3 + 3NaOH -> 3NaCl + Fe(OH)3
2Fe(OH)3 -to> Fe2O3 + 3H2O
Fe2O3 + 3H2SO4 -> Fe2(SO4)3 + 3H2O
Câu 8:
- Lấy mỗi chất một ít làm mẫu thử
- Nhúng quỳ tím vào từng mẫu thử
+ Mẫu thử ko làm quỳ tím chuyển màu là Na2SO4
+ Mẫu thử làm quỳ tím chuyển đỏ là HCl và H2SO4
- Cho dung dịch Ba(OH)2 vào hai mẫu thử làm quỳ tím chuyển đỏ
+ Mẫu thử tạo kết tủa trắng là H2SO4
Ba(OH)2 + H2SO4 -> BaSO4 + 2H2O
+ Mẫu thử ko có hiện tượng là HCl
Ba(OH)2 + 2HCl -> BaCl2 + 2H2O
Câu 9:
200 ml = 0,2 l
nH2 = 4,48/22,4 = 0,2 (mol)
Fe + H2SO4 -> FeSO4 + H2
0,2 <- 0,2 <- 0,2 <- 0,2
mFe = 0,2.56 = 11,2 (g)
CMH2SO4 = 0,2/0,2 = 1 M