Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a.
BTKL ta có mX = mY => nX . MX = nY . mY
MX / My = nY / mY =0.75
Đặt nX = 1 mol => nY = 0,75 mol => nH2 phản ứng = 1 – 0,75 = 0,25mol
* TH hidrocacbon là anken: n anken = n H2 = 0,25 mol => n H2 trong X = 0,75 => M = (6,75 – 0,75 . 2)/0,25 = 21 (loại) * TH là ankin: => n akin = 0,25/2 = 0,125 => n H2 trong X = 0,875 mol => M = (6,75 – 0,875 . 2)/0,125 = 40 =>C3H4
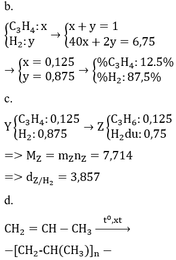


Chỉ có Zn phản ứng thôi. Cu không phản ứng, không tan.---->Chất rắn không tan là Cu
Zn+ H2SO4 ---> ZnSO4+ H2↑
0.1 0.1
nH2= 2.24: 22.4=0.1 mol
mZn= 0.1x65=6.5 g
mCu=10.5-6,5=4 g
%Zn=6.5:10.5x100%=61.9%
%Cu=4:10.5x100%=38.1%

Bài 3:
Khi cho tác dụng với HCl thì chỉ có Zn phản ứng
Zn + 2HCl ----> ZnCl2 + H2 (1)
0.2mol <------------------------- 0.2mol
Vậy khối lượng Zn = 13g
Nung hh trên trong không khí sẽ có các phản ứng:
Zn + O2 ----> ZnO (2)
0.2mol -----------------> 0.2mol = 16.2g
Cu + 1/2O2 ----> CuO
Ta nhận thấy Ag không phản ứng với Ôxi vậy khối lượng chất rắn tăng lên là do sự hình thành 2 ôxit ZnO và CuO. Số mol của O trong hổn hợp 2 ôxit = (51.9 - 45.5) / 16 = 0.4 mol
Theo PT (2) ta thấy số mol của O trong ZnO =số mol của ZnO = 0.2 mol, vậy số mol của O trong CuO = 0.4 - 0.2 = 0.2 mol. Số mol của Cu = 0.2 mol -> khối lượng Cu ban đầu = 0.2 * 64 = 12.8g
Khối lượng Ag trong hh ban đầu = 45.5 - 12.8 - 13 = 19.7g.
Vì Cu và Ag là hai kim loại đứng sau H2 trong dãy hoạt động của kim loại nên không thể tác dụng được với dd HCl
Theo bài ra ta có: \(nH_2=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
a) PTHH:
\(Z_n+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
\(0,2mol....................0,2mol\)
\(2Cu+O_2-^{t0}\rightarrow2CuO\)
\(2Zn+O_2-^{t0}\rightarrow2ZnO\)
\(0,2mol.......................0,2mol\)
\(Ag+O_2\ne ko-pư\)
Chất rắn thu được sau khi nung là CuO, ZnO và Ag.
Gọi x,y lần lượt là số mol của Cu và Ag
Ta có:
mZnO + mCuO + mAg = 51,9
mZn + mCu + mAg = 45,5
Ta có:
mCu + mAg = 45,5 - 0,2.65
⇔ 64x + 108y = 32,5 (1)
mCuO + mAg = 51,9 - 0,2.81
⇔ 80x + 108y = 35,7 (2)
Từ (1) và ( 2) ta được: \(\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,182\left(mol\right)\end{matrix}\right.\)
b) Thành phần % theo khối lượng có trong hỗn hợp ban đầu là:
\(\left\{{}\begin{matrix}\%mZn=\dfrac{0,2.65}{45,5}.100\%\approx28,57\%\\\%mCu=\dfrac{0,2.64}{45,5}.100\%\approx28,133\%\\\%mAg=100\%-28,75\%-28,13\%=43,3\%\end{matrix}\right.\)

a) MX = 146g/mol
VCO2 : VH2O = 6 : 5
=> nC : nH = 3 : 5
=> CTĐGN: (C3H5Oa)n
→ (41 + 16a).n = 146 → (a; n) = (4; 2) → X: C6H10O4
b) C6H10O4 + 6,5O2 → 6CO2 + 5H2O
0,05 0,325
=> p = 7,3g
c)
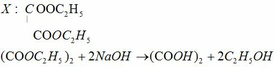

2yAl +3FexOy -to-> 3xFe + yAl2O3 (1)
phần 1 : Fe +4HNO3 --> Fe(NO3)3 + NO +2H2O (2)
Al2O3 + 6HNO3 --> 2Al(NO3)3 +3H2O (3)
Al +4HNO3 --> Al(NO3)3 +NO +2H2O (4)
P2 : Al2O3 +2NaOH --> 2NaAlO2 +H2O (5)
2Al +2H2O +2NaOH --> 2NaAlO2 +3H2 (6)
vì khi cho phần 2 td vs NaOH dư thấy giải phóng H2 => Al dư sau (1)
nH2=0,015(mol)
nFe(P2)=0,045(mol)
giả sử P1 gấp k lần P2
=> nFe(P1)=0,045k(mol)
theo (5) : nAl(P2)=2/3nH2=0,01(mol)
=>nAl(P1)=0,01k(mol)
nNO=0,165(mol)
theo (2,4) :nNO=(0,045k+0,01k) (mol)
=>0,055k=0,165=> k=3
=>nAl(P1)=0,03(mol)
nFe(p1)=0,135(mol)
\(\Sigma nFe=0,045+0,135=0,18\left(mol\right)\)
\(\Sigma nAl=0,03+0,01=0,04\left(mol\right)\)
mAl2O3=\(14,49-0,135.56-0,03.27=6,12\left(g\right)\)
nAl2O3(P1)=0,06(mol)
=> nAl2O3(P2)=0,02(mol)
\(\Sigma nAl2O3=0,08\left(mol\right)\)
theo (1) : nFe=3x/ynAl2O3
=> 0,18=3x/y.0,08=> x/y=3/4
=>CTHH : Fe3O4
theo (1) :nFe3O4 =1/3nFe=0,06(mol)
=>m=0,04.27+0,06.232=15(g)
bạn Lê Đình Thái ơi bạn giải nhầm tìm m rồi. Cái 0,04 mol đó là mol dư, bạn phải cộng với 0,16 mol phản ứng khi xảy ra phản ứng nhiệt phân nữa.
Kết quả là m=0,2.27+0,06.232=19,32 gam

(a) Gọi CTPT của các chất là CxHyOz
M<170 => mC<170.55,8% => 12x<94,86 => x<7,9
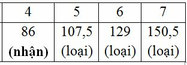
Vậy CTPT có dạng: C4HyOz (y≤10)(Do M là các số nguyên và là số chẵn)
Ta có: 12.4 + y + 16z = 86 => y + 16z = 38
+ z = 1: y = 22 (loại)
+ z = 2: y = 6 (nhận)
Vậy CTPT của các chất là: C4H6O2
b) A, B đều có nhóm CH3 và phản ứng với NaHCO3 tạo khí và chỉ có B có đồng phân hình học nên cấu tạo của A và B là:
A: CH2=C(CH3)-COOH
B: CH3-CH=CH-COOH
F, H, K có phản ứng với NaHCO3 tạo khí nên F, H, K là các axit.
- G là hợp chất không bền và chuyển hóa ngay thành G’ (G và G’ có cùng công thức phân tử) và khi oxy hóa bằng H2CrO4, hợp chất G’ chuyển hóa thành F nên G’ và F có cùng số nguyên tử C
C: CH3COOCH=CH2
F: CH3COOH
G: CH2=CH-OH
G’: CH3CHO
- H có phản ứng với NaHCO3 tạo khí nên H là axit. Mặt khác, phản ứng của H với bạc nitrat trong amoniac chỉ tạo thành các chất vô cơ nên H là HCOOH
D: HCOOCH2-CH=CH2
H: HCOOH
I: CH2=CH-CH2-OH
- L bị oxi hóa tạo HCOOH nên L là CH3OH
E: CH2=CH-COOCH3
K: CH2=CH-COOH
L: CH3OH
(1) CH2=C(CH3)-COOH (A) + NaHCO3 → CH2=C(CH3)-COONa + H2O + CO2
(2) CH3-CH=CH-COOH (B) + NaHCO3 → CH3-CH=CH-COONa + H2O + CO2
(3) CH3COOCH=CH2 (C) + NaOH → CH3COONa + CH3CHO (G’)
(4) CH3COONa + HCl → CH3COOH (F) + NaCl
(5) HCOOCH2-CH=CH2 (D) + NaOH → HCOONa + CH2=CH-CH2-OH (I)
(6) HCOONa + HCl → HCOOH (H) + NaCl
(7) CH2=CH-COOCH3 (E) + NaOH → CH2=CH-COONa + CH3OH (L)
(8) CH2=CH-COONa + HCl → CH2=CH-COOH (K) + NaCl
(9) CH3CHO + H2CrO4 → CH3COOH + H2CrO3
(10) CH3OH + 2H2CrO4 → HCOOH + 2H2CrO3 + H2O
(11) HCOOH + 2AgNO3 + 4NH3 + H2O → (NH4)2CO3 + 2Ag + 2NH4NO3
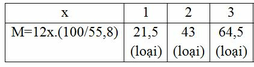
(c) Phản ứng polime hóa của A và C:
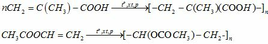
(d)
