Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) MgO + 2HCl ---> MgCl2 + H2O (1)
MgCO3 + 2HCl ---> MgCl2 + H2O + CO2 (2)
b) \(n_{CO_2}=\dfrac{m}{M}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
=> \(m_{MgCO_3}=n.M=0,1.84=8,4\left(g\right)\)
\(m_{MgO}=16-8,4=8\left(g\right)\)
c) \(n_{MgO}=\dfrac{m}{M}=\dfrac{8}{40}=0,2\left(mol\right)\)
=> \(n_{HCl\left(1\right)}=0,4\left(mol\right)\); nHCl(2) = 0,2(mol)
=> nHCl = 0.4 + 0,2 = 0,6 (mol)
=> VHCl = \(\dfrac{n}{C_M}=\dfrac{0,6}{1,5}=0,4\left(l\right)=400\left(ml\right)\)

a, \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
b, Gọi: \(\left\{{}\begin{matrix}n_{CuO}=x\left(mol\right)\\n_{Fe_2O_3}=y\left(mol\right)\end{matrix}\right.\) ⇒ 80x + 160y = 32 (1)
Theo PT: \(\left\{{}\begin{matrix}n_{CuCl_2}=n_{Cu}=x\left(mol\right)\\n_{FeCl_3}=2n_{Fe_2O_3}=2y\left(mol\right)\end{matrix}\right.\) ⇒ 135x + 325y = 59,5 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{CuO}=0,2.80=16\left(g\right)\\m_{Fe_2O_3}=0,1.160=16\left(g\right)\end{matrix}\right.\)
c, Theo PT: \(n_{HCl}=2n_{CuO}+6n_{Fe_2O_3}=1\left(mol\right)\)
\(\Rightarrow V_{ddHCl}=\dfrac{1}{0,5}=2\left(l\right)\)

\(n_{H2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
a) Pt : \(2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2|\)
2 2 2 2 3
0,2 0,2 0,3
\(Al_2O_3+2NaOH\rightarrow2NaAlO_2+H_2O|\)
1 2 2 1
0,1 0,2
b) \(n_{Al}=\dfrac{0,3.2}{3}=0,2\left(mol\right)\)
\(m_{Al}=0,2.27=5,4\left(g\right)\)
\(m_{Al2O3}=15,6-5,4=10,2\left(g\right)\)
c) Có : \(m_{Al2O3}=10,2\left(g\right)\)
\(n_{Al2O3}=\dfrac{10,2}{102}=0,1\left(mol\right)\)
\(n_{NaOH\left(tổng\right)}=0,2+0,2=0,4\left(mol\right)\)
\(V_{ddNaOH}=\dfrac{0,4}{1}=0,4\left(l\right)=400\left(ml\right)\)
Chúc bạn học tốt

m rắn giảm = mO (oxit) => nO (oxit) = (1,6 – 1,408) : 16 = 0,012mol
Dễ thấy n = nO (oxit) = 0,012mol
=> nH2 ban đầu = 0,012 : 80% = 0,015
=> nFe = nH2= 0,015 → x = 0,015
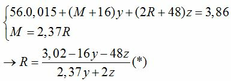
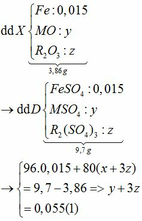
Ta có: CO + O(Oxit) → CO2
Vì: m(Rắn giảm) = mO(Oxit) → nO(Oxit) = (3,86 – 3,46) : 16 = 0,025
TH1: cả 2 oxit đều bị khử bởi CO
→ nO(Oxit) = y + 3z = 0,025 kết hợp với (1) loại
TH2: chỉ có MO bị khử bởi CO
→ nO(Oxit) = nMO = 0,025 → y = 0,025 kết hợp với (1) => z = 0,01
Kết hợp với (*) => M = 64 (Cu)
TH3: chỉ có R2O3 bị khử bởi CO
→ nO(Oxit) = 3.nR2O3 → z = 0,025/3 kết hợp với (1) => y = 0,03
Kết hợp với (*) y => M lẻ => loại
Vậy %m các chất trong X là: 21,76%; 51,81%; 26,43%

nH2=0,1(mol)
PTHH: Mg + 2 HCl -> MgCl2 + H2
0,1__________0,2___________0,1(mol)
MgO + 2 HCl -> MgCl2 + H2O
0,05____0,1___0,05(mol)
mMg=0,1. 24= 2,4(g) -> mMgO=4,4-2,4= 2(g) -> nMgO=0,05((mol)
b) %mMg= (2,4/4,4).100=54,545%
=> %mMgO=45,455%
c) nHCl=0,3(mol) -> mHCl=0,3.36,5=10,95(g)
=> mddHCl=(10,95.100)/7,3=150(g)

PTHH: \(CaO+2HCl\rightarrow CaCl_2+H_2O\) (1)
\(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\uparrow\) (2)
a) Ta có: \(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)=n_{CaCO_3}\)
\(\Rightarrow m_{CaCO_3}=0,2\cdot100=20\left(g\right)\) \(\Rightarrow\%m_{CaCO_3}=\dfrac{20}{25,6}\cdot100\%=78,125\%\)
\(\Rightarrow\%m_{CaO}=21,875\%\)
b) Theo 2 PTHH: \(\left\{{}\begin{matrix}n_{HCl\left(2\right)}=2n_{CaCO_3}=0,4mol\\n_{HCl\left(1\right)}=2n_{CaO}=2\cdot\dfrac{25,6-20}{56}=0,2mol\end{matrix}\right.\)
\(\Rightarrow\Sigma n_{HCl}=0,6mol\) \(\Rightarrow C\%_{HCl}=\dfrac{0,6\cdot36,5}{210\cdot1,05}\cdot100\%\approx9,93\%\)

Gọi: M là NTK của R
a là số oxi hóa của R trong muối --> CTPT muối của R là R(2/a)CO3.
a) Từ nCO2 = n hỗn hợp = 0,5 nHCl = 3,36/22,4 = 0,15
--> nHCl = 0,15 x 2 = 0,3 mol nặng 0,3 x 36,5 = 10,95 gam.
--> dung dịch axit HCl 7,3% nặng 10,95/0,073 = 150 gam.
Mà
m dung dịch sau phản ứng = m dung dịch axit + m C - m CO2 bay ra
= 150 + 14,2 - (0,15 x 44) = 157,6 gam
--> m MgCl2 = 0,06028 x 157,6 = 9,5 gam
--> n MgCl2 = 9,5/95 = 0,1 mol = n MgCO3
--> m MgCO3 = 0,1 x 84 = 8,4 gam chiếm 8,4/14,2 = 59,154929%
--> m R(2/a)CO3 = 14,2 - 8,4 = 5,8 gam chiếm 5,8/14,2 = 40,845071%
--> n R(2/a)CO3 = 0,15 - 0,1 = 0,05 mol.
--> PTK của R(2/a)CO3 = 5,8/0,05 = 116.
--> 2M/a = 116 - 60 = 56 hay M = 23a.
Chọn a = 2 với M = 56 --> R là Fe.
b) Khối lượng chất rắn sau khi nung đến khối lượng không đổi là khối lượng của 0,1 mol MgO và 0,05 mol FeO(1,5). (FeO(1,5) là cách viết khác của Fe2O3. Cũng là oxit sắt 3 nhưng PTK chỉ bằng 80).
m chất rắn sau khi nung = (0,1 x 40) + (0,05 x 80) = 8 gam.

\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ a,PTHH:MgCO_3+H_2SO_4\rightarrow MgSO_4+H_2O+CO_2\uparrow\\ MgO+H_2SO_4\rightarrow MgSO_4+H_2O\\ \Rightarrow n_{MgCO_3}=n_{CO_2}=0,1\left(mol\right)\\ \Rightarrow m_{MgCO_3}=0,1\cdot84=8,4\left(g\right)\\ \Rightarrow\%_{MgCO_3}=\dfrac{8,4}{10,4}\cdot100\%\approx80,77\%\\ \Rightarrow\%_{MgO}=100\%-80,77\%=19,23\%\)
\(b,m_{MgO}=10,4-8,4=2\left(g\right)\\ \Rightarrow n_{MgO}=\dfrac{2}{40}=0,05\left(mol\right)\\ \Rightarrow\sum n_{H_2SO_4}=n_{MgCO_3}+n_{MgO}=0,15\left(mol\right)\\ \Rightarrow\sum m_{H_2SO_4}=0,15\cdot98=14,7\left(g\right)\\ \Rightarrow\sum m_{dd_{H_2SO_4}}=\dfrac{14,7}{9,8\%}=150\left(g\right)\\ \sum n_{MgSO_4}=\sum n_{H_2SO_4}=0,15\left(mol\right)\\ \Rightarrow\sum m_{MgSO_4}=0,15\cdot120=18\left(g\right)\\ \Rightarrow C\%_{MgSO_4}=\dfrac{18}{10,4+150-0,1\cdot44}\approx11,54\%\)
4. \(MgCO_3+2HCl\rightarrow MgCl_2+H_2O+CO_2\)
\(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\)
Gọi a,b lần lượt là số mol MgCO3 và CaCO3\(\rightarrow\left\{{}\begin{matrix}a+b=0,05\\84a+100b=4,52\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}a=0,03\\b=0,02\end{matrix}\right.\)
\(\rightarrow m_{MgCO3}=2,52\left(g\right);m_{CaCO3}=2\left(g\right)\)
\(n_{HCl_{pu}}=2.\left(0,03+0,02\right)=0,1\left(mol\right)\)
\(m_{ddHCl_{candung}}=\frac{\left(0,1.36,5\right).100\%}{7,3}=50\left(g\right)\)
mdd Y = mhh rắn + mdd HCl - mCO2 thoát ra
\(=4,52+50-0,05.44=53,32\left(g\right)\)
5. Gọi a,b lần lượt là số mol ZnO và Fe2O3\(\left\{{}\begin{matrix}81a+160b=4,01\left(g\right)\\65a+56.2b=2,89\left(g\right)\rightarrow\end{matrix}\right.\left\{{}\begin{matrix}a=0,01\left(mol\right)\\b=0,02\left(mol\right)\end{matrix}\right.\)
\(n_{O2}=0,01+0,02.3=0,07\)
\(\rightarrow n_{CO}=n_{O2}=0,07\left(mol\right)\rightarrow V_{CO}=0,07.22,4=1,569\left(l\right)\)
Câu 5:
ZnO + CO ----->Zn + CO2 (1)
Fe2O3 + 3CO -----------> 2Fe + 3CO2 (2)
Gọi nZnO = x (mol) ; nFe2O3 = y (mol )
Theo (1) :
nZn = nCO(1) = n ZnO = x (mol)
Theo (2):
nFe = 2nFe2O3 = 2x ( mol)
Theo đề bài , ta có hệ phương trình :
\(\left\{{}\begin{matrix}81x+160y=4,01\\65x+112y=2,89\end{matrix}\right.\)
Giải hệ ta được :
x =0,01 (mol)
y = 0,02 (mol)
=> %mZnO = (0,01 . 81 / 4,01) . 100% =20,2%
%mFe2O3 = ( 0,02 . 160 /4,01) .100% = 79,8 %
Theo (2) :
nCO (2) = 3nFe2O3 = 3y (mol)
=> VCO cần dùng = (x+3y).22,4 = (0,01 + 0,06 ) .22,4 =1,568 (l)