Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1 :
\(2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ 2Mg + O_2 \xrightarrow{t^o} 2MgO\\ 2Cu + O_2 \xrightarrow{t^o} 2CuO\\ S + O_2 \xrightarrow{t^o} SO_2\\ 4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3\\ C + O_2 \xrightarrow{t^o} CO_2\\ 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\)

a)
\(C + O_2 \xrightarrow{t^o} CO_2\\ n_{CO_2} = n_{O_2} = \dfrac{6,4}{32} = 0,2(mol)\\ \Rightarrow m_{CO_2} = 0,2.44 = 8,8(gam)\)
b)
\(n_C = \dfrac{6}{12} = 0,5(mol)\\ n_{O_2} =\dfrac{19,2}{32} = 0,6(mol)\\ C + O_2 \xrightarrow{t^o} CO_2\)
\(n_C = 0,5 < n_{O_2} = 0,6 \Rightarrow\) Oxi dư.
\(n_{CO_2} = n_C = 0,5(mol)\\ \Rightarrow m_{CO_2} = 0,5.44 = 22(gam)\)

1.
H2+ 1/2O2 --to> H2O
Mg + 1/2O2 --to> MgO
Cu+ 1/2O2--to>CuO
S+O2 --to>SO2
4Al+ 3O2--to>2Al2O3
C+ O2--to> CO2
2P+5/2O2--to> P2O5
b2
a)
C+O2to→CO2
nCO2=6,4\32=0,2
=>nCO2=nO2=0,2 mol
mCO2=0,2x44=8,8 g
b)
nC=6\12=0,5
nO2=19,2\32=0,6
C+O2to→CO2
TPU 0,5 0,6
PU 0,5 0,5 0,5
SPU 0 0,1 0,5
mCO2=0,5x44=22 g
b3
CH4+2O2to→CO2+2H2O
2C2H2+5O2to→4CO2+2H2O
C2H6O+3O2to→2CO2+3H2O
b4
a)
4P+5O2->2P2O5
nP=46,5/31=1,5 mol
=>nO2=1,5x5/4=1,875 mol
mO2=1,875x32=60 g
b)
nC=30/12=2,5 mol
C+O2->CO2
2,5 2,5
mO2=2,5x32=80 g
c)
nAl=67,5/27=2,5 mol
4Al+3O2->2Al2O3
2,5 1,875
mO2=1,875x32=60 g
d)
nH2=33,6/22,4=1,5 mol
2H2+O2->2H2O
1,5 0,75
mO2=32x0,75=24 g
b5
a,
nO2= 0,46875 mol
nSO2= 0,3 mol
S+ O2 -> SO2
=> O2 dư 0,16875 mol. Có 0,3 mol S cháy
mS= 9,6g
b,
mO2 dư= 5,4g
b6
CÓ nO2 = S/6.1023 = 3.1024 / 6. 1023 = 5 (mol)
=> VO2 = n x 22.4 = 5 x 22.4 =112(l)
b7
4P+5O2=to=>2P2O5
nP=6,2\31=0,2(mol);nO2=6,72\22,4=0,3(mol)
Theo PTHH, ta có: 0,2\4<0,3\5=>O2 dư
nO2(dư)=0,3−(0,2.5\4)=0,05(mol)
mO2(dư)=0,05.32=1,6(g)
nP2O5=2\4.nP=2\4.0,2=0,1(mol)
mP2O5=0,1.142=14,2(g)
b8
a. Số mol oxit sắt từ : nFe3O4=2,32\(56.3+16.4) = 0,01 (mol).
Phương trình hóa học.
3Fe + 2O2 -to> Fe3O4
3mol 2mol 1mol.
.................................... 0,01 mol.
Khối lượng sắt cần dùng là : m = 56.3.0,011=1,6856.3.0,01\1=1,68 (g).
Khối lượng oxi cần dùng là : m = 32.2.0,011=0,6432.2.0,01\1=0,64 (g).
b. Phương trình hóa học :
2KMnO4 to-> K2MnO4 + O2
2mol 1mol
n = 0,04 0,02
Số gam penmangarat cần dùng là : m= 0,04. (39 + 55 +64) = 6,32 g.
b9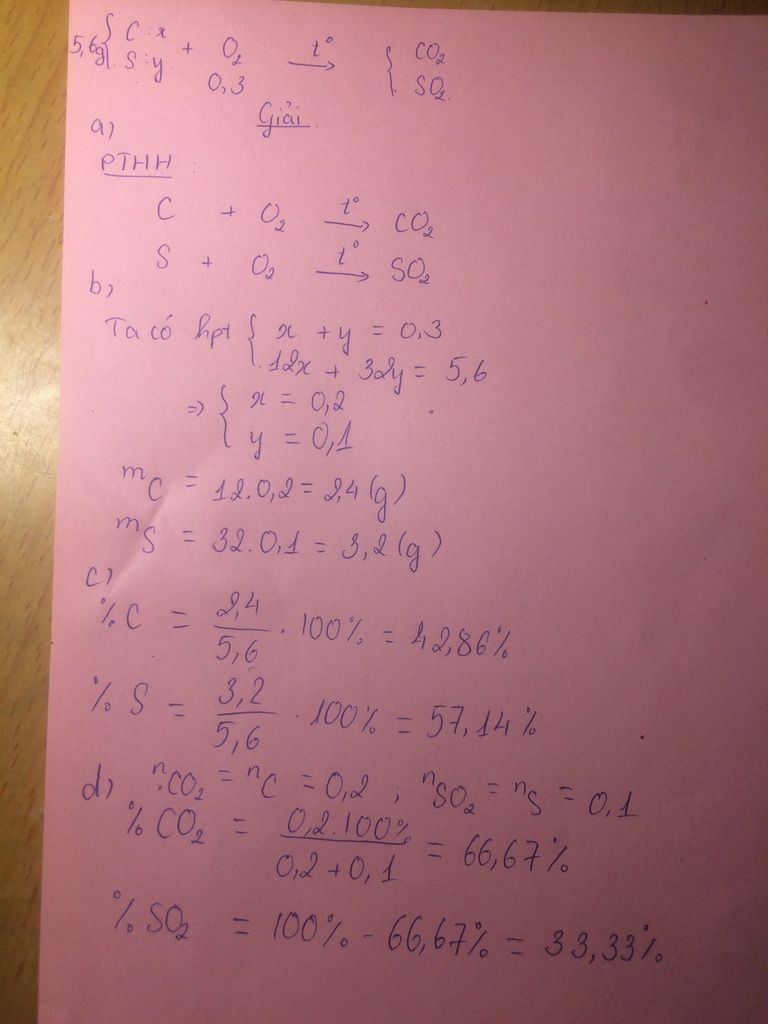
b11
a) PTHH: C + O2 → CO2 ↑
Đổi: 1 tấn = 1000000 gam
Khối lượng của C trong than là: 1000000.95% = 950000 gam
Số mol của C là: 950000:12 = 79166,67 mol
Số mol của O2 = 79166,67 mol
Khối lượng ôxi cần dùng là: 79166,67 . 32 = 2533333,44 gam

Câu 1:
PTHH: Fe + 2HCl ===> FeCl2 + H2
a/ nFe = 11,2 / 56 = 0,2 mol
=> nH2 = 0,2 mol
=> VH2(đktc) = 0,2 x 22,4 = 4,48 lít
b/ => nHCl = 0,2 x 2 = 0,4 mol
=> mHCl = 0,4 x 36,5 = 14,6 gam
c/ => nFeCl2 = 0,2 mol
=> mFeCl2 = 0,2 x 127 = 25,4 gam
Câu 3/
a/ Chất tham gia: S, O2
Chất tạo thành: SO2
Đơn chất: S, O2 vì những chất này chỉ do 1 nguyên tố tạo nên
Hợp chất: SO2 vì chất này do 2 nguyên tố S và O tạo tên
b/ PTHH: S + O2 =(nhiệt)==> SO2
=> nO2 = 1,5 mol
=> VO2(đktc) = 1,5 x 22,4 = 33,6 lít
c/ Khí sunfuro nặng hơn không khí

PTHH: 2C2H2 + 5O2 → 2H2O + 4CO2
VO2(đktc) = \(\frac{1,12\times20}{100}=0,244\left(lít\right)\)
=> nO2 = 0,224 / 22,4 = 0,01 (mol)
nC2H2 = 0,004(mol)
=> a = 0,004 x 26 = 0,104 (gam)
nH2O = 0,004 (mol)
=> mH2O = 0,004 x 18 = 0,072 (gam) = b
nCO2 = 0,008 (mol)
=> VCO2(đktc) = 0,008 x 22,4 = 0,1792(lít) = c

bài 5:
PTHH: C + O2 -> CO2
a) Số Mol của Oxi là:
ADCT: n= m/M
=>nO2= 6,4/ 32= 0,2 ( mol)
theo PT: nCO2 = nO2 = 0,2 mol
klg của CO2 là:
ADCT: m = n. M
=> mCO2= 0.2 . 12 = 2,4 (g)
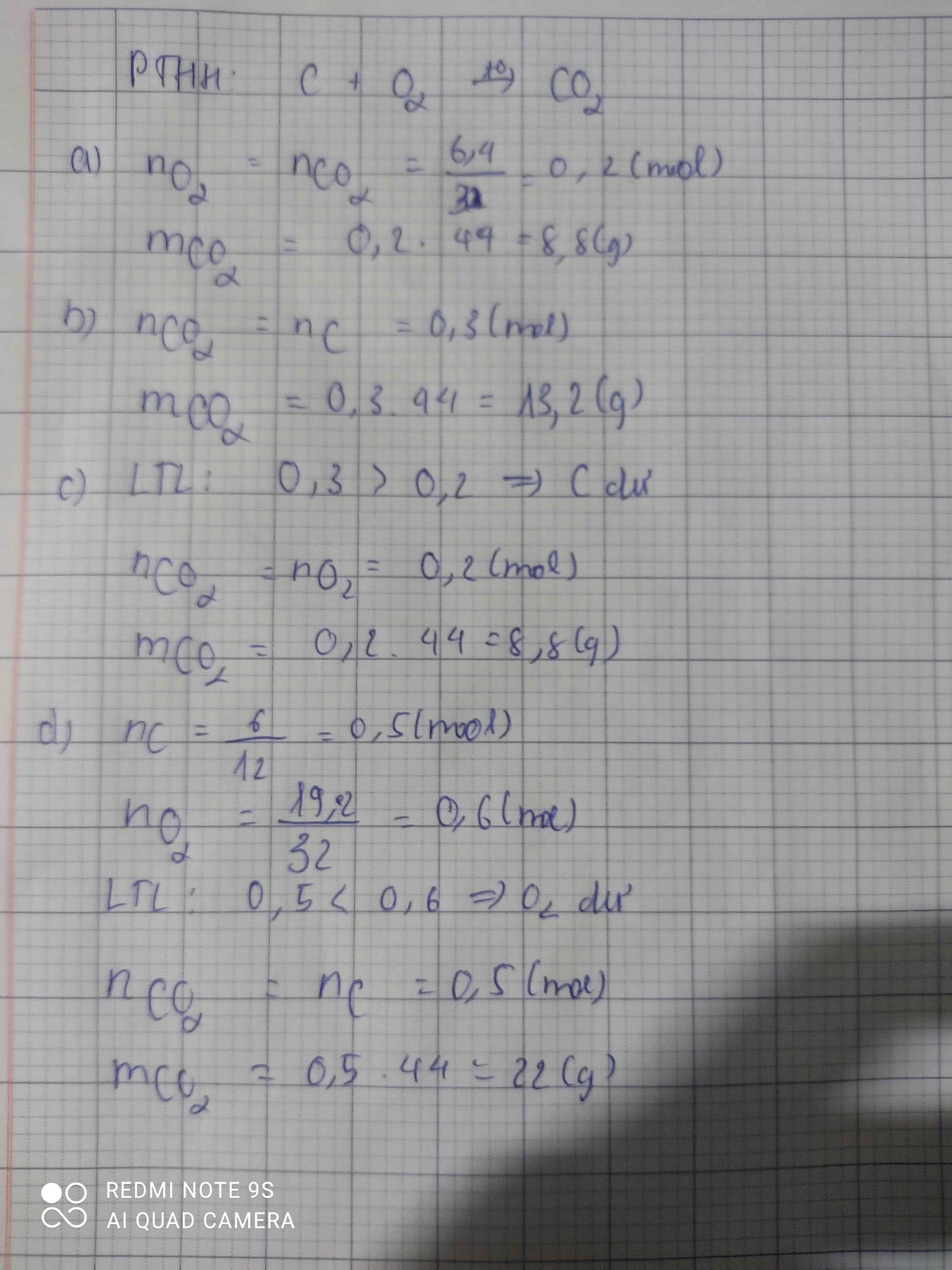
\(1,2H_2+O_2\underrightarrow{t}2H_2O\)
\(2Mg+O_2\underrightarrow{t}2MgO\)
\(2Cu+O_2\underrightarrow{t}2CuO\)
\(S+O_2\underrightarrow{t}SO_2\)
\(4Al+3O_2\underrightarrow{t}2Al_2O_3\)
\(C+O_2\underrightarrow{t}CO_2\)
\(4P+5O_2\underrightarrow{t}2P_2O_5\)
\(2,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(a,n_{O_2}=0,2\left(mol\right)\Rightarrow n_{CO_2}=0,2\left(mol\right)\Rightarrow m_{CO_2}=8,8\left(g\right)\)
\(b,n_C=0,3\left(mol\right)\Rightarrow n_{CO_2}=0,3\left(mol\right)\Rightarrow m_{CO_2}=13,2\left(g\right)\)
c, Vì\(\frac{0,3}{1}>\frac{0,2}{1}\)nên C phản ửng dư, O2 phản ứng hết, Bài toán tính theo O2
\(n_{O_2}=0,2\left(mol\right)\Rightarrow n_{CO_2}=0,2\left(mol\right)\Rightarrow m_{CO_2}=8,8\left(g\right)\)
\(3,PTHH:CH_4+2O_2\underrightarrow{t}CO_2+2H_2O\)
\(C_2H_2+\frac{5}{2}O_2\underrightarrow{t}2CO_2+H_2O\)
\(C_2H_6O+3O_2\underrightarrow{t}2CO_2+3H_2O\)
\(4,a,PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
\(n_P=1,5\left(mol\right)\Rightarrow n_{O_2}=1,2\left(mol\right)\Rightarrow m_{O_2}=38,4\left(g\right)\)
\(b,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(n_C=2,5\left(mol\right)\Rightarrow n_{O_2}=2,5\left(mol\right)\Rightarrow m_{O_2}=80\left(g\right)\)
\(c,PTHH:4Al+3O_2\underrightarrow{t}2Al_2O_3\)
\(n_{Al}=2,5\left(mol\right)\Rightarrow n_{O_2}=1,875\left(mol\right)\Rightarrow m_{O_2}=60\left(g\right)\)
\(d,PTHH:2H_2+O_2\underrightarrow{t}2H_2O\)
\(TH_1:\left(đktc\right)n_{H_2}=1,5\left(mol\right)\Rightarrow n_{O_2}=0,75\left(mol\right)\Rightarrow m_{O_2}=24\left(g\right)\)
\(TH_2:\left(đkt\right)n_{H_2}=1,4\left(mol\right)\Rightarrow n_{O_2}=0,7\left(mol\right)\Rightarrow m_{O_2}=22,4\left(g\right)\)
\(5,PTHH:S+O_2\underrightarrow{t}SO_2\)
\(n_{O_2}=0,46875\left(mol\right)\)
\(n_{SO_2}=0,3\left(mol\right)\)
Vì\(0,46875>0,3\left(n_{O_2}>n_{SO_2}\right)\)nên S phản ứng hết, bài toán tính theo S.
\(a,\Rightarrow n_S=n_{SO_2}=0,3\left(mol\right)\Rightarrow m_S=9,6\left(g\right)\)
\(n_{O_2}\left(dư\right)=0,16875\left(mol\right)\Rightarrow m_{O_2}\left(dư\right)=5,4\left(g\right)\)
\(6,a,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_C=1,5\left(mol\right)\Rightarrow m_C=18\left(g\right)\)
\(b,PTHH:2H_2+O_2\underrightarrow{t}2H_2O\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_{H_2}=0,75\left(mol\right)\Rightarrow m_{H_2}=1,5\left(g\right)\)
\(c,PTHH:S+O_2\underrightarrow{t}SO_2\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_S=1,5\left(mol\right)\Rightarrow m_S=48\left(g\right)\)
\(d,PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_P=1,2\left(mol\right)\Rightarrow m_P=37,2\left(g\right)\)
\(7,n_{O_2}=5\left(mol\right)\Rightarrow V_{O_2}=112\left(l\right)\left(đktc\right)\);\(V_{O_2}=120\left(l\right)\left(đkt\right)\)
\(8,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(m_C=0,96\left(kg\right)\Rightarrow n_C=0,08\left(kmol\right)=80\left(mol\right)\Rightarrow n_{O_2}=80\left(mol\right)\Rightarrow V_{O_2}=1792\left(l\right)\)
\(9,n_p=0,2\left(mol\right);n_{O_2}=0,3\left(mol\right)\)
\(PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
Vì\(\frac{0,2}{4}< \frac{0,3}{5}\)nên P hết O2 dư, bài toán tính theo P.
\(a,n_{O_2}\left(dư\right)=0,05\left(mol\right)\Rightarrow m_{O_2}\left(dư\right)=1,6\left(g\right)\)
\(b,n_{P_2O_5}=0,1\left(mol\right)\Rightarrow m_{P_2O_5}=14,2\left(g\right)\)
đủ cả 9 câu bạn nhé,