Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Dẫn 2 khí qua dung dịch Ca(OH)2
+ Xuấn hiện kết tủa trắng : CO2
CO2 + Ca(OH)2 ------> CaCO3 + H2O
+ Không hiện tượng: O2
b) Dẫn 2 khí qua dung dịch Ca(OH)2
+ Xuấn hiện kết tủa trắng : SO2
SO2 + Ca(OH)2 ------> CaSO3 + H2O
+ Không hiện tượng: O2
c) Cho quỳ tím vào các mẫu thử
+ Hóa xanh : NaOH
+ Hóa đỏ: H2SO4, HCl
+ Không đổi màu : NaCl
Cho dung dịch BaCl2 vào 2 mẫu thử làm quỳ tím hóa đỏ
+ Xuất hiện kết tủa trắng : H2SO4
BaCl2 + H2SO4 ------> BaSO4 + 2HCl
+ Không hiện tượng : HCl

a) - Hòa tan các chất rắn này vào nước sau đó dùng quỳ tím cho vào, quan sát:
+ Qùy tím hóa đỏ -> dd H3PO4 -> Rắn P2O5
PTHH: P2O5 +3 H2O -> 2 H3PO4
+ Qùy tím hóa xanh -> dd KOH -> Rắn KOH
PTHH: K2O + H2O -> 2 KOH

a. Trích mẫu thử, đánh số thứ tự
Sử dụng quỳ tím ẩm để nhận biết
- Quỳ hoá đỏ là \(P_2O_5\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
- Quỳ hoá xanh là CaO
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
b. Trích mẫu thử, đánh số thứ tự
Dẫn khí qua dung dịch \(Br_2\)
- Dung dịch \(Br_2\) mất màu là \(SO_2\)
\(SO_2+Br_2+2H_2O\rightarrow2HBr+H_2SO_4\)
- Không có hiện tượng là \(O_2\)

a)
Trích mẫu thử
Cho giấy quỳ tím ẩm vào :
- mẫu thử làm giấy quỳ tím hóa đỏ là $P_2O_5$
$P_2O_5 + 3H_2O \to 2H_3PO_4$
- mẫu thử làm giấy quỳ tím hóa xanh là $CaO$
$CaO + H_2O \to Ca(OH)_2$
b)
Trích mẫu thử
Sục mẫu thử vào nước vôi trong
- mẫu thử tạo kết tủa trắng là $SO_2$
- mẫu thử không hiện tượng là $O_2$

Bằng phương pháp hóa học nào có thể nhận biết từng chất trong mỗi chất sau đây:
a. Hai chất rắn màu trắng: CaO và P2O5
a) Cho nước vào hai ống nghiệm có chứa CaO và P2O5. Sau đó cho quỳ tím vào mỗi dung dịch:
- dung dịch nào làm đổi màu quỳ tím thành xanh là dung dịch bazơ, chất ban đầu là CaO.
- dung dịch nào làm đổi màu quỳ tím thành đỏ là dung dịch axit, chất ban đầu là P2O5
CaO + H2O → Ca(OH)2
P2O5 + 3H2O → 2H3PO4
b. Hai chất khí không màu: CO2 và O2
Dẫn lần lượt từng khí vào dung dịch nước vôi trong, nếu có kết tủa xuất hiện thì khí dẫn vào là CO2
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
Nếu không có hiện tượng gì thì khí dẫn vào là khí O2. Để xác định là khí O2 ta dùng que đóm còn than hồng, que đóm sẽ bùng cháy trong khí oxi.
c. MgO, CaO, P2O5 đều là những chất bột màu trắng.
Ta nhỏ nước sau đó nhúm quỳ tím
- chất tan làm quỳ chuyển đỏ là P2O5
- chất tan làm quỳ chuyển xanh là CaO
- chất ko tan là MgO
CaO + H2O → Ca(OH)2
P2O5 + 3H2O → 2H3PO4

b: Cho NaOH vào các mẫu thử.
Mẫu thử có khí bay lên là Al
Mẫu thử không có khí bay lên là Fe,Ag
Cho HCl vào hai mẫu thử còn lại.
Mẫu nào có khí bay lên là Fe
Còn lại là Ag

a) Trích một ít chất rắn làm mẫu thử :
Cho các chất hòa tan vào nước :
+ Tan : P2O5 , CaO
+ Không tan : MgO
Pt : \(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
Cho quỳ tím vào 2 mẫu thử tan :
+ Hóa đỏ : P2O5
+ Hóa xanh : CaO
Chúc bạn học tốt
a)
Trích mẫu thử
Cho giấy quỳ tím ẩm vào
- mẫu thử hóa đỏ là $P_2O_5$
- mẫu thử hóa xanh là $CaO$
- mẫu thử không đổi màu là $MgO$
$P_2O_5 + 3H_2O \to 2H_3PO_4$
$CaO + H_2O \to Ca(OH)_2$
b)
Cho quỳ tím vào mẫu thử :
- mẫu thử hóa xanh là $NaOH$
- mẫu thử hóa đỏ là $H_2SO_4$
- mẫu thử không đổi màu là $Na_2SO_4,NaCl$
Cho dung dịch $BaCl_2$ vào 2 mẫu thử còn
- mẫu thử tạo kết tủa trắng là $Na_2SO_4$
$BaCl_2 + Na_2SO_4 \to BaSO_4 + 2NaCl$
- mẫu thử không hiện tượng là $NaCl

- Trích mẫu thử.
- Hòa tan từng mẫu thử vào nước có quỳ tím.
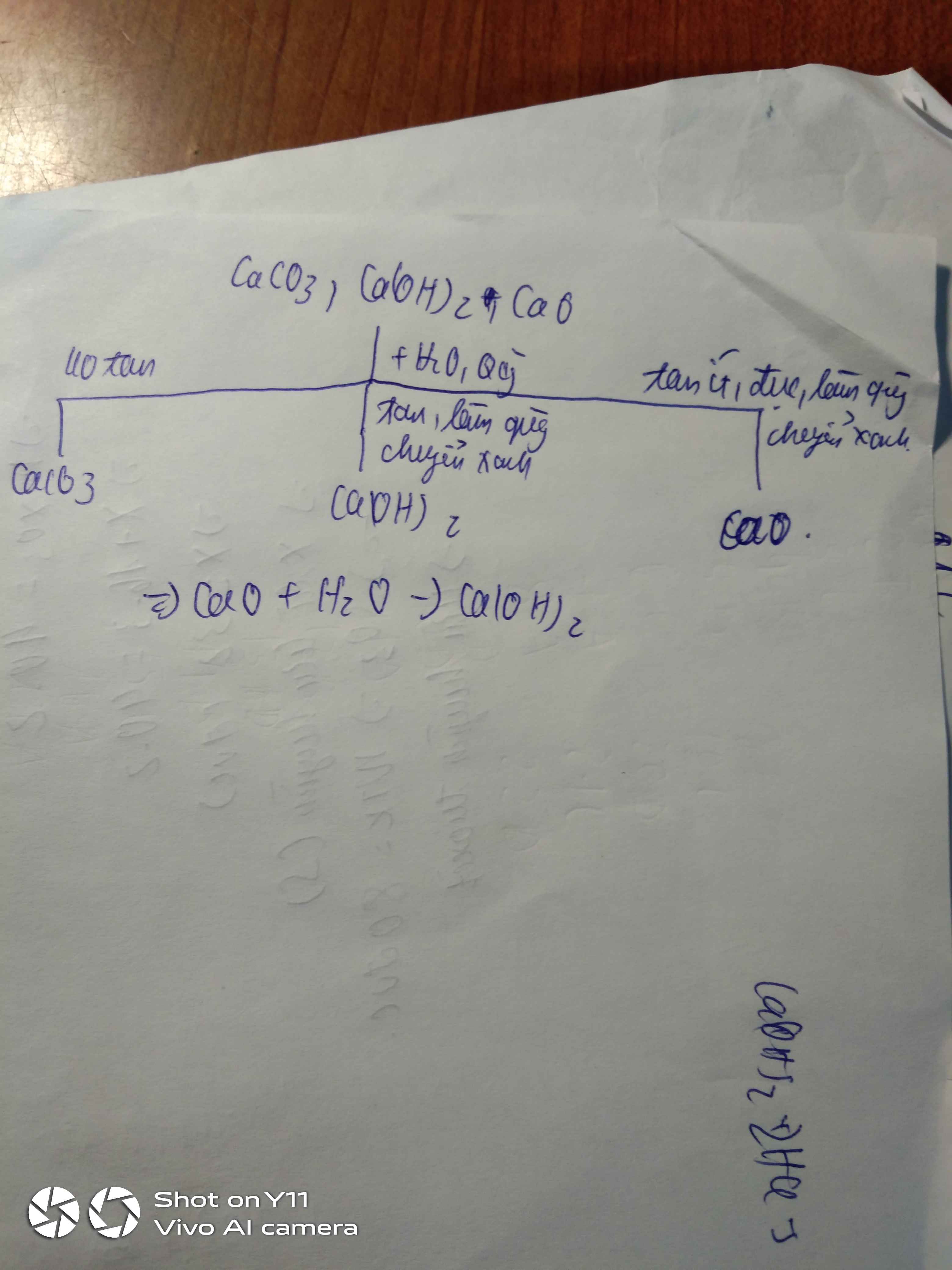
+ Không tan: CaCO3.
+ Tan, quỳ hóa xanh: CaO.
PT: \(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
+ Tan, quỳ hóa đỏ: P2O5.
PT: \(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
- Dán nhãn.
6.
a, Xuất hiện váng trắng CaCO3 do Ca(OH)2 pư với CO2 trong không khí.
b, PT: \(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
c, \(n_{CaCO_3}=\dfrac{11}{100}=0,11\left(mol\right)\)
Theo PT: \(n_{Ca\left(OH\right)_2}=n_{CaCO_3}=0,11\left(mol\right)\)
\(\Rightarrow m_{Ca\left(OH\right)_2}=0,11.74=8,14\left(g\right)\)
a. - Trích mẫu thử:
- Cho lần lượt nước và quỳ tím vào các mẫu thử:
+ Nếu tan và làm quỳ tím hóa đỏ là P2O5
P2O5 + 3H2O ---> 2H3PO4
+ Nếu tan và làm quỳ tím hóa xanh là CaO
CaO + H2O ---> Ca(OH)2
+ Không tan kaf MgO
b. - Trích mẫu thử:
- Cho quỳ tím vào các mẫu thử:
+ Nếu quỳ tím hóa đỏ là H2SO4
+ Nếu quỳ tím hóa xanh là NaOH
+ Nếu quỳ tím không đổi màu là NaCl và Na2SO4
- Cho BaCl2 vào NaCl và Na2SO4
+ Nếu có kết tủa trắng xuất hiện là Na2SO4
Na2SO4+BaCl2−−−>BaSO4↓+2NaClNa2SO4+BaCl2−−−>BaSO4↓+2NaCl
+ Không có phản ứng là NaCl
THAM KHẢO
làm đou đc hay vậy :V