
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Dù biết là bạn thân nhưng thực sự không thể nói, đủ can đảm mọi chuyện sẽ rõ
Câu 1:
1. Dẫn lần lượt 3 khí qua bình đựng dd AgNO3/NH3 dư, đun nóng nhẹ. Khí nào tạo kết tủa vàng nhạt với dd này là C2H2
CH≡CH + 2AgNO3 + 2NH3 --t*--> CAg≡CAg + 2NH4NO3
(bạc axetilua)
4 khí còn lại dẫn qua dd H2S, khí nào tạo ↓ vàng keo với H2S là SO2:
SO2 + 2H2S -> 3S↓ + 2H2O (phản ứng đặc trưng nhận biết SO2)
Khí còn lại dẫn qua dd Br2 màu vàng nâu (dư), khí nào làm nhạt màu Br2 là C2H4
C2H4 + Br2 -> C2H4Br2

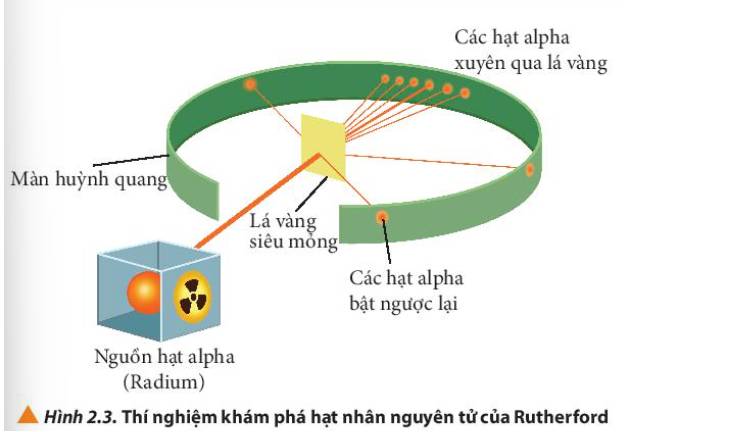
- Quan sát Hình 2.3 thấy được: hầu hết các hạt α đi thẳng, có vài hạt bị bắn theo đường gấp khúc
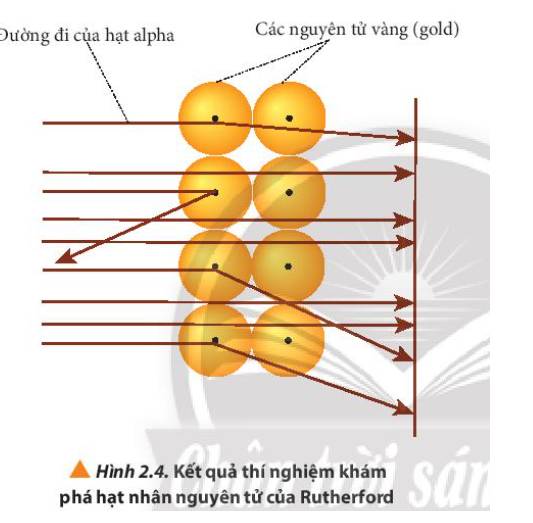
- Quan sát Hình 2.4 giải thích: các hạt α bị bắn theo đường gấp khúc là do va vào hạt nhân của nguyên tử vàng, các hạt không va vào hạt nhân thì đi thẳng
- Các hạt alpha hầu hết đều xuyên thẳng qua lá vàng, một số ít bị lệch hướng và một số rất ít bị bật ngược lại.
Giải thích: Do nguyên tử có cấu tạo rỗng, ở tâm chứa một hạt nhân mang điện tích dương có kích thước rất nhỏ so với kích thước nguyên tử nên hầu hết các hạt alpha có thể đi xuyên qua lá vàng.


Bài 5 :
Theo đề bài ta có : nHCl = \(\dfrac{36,5.20}{100.36,5}=0,2\left(mol\right)\)
Đặt tên kim loại có hóa trị cần tìm là R
PTHH :
\(R+2HCl->RCl2+H2\uparrow\)
0,1mol...0,2mol
=> MR = \(\dfrac{6,5}{0,1}=65\left(\dfrac{g}{mol}\right)\left(nh\text{ận}\right)\)
Vậy R là kim loại kẽm ( Zn = 65 )
Bài 4:
-Cấu hình e của X: 1s22s22p63s23p64s1(ZX=19: K)
-Cấu hình e của Y: 1s22s22p63s23p5(ZY=17:Cl)
-X: K2O và KOH

6.
tổng số p của chúng là 22=> ZA + ZB= 22 (1)
ta có 4<22<32 thì A,B thuộc chu kì nhỏ: ZB - ZA=8 (2)
từ (1) và (2) =>giải hệ pt được A=7; B=15 rồi viết cấu hình bình thường
bài 7 tượng tự nhé!!!
5.theo đề bài ,ta có hệ phương trình: \(\begin{cases}2Z+N=52\\-Z+N=1\end{cases}\)
giải hệ trên,ta được:\(\begin{cases}Z=17\\N=18\end{cases}\) => Z=17(Clo)
a)kí hiệu nguyên tử \(\frac{35}{17}Cl\)
b)Cấu hình electron: \(\left[Ne\right]3s^23p^5\)
Vậy Clo nằm ở chu kì 3(3 lớp),nhóm VIIA (có 7 e ngoài cùng)
bài 6 từ từ anh giải nhé


BT7
Gọi: a là thành phần % cuả đồng vị thứ nhất
b là thành phần % cuả đồng vị thứ hai
Ta có:
a+b=100 (1)
theo ct tính ngtử khối trung bình là
A= aA1 + bA2/100
=> 10a+11b/100=10.812
<=> 10a+11b=1081.2 (2)
Từ 1,2 ta có hệ
a+b=100
10a+11b=1081.2
=> a=18.8, b=81.2 <=> a= 19 , b = 81
BT7
b)
Gọi :a là thành phần % cuả đồng vị Cl thứ nhất
b là thành phần % cuả đồng vị Cl thứ hai
Ta có :
a+b=100 (1)
theo ct tính ngtử trung bình
A=\(\dfrac{aA_1+bA_2}{100}\)
=> \(\dfrac{35a+37b}{100}=35.5\)
<=> 35a +37b=3550 (2)
Từ 1.2 ta có hệ
a+b=100
35a+37b=3550
=> a=72% , b=25%

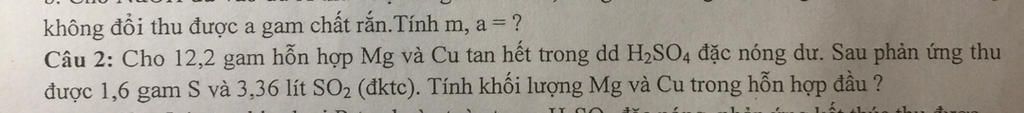






 giúp em với
giúp em với
 O
O
Gọi số mol Mg, Cu là a, b (mol)
=> 24a + 64b = 12,2 (1)
\(n_S=\dfrac{1,6}{32}=0,05\left(mol\right)\)
\(n_{SO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Mg0 - 2e --> Mg+2
a---->2a
Cu0 - 2e --> Cu+2
b---->2b
S+6 + 6e --> S0
0,3<-0,05
S+6 + 2e --> S+4
0,3<-0,15
Bảo toàn e: 2a + 2b = 0,6 (2)
(1)(2) => a = 0,175 (mol); b = 0,125 (mol)
=> \(\left\{{}\begin{matrix}m_{Mg}=0,175.24=4,2\left(g\right)\\m_{Cu}=0,125.64=8\left(g\right)\end{matrix}\right.\)