Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Oxit cao nhất của một nguyên tố là RO3, theo bảng tuần hoàn suy ra công thức hợp chất khí với hiđro của nó là RH2, trong phân tử RH2, có 5,88% H về khối lượng
nên R có 100 - 5,88 = 94,12% về khối lượng
Trong phân tử RH2, có: 5,88% H là 2u
94,12% R là x u
Giải ra ta có x ≈ 32. Nguyên tử khối của R = 32. R là S. Công thức phân tử là SO3 và H2S.

RH4 -> RO2
%R= 53,3% => %O = 100-53,3= 46,7%
\(\dfrac{R}{53,3}\)=\(\dfrac{32}{46,7}\)
giải tìm R

Nguyên tố X hợp với hidro cho hợp chất XH4 => Oxit cao nhất của X là XO2
Ta có : \(\frac{16\cdot2}{X+16\cdot2}\cdot100\%=53,3\%\)
\(\Rightarrow X=28\)(Silic)

Hợp chất khí với hidro của nguyên tố R là RH2. Oxit cao nhất của nguyên tố R chứa 60% oxi về khối lượng. Xác định nguyên tố R
===============
Hợp chất khí với hidro của nguyên tố R là RH2.
=> công thức với Oxi là RO
=>R/(R+16).100%=60%
<=>R/(R+16)=0,6
<=>0,4R=9,6
<=>R=24
=>R la Mg

Đáp án B
Vì công thức khí với hidro của R là RH3
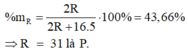
Vậy công thức oxit cao nhất của R là P2O5.

Đáp án B
Vì công thức khí với hidro của R là RH3
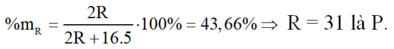
Vậy công thức oxit cao nhất của R là P2O5.



Hóa trị cao nhất trong oxit là 4, suy ra hóa trị của R trong hợp chất với hidro là 8 - 4 = 4
CTHH : $RH_4$
$\%H = \dfrac{4}{4 + R}.100\% = 12,5\% \Rightarrow R = 28(Silic)$
Vậy R là Silic