Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1)
- Xét phần 1:
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,2<-------------------0,2
=> nFe = 0,2 (mol)
- Xét phần 2:
\(n_{SO_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: 2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
0,2-->0,6-------->0,1--------->0,3
Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
0,3<----0,6<------0,3<-----0,3
=> nCu = 0,3 (mol)
m = 2.(0,2.56 + 0,3.64) = 60,8 (g)
2)
\(m_{H_2SO_4\left(bđ\right)}=\dfrac{200.98}{100}=196\left(g\right)\)
=> \(m_{H_2SO_4\left(sau.pư\right)}=196-98\left(0,6+0,6\right)=78,4\left(g\right)\)
mdd sau pư = \(\dfrac{60,8}{2}+200-0,6.64=192\left(g\right)\)
\(\left\{{}\begin{matrix}C\%_{\left(Fe_2\left(SO_4\right)_3\right)}=\dfrac{0,1.400}{192}.100\%=20,83\%\\C\%_{\left(CuSO_4\right)}=\dfrac{0,3.160}{192}.100\%=25\%\\C\%_{\left(H_2SO_4.dư\right)}=\dfrac{78,4}{192}.100\%=40,83\%\end{matrix}\right.\)

A + H2SO4 → Hỗn hợp khí ⇒ Fe dư; khí Y gồm: H2 ( x mol) và H2S (y mol)
⇒ x + y = 0,1 mol (1)
Bảo toàn S: nH2S = nFeS = nS = y mol
nFe dư = nH2 = x
Bảo toàn Fe: nFe = nFeS + nFe dư = x + y
mX = 56(x + y ) + 32y = 7,2g (2)
Từ (1)(2) ⇒ x = 0,05 mol; y = 0,05 mol
MY = mY : nY = (0,05.2 + 0,05.34) : 0,1 = 18 ⇒ dY/H2 = 9
Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{FeS}=b\left(mol\right)\end{matrix}\right.\left(đk:a,b>0\right)\)
TH1: S dư
Vậy toàn bộ lượng khí sinh ra là H2S
\(d_{Y\text{/}H_2}=d_{H_2S\text{/}H_2}=\dfrac{34}{2}=17\)
TH2: Fe dư
\(n_{khí}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Bảo toàn KL: \(m_A=m_X=7,2\left(g\right)\)
PTHH:
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
a----------------------------->a
\(FeS+2HCl\rightarrow FeCl_2+H_2S\uparrow\)
b-------------------------------->b
Ta có hệ phương trình: \(\left\{{}\begin{matrix}56a+88b=7,2\\a+b=0,1\end{matrix}\right.\)
\(\Leftrightarrow a=b=0,05\left(TM\right)\)
\(M_Y=\dfrac{0,05.\left(2+34\right)}{0,1}=18\left(g\text{/}mol\right)\\ \rightarrow d_{Y\text{/}H_2}=\dfrac{18}{2}=9\)

a,
Z: {H2S: aH2: b34a+2b=26(a+b)↔a=3bFeS+2HCl→FeCl2+H2SFe+2HCl→FeCl2+H2nFe=a+b=4b, nS=a=3bZ: {H2S: aH2: b34a+2b=26(a+b)↔a=3bFeS+2HCl→FeCl2+H2SFe+2HCl→FeCl2+H2nFe=a+b=4b, nS=a=3b
Từ đó tính phần trăm khối lượng ta được %Fe=70%, %S=30%
b,
Phần 2 có 3b mol FeS và b mol Fe
Kết tủa có BaSO4BaSO4
FeS→Fe3++1e+S+6+8eFe→Fe3++3eFeS→Fe3++1e+S+6+8eFe→Fe3++3e
Số mol e trao đổi là 9.3b+3b=30b
4H++SO2−4+2e→2H2O+SO2 15b 30b4H++SO42−+2e→2H2O+SO2 15b 30b
Có nH2SO4=55.0.9898=0.55nH2SO4=55.0.9898=0.55
Suyra nBaSO4=0.55−15b=0.25→b=0.02nBaSO4=0.55−15b=0.25→b=0.02




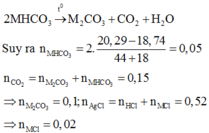
Ở mỗi phần, Y gồm FeS(x mol), Fe dư(y mol)
Phần 2 :
n H2SO4 = 55.98%/98 = 0,55(mol)
n SO4(trong A) = n BaSO4 = 58,25/233 = 0,25(mol)
Gọi n SO2 = z(mol)
Bảo toàn electron : 9x + 3y = 2z(1)
Bảo toàn S : x + 0,55 = 0,25 + z(2)
Phần 1 :
$Fe + 2HCl \to FeCl_2 + H_2$
$FeS + 2HCl \to FeCl_2 + H_2S$
n H2 = n Fe = y(mol)
n H2S = n FeS = x(mol)
M Z = 13.2 = 26
Suy ra: 34x + 2y = 26(x + y) (3)
Từ (1)(2)(3) suy ra x = 0,075 ; y = 0,025 ; z = 0,375
Suy ra :
1/2 X có :
n Fe = 0,075 + 0,025 = 0,1(mol)
n S = 0,075(mol)
Vậy :
a = (0,1.56 + 0,075.32).2 = 16 gam