
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


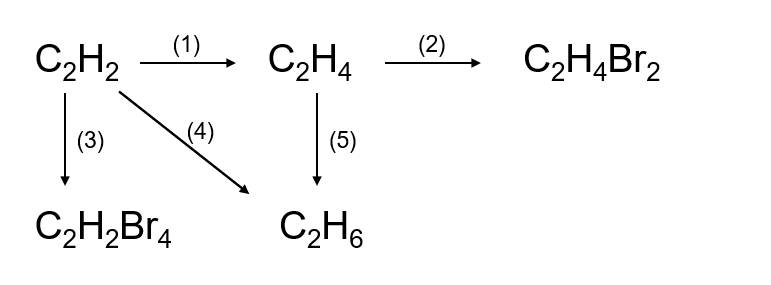
(1) \(2CH_4\xrightarrow[lln]{1500^oC}C_2H_2+3H_2\)
(2) \(C_2H_2+H_2\underrightarrow{t^o,Pd}C_2H_4\)
(3) \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
(4) \(CH_4+Cl_2\underrightarrow{as}CH_3Cl+HCl\)
(5) \(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
(6) \(C_2H_2+2H_2\underrightarrow{t^o,Ni}C_2H_6\)
(7) \(C_2H_4+H_2\underrightarrow{t^o,Ni}C_2H_6\)
(1) 2��4→���1500���2�2+3�22CH41500oCllnC2H2+3H2
(2) �2�2+�2��,��→�2�4C2H2+H2to,PdC2H4
(3) �2�4+��2→�2�4��2C2H4+Br2→C2H4Br2
(4) ��4+��2��→��3��+���CH


Câu 3:
N2+O2\(\overset{t^0}{\rightarrow}\)2NO
4NO+3O2+2H2O\(\rightarrow\)4HNO3
NO3- : làm tăng lượng phân đạm cho cây!

ta co
M=5.4 , O2=32 va M2O=10,2
==>5,4+32=2M+16
giai ra M=10,7~11
ma 11 la Na
cau tra loi minh chua chac dung nhe
\(4M+nO_2\rightarrow2M_2O_n\)
\(m_{oxit}=m_O+m_M\Rightarrow m_O=m_{oxit}-m_M=10,2-5.4=4,8\)
\(n_O=\frac{4,8}{16}=0,3\Rightarrow n_{O_2}=0,15\)
\(\Rightarrow n_M=\frac{4}{n}.0,15\Rightarrow M_M=\frac{5,4}{\frac{4}{n}.0,15}=9n\)
lập bảng ta được n=3 thi M=27 nên M là nhôm

nNO = 0.035mol
-hỗn hợp B gồm Fe và Fe3O4 dư
-muối trong dd Z là Fe(NO3)3 với số mol =\(\dfrac{18,15}{242}\) = 0.075mol
-toàn bộ Fe trong B( chính bằng Fe trong oxit ban đầu) đều đi vào muối \(\rightarrow\) nFe ban đầu = 0.075mol \(\rightarrow\) mFe ban đầu = 4.2g
\(\rightarrow\) mO trong oxit = 5,8-4,2=1.6g \(\rightarrow\) nO = 0.1mol
\(\rightarrow\)FexOy: \(\dfrac{x}{y}=\dfrac{0,075}{0,1}=\dfrac{3}{4}\)\(\rightarrow\)Fe3O4
Fe+ 2HCl\(\rightarrow\)FeCl2+H2
\(n_{Fe}=n_{H_2}=\dfrac{0,672}{22,4}=0,03mol\)\(\rightarrow\)mFe=0,03.56=1,68 g
\(n_{NO}=\dfrac{0,784}{22,4}=0,035mol\)
Fe+4HNO3\(\rightarrow\)Fe(NO3)3+NO+2H2O
3Fe3O4+28HNO3\(\rightarrow\)9Fe(NO3)3+NO+14H2O
\(n_{NO}=n_{Fe}+n_{Fe_3O_4}\)
\(\rightarrow\)\(n_{Fe_3O_4}=0,035-0,03=0,05mol\)
\(m_{Fe_3O_4}=0,05.232=11,6gam\)
%Fe=\(\dfrac{1,68.100}{1,68+11,6}\approx12,65\%\)
\(\%Fe_3O_4=100\%-12,65\%=87,35\%\)
4CO+Fe3O4\(\rightarrow\)4CO2+3Fe
\(n_{CO\left(pu\right)}=n_{CO_2\left(tt\right)}=4n_{Fe}=4.0,03=0,12mol\)
-Gọi số mol CO ban đầu là x.Hỗn hợp A có: 0,12 mol CO2 và x-0,12 mol CO
\(\rightarrow\)nA=0,12+x-0,12=x mol
\(\overline{M_A}=17,2.2=34,4\)
\(\rightarrow\)\(\dfrac{44.0,12+28\left(x-0,12\right)}{x}=34,4\)
\(\rightarrow\)44.0,12+28x-28.0,12=34,4x
\(\rightarrow\)6,4x=1,92\(\rightarrow\)x=0,3 mol
\(V_{CO}=0,3.22,4=6,72l\)
Trong A có: 0,12 mol CO2 và 0,3-0,12=0,18 mol CO
%CO2=\(\dfrac{0,12.100}{0,12+0,18}=40\%\)
%CO=60%

1. a) Tên gọi của axit:
HNO3: axit nitric
HCl: axit clohidric
H2CO3: axit cacbonic
H2S: axit sunfuhidric
H2SO4: axit sunfuric
H2SO3: axit sunfurơ
Axit mạnh: HCl, HNO3, H2SO4...
Axit yếu: H2S, H2CO3...


Bài 2) Ở 90 độ C:
- 100 gam nước hoà tan 50 gam KCl để tạo 150 gam dung dịch bão hoà ở nhiệt độ này
a) C% của dung dịch bão hoà tại 90 độ C là:
(Khối lượng chất tan/Khối lượng dung dịch) . 100%
<=> (50:150).100% = 33,33%
b) Ở 0 độ C:
Gọi m là khối lượng chất tan KCl ở 0o C => Khối lượng dung dịch tại nhiệt độ này là: 100+m
Theo đề bài ra ta có: m/100+m = 25,93%
=> m = 35 gam
Vậy ở 0 độ C độ tan của KCl trong nước là 35 gam
c) Ở 90 độ C:
100 gam nước hoà tan 50 gam KCl tạo 150 gam dd
=> 600 gam dung dịch tạo 200 gam KCl và 400 gam nước
- Ở 0 độ C:
100 gam nước hoà tan 35 gam KCl tạo 135 gam dd
=> 400 gam nước hoà tan được 140 gam KCl tạo 400 + 140 = 540 gam dung dịch
Vậy khi làm lạnh 600 gam dung dịch KCl từ 90 độ xuống 0 độ thì khối lượng dung dịch thu được là 540 gam

\(n_{H_2}=\dfrac{15,68}{22,4}=0,7mol\)
-Gọi số mol Al là x, số mol Mg là y
2Al+6HCl\(\rightarrow\)2AlCl3+H2
x\(\rightarrow\).............................\(\dfrac{3x}{2}\)
Mg+2HCl\(\rightarrow\)MgCl2+H2
y\(\rightarrow\).............................y
- Ta có hệ: \(\left\{{}\begin{matrix}27x+24y=15\\\dfrac{3x}{2}+y=0,7\end{matrix}\right.\)
Giải ra x=0,2 và y=0,4
mAl=27.0,2=5,4gam
mMg=24.0,4=9,6gam
%Al=\(\dfrac{5,4}{15}.100\%=36\%\)
%Mg=100%-36%=64%


 mn giúp e những câu còn lại ạ :)
mn giúp e những câu còn lại ạ :)










 Giúp mình giải vài câu thực tế Hoá nha..
Giúp mình giải vài câu thực tế Hoá nha.. giúp em giải câu đó với
giúp em giải câu đó với

 Giúp hộ mình nha !!!
Giúp hộ mình nha !!! Cảm ơn bạn !!!
Cảm ơn bạn !!!











Câu 3:
a, - Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Quỳ hóa đỏ: H2SO4
+ Quỳ hóa xanh: Ba(OH)2
+ Quỳ không đổi màu: Na2SO4, NaCl (1)
- Cho mẫu thử nhóm (1) pư với dd BaCl2
+ Có tủa trắng: Na2SO4
PT: \(BaCl_2+Na_2SO_4\rightarrow2NaCl+BaSO_4\)
+ Không hiện tượng: NaCl.
- Dán nhãn.
b, \(FeCl_2+\dfrac{1}{2}Cl_2\underrightarrow{t^o}FeCl_3\)
\(FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3+3NaCl\)
\(2Fe\left(OH\right)_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+6H_2O\)
\(Fe_2\left(SO_4\right)_3+3Ba\left(NO_3\right)_2\rightarrow2Fe\left(NO_3\right)_3+3BaSO_4\)
a)
\(Ba\left(OH\right)_2+Na_2SO_4\rightarrow BaSO_4+2NaOH\)
\(b)2FeCl_2+Cl_2\xrightarrow[]{t^0}2FeCl_3\\ FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3+3NaCl\\ 2Fe\left(OH\right)_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+6H_2O\)