Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Số electron : 12
Số đơn vị điện tích hạt nhân : + 12
Số hạt electron lớp ngoài cùng : 2
Số electron : 12
Số đơn vị điện tích hạt nhân : + 12
Số hạt electron lớp ngoài cùng : 2

Số e ngoài cùng của nguyên tử X mà anh, có phải tìm số p, n, e đâu ạ
`#3107.101107`
Gọi số hạt proton, neutron, electron trong nguyên tử X lần lượt là `p, n, e`
Tổng số hạt của nguyên tử X là `48`
`=> p + n + e = 48`
Mà trong nguyên tử, số `p = e`
`=> 2p + n = 48 (1)`
Số hạt mang điện gấp đôi số hạt không mang điện
`=> 2p = 2n (2)`
Từ `(1)` và `(2)`
`=> 2n + n = 48`
`=> 3n = 48`
`=> n = 48 \div 3`
`=> n = 16`
Vì `2p = 2n`
`=> 2p = 16*2`
`=> 2p = 32`
`=> p = 16`
Vậy, số `p, n, e` trong nguyên tử X là `16`
Ta có:
Lớp 1 của nguyên tử X: `2` electron
Lớp 2 ..... : `8` electron
Lớp 3 ..... : `6` electron
`=>` Số e lớp ngoài cùng của nguyên tử X là `6` electron.

Đầu tiên là F fluorine số electon 19 stt 9 chu kì 2 nhóm VIIA
Thứ 2 là sodium số electon 23 stt 11 chu kì 3 nhóm IA
Cuối cùng là scandium số electon là 45 stt 21 chu kì 4 nhóm IIIB

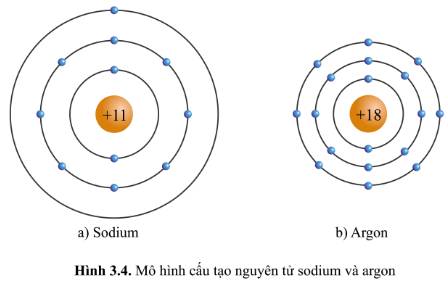
- Xét mô hình nguyên tử natri:
+ Số hiệu nguyên tử: 11
+ Điện tích hạt nhân: +11
+ Có 3 vòng tròn quanh hạt nhân => Số lớp electron = chu kì = 3
+ Có 1 hình tròn xanh ở vòng tròn ngoài cùng => Có 1 electron ở lớp ngoài cùng
- Xét mô hình nguyên tử argon:
+ Số hiệu nguyên tử: 18
+ Điện tích hạt nhân: +18
+ Có 3 vòng tròn quanh hạt nhân => Số lớp electron = chu kì = 3
+ Có 8 hình tròn xanh ở vòng tròn ngoài cùng => Có 8 electron ở lớp ngoài cùng
số e lớp ngoài cùng là 7e
Ta có : 1s22s22p5
Vậy số e lớp ngoài cùng là 7