Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) 4HCl + MnO2 --> MnCl2 + Cl2 +2H2O
2Fe + 3Cl2 ---> 2FeCl3
FeCl3 + 3NaOH --> Fe(OH)3 + 3NaCl
NaCl + H2SO4 đ---> NaHSO4 + HCl
2HCl + CuO ---> CuCl2 + H2O
CuCl2 +2AgNO3 ---> Cu(NO3)2 + 2AgCl
b) 2KMnO4 + 16HCl ---> 2KCl + 2MnCL2 +5Cl2 +8H2O
Cl2 + H2--->2HCl
6HCl + Fe2O3 ---> 2FeCl3 +3H2O
FeCl3 + 3AgNO3 --> Fe(NO3)3 +3AgCl
2AgCl --to---> 2Ag + Cl2
Cl2 + 2NaBr ---> 2NaCl + Br2
Br2 + 2NaI --> 2NaBr + I2
I2 +Zn --to--> ZnI2
ZnI2 + 2NaOH --> Zn(OH)2 +2NaI
c) 2KCl ---dpnc--> 2K + Cl2
Cl2 + 2KOH --> KCl + KClO + H2O
4KClO --> KClO3 +3 KCl
4KClO3 ---> 3KClO4 + KCl
3KClO4 + 8Al ---> 4Al2O3 + 3KCl
KCl + AgNO3 --> AgCl + KNO3
d) 3Cl2 + 6KOH ---> KClO3 + 5KCl +3H2O
2KClO3 ---> 2KCl +#O2
2KCl --> 2K + Cl2
2Cl2 + Ca(OH)2 ---> CaCl2 +Ca(ClO)2
Ca(ClO)2 ---> CaCl2 + O2
CaCl2 ---> Ca + Cl2
Cl2 ra O2 ????
e)6HCl + KClO3 ---> KCl +3Cl2 +3H2O
3Cl2 +6KOH --> 5KCl + KClO +3 H2O
2KClO3 --> 2KCl + 3O2
2KCl --> 2K + CL2
CL2 +H2 --> 2HCl
2HCl +Fe--> FeCl2 + H2
Cl2 + 2FeCl2 -->2FeCl3
FeCl3 +3NaOH --> Fe(OH)3 +3NaCl

a/
\(2HCl\underrightarrow{^{đpdd}}H_2+Cl_2\)
\(3Cl_2+2Fe\underrightarrow{^{to}}2FeCl_3\)
\(FeCl_3+3NaOH\rightarrow3NaCl+Fe\left(OH\right)_3\)
\(2NaCl+H_2SO_4\underrightarrow{^{to}}Na_2SO_4+2HCl\)
\(HCl+CuO\rightarrow CuCl_2+H_2O\)
\(CuCl_2+AgNO_3\rightarrow AgCl+Cu\left(NO_3\right)2\)
b/
\(2HCl\underrightarrow{^{đpdd}}H_2+Cl_2\)
\(Cl_2+2Na\underrightarrow{^{to}}2NaCl\)
\(2NaCl+H_2SO_{4_{dac}}\underrightarrow{^{to}}Na_2SO_4+2HCl\)
\(2HCl+Fe\rightarrow FeCl_2+H_2\)
c/
\(MnO_2+4HCl_đ\underrightarrow{^{to}}MnO_2+Cl_2+2H_2O\)
\(Cl_2+2K\underrightarrow{^{to}}2KCl\)
\(2KCl+H_2SO_4\underrightarrow{^{to}}K_2SO_4+2HCl\)
\(2HCl\underrightarrow{^{đpdd}}H_2+Cl_2\)
\(Cl_2+2NaBr\rightarrow2NaCl+Br_2\)
\(Br_2+2NaI\rightarrow NaBr+I_2\)
d/
\(2KMnO_4+16HCl_đ\underrightarrow{^{to}}2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(Cl_2+H_2\underrightarrow{^{as}}2HCl\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
\(FeCl_3+3AgNO_3\rightarrow3AgCl+Fe\left(NO_3\right)_3\)

a) (1) MnO2 + 4 HCl(đặc) -to-> MnCl2 + Cl2 + 2 H2O
(2) Cl2 + H2 \(\Leftrightarrow\) 2 HCl
(3) HCl + NaOH -> NaCl + H2O
(4) 2 NaCl + 2 H2O -đpddcmnx-> 2 NaOH + H2 + Cl2
(5) Cl2 + 2 H2O + SO2 -> H2SO4 + 2 HCl
(6) H2SO4 + BaCl2 -> BaSO4 + 2 HCl
b)
(1) BaCl2 -điện phân nóng chảy nhiệt độ cao-> Ba + Cl2
(2) Cl2 + H2 \(\Leftrightarrow\) 2 HCl
(3) Fe + 2 HCl -> FeCl2 + H2
(4) 2 FeCl2 + Cl2 -to-> 2 FeCl3
(5) 2 FeCl3 + 3 Ba(OH)2 -> 2 Fe(OH)3 +3 BaCl2
(6) BaCl2 + H2SO4 -> BaSO4 + 2 HCl
c) (1) BaCl2 + H2SO4 -> BaSO4 +2 HCl
(2) 2 HCl + CuO -> CuCl2 + H2O
(3) CuCl2 + 2 KOH -> Cu(OH)2 + 2 KCl
(4) KCl + H2O -đpddcmnx-> KOH + 1/2 Cl2 + 1/2 H2
(5) 6 KOH + 3 Cl2 -to->5 KCl + KClO3 +3 H2O
(6) 2 KClO3 -to-> 2 KCl + 3 O2
a)
(1) MnO2 + 4HCl(đ) -to-> MnCl2 + Cl2 + 2H2O
(2) Cl2 + H2 <-as-> 2 HCl
(3) HCl + NaOH => NaCl + H2O
(4) 2NaCl + 2H2O -đpddcmn-> 2NaOH + H2 + Cl2
(5) Cl2 + 2H2O + SO2 => H2SO4 + 2HCl
(6) H2SO4 + BaCl2 => BaSO4 + 2HCl
b)
(1) BaCl2 -đpdd-> Ba + Cl2
(2) Cl2 + H2 ⇔ 2HCl (Đk : ánh sáng hoặc nhiệt độ)
(3) Fe + 2HCl => FeCl2 + H2
(4) 2FeCl2 + Cl2 -to-> 2FeCl3
(5) 2FeCl3 + 4Ba(OH)2 => 2Fe(OH)3 + 3BaCl2
(6) BaCl2 + H2SO4 => BaSO4 + 2HCl
c)
(1) BaCl2 + H2SO4 => BaSO4 +2HCl
(2) 2HCl + CuO => CuCl2 + H2O
(3) CuCl2 + 2KOH => Cu(OH)2 + 2KCl
(4) 2KCl + 2H2O -đpddcmn-> 2KOH + Cl2 + H2
(5) 6KOH + 3Cl2 -to-> 5KCl + KClO3 +3H2O
(6) 2KClO3 -to-> 2KCl + 3O2

a)
Giả sử lấy lượng mỗi chất là a gam.
MnO2 + 4HCl \(\rightarrow\) MnCl2 + Cl2 + 2H2O (1)
2KMnO4 + 14 HCl \(\rightarrow\)2MnCl2 + 2KCl + 5Cl2 + 8H2O (2)
K2Cr2O7 + 14 HCl \(\rightarrow\)2CrCl2 + 2KCl + 3Cl2 + 7H2O (3)
Vậy dùng : KMnO4 điều chế được nhiều Cl2 hơn
b) Nếu số mol các chất bằng n mol
Theo (1) nmol MnO2 \(\rightarrow\) nmol Cl2
Theo (2) nmol KMnO4 \(\rightarrow\) 2,5 nmol Cl2
Theo (3) nmol K2Cr2O7 \(\rightarrow\) 3nmol Cl2
Ta có: 3n > 2,5n > n
Vậy dùng K2Cr2O7 được nhiều hơn Cl2 hơn
Clo oxi hóa dễ dàng Br – tronh dung dịch muối bromua và I- trong dung dịch muối iotua.
Cl2 + 2NaBr \(\rightarrow\) 2NaCl + Br2
Cl2 + 2NaI \(\rightarrow\) 2NaCl + I2

a) Số oxi hóa của S trong các chất: H2, S-2 , S0, H2S+4O3, H2S+6O4
b) Số oxi hóa của Cl trong các hợp chất: HCl-1, HCl+1O, NaCl+3O2, HCl+5O3, HCl+7O4.
c) Số oxi hóa của Mn trong các chất: Mn0, Mn+2Cl2, Mn+4O2, KMn+7O4
d) 

b>
Giả sử mỗi chất đều có khối lượng là 1 gam
nKMnO4=0,00633mol
nKClO3=0,00816mol
nMnO2=0,0115mol
nK2Cr2O7=0,0034mol
Các phản ứng :
2KMnO4 + 16HCl -> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,00663 --------------------------- →0,0158
KClO3 + 6HCl -> KCl + 3Cl2 + 3H2O
0,00816 -------------- → 0,0245
MnO2 + 4HCl -> MnCl2 + Cl2 + 2H2O
0,0115------------------- → 0,0115
K2Cr2O7 + 14HCl -> 2KCl + 2CrCl3 + 3Cl2 + 7H2O
0,0034 ---------------------------------- →0,0102
=> Chất cho lượng khí lớn nhất là Cl2 : KClO3.

Đặt X là số oxi hoá của nguyên tố ni tơ trong các hợp chất trên ta có
Trong NO: x + (-2) = 0 -> X = +2
Trong NO2: x + 2(-2) = 0 -> x = +4
Trong N2O5 : 2x + 5(-2) = 0 \(\rightarrow\) x = +5
Trong HNO3 : (+1) + x + 3(-2) = 0 \(\rightarrow\) X = +5
Trong HNƠ2 : (+1) + x + 2(-2) = 0 \(\rightarrow\) X = +3
Trong NH3 : X + 3(+l) = 0 \(\rightarrow\) X = -3
Trong NH4Cl: X + 4(+l) + (-1) = 0 \(\rightarrow\) X = -3.
Cũng giải tương tự như trên ta có:
.jpg)
- Đặt x là oxi hóa của nguyên tố nitơ trong các hợp chất trên, ta có:
Trong NO: x + (-2) = 0 → x = +2.
Trong NO2: x + 2(-2) = 0 → x = +4.
Trong N2O5: 2x + 5(-2) = 0 → x = +5.
Trong HNO3: (+1) +x + 3(-3) = 0 → x = +5.
Trong HNO2: (+1) + x +2(-2) = 0 → x = +3.
Trong NH3 : x + 3(+1) = 0 → x = -3.
Trong NH3Cl: x + 4(+1) +(-1) = 0 → x = -3.
- Cũng giải tương tự như trên ta có:


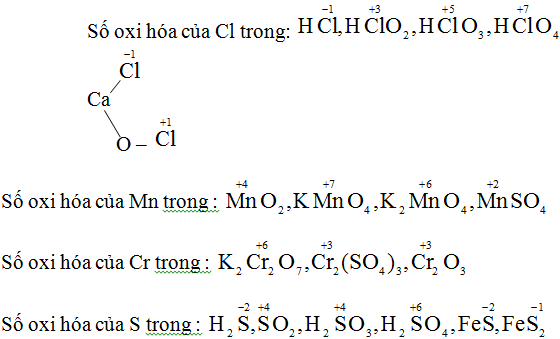
Đáp án B
16HCl + 2KMnO4→ 5Cl2+ 2MnCl2+ 2KCl+8H2O
m/15 → m/63,2
6HCl + KClO3 →3Cl2+ KCl+3H2O
m/122,5→ m/40,8
4HCl + MnO2→ Cl2+ MnCl2+ 2H2O
m/87 → m/87
So sánh thấy nếu lấy cùng 1 lượng các chất phản ứng với HCl thì KClO3 cho nhiều khí Cl2 nhất